┴_Ąż├„BÅU╦«╣ż╦ć
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2014-12-20 10:15:00
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
╚Š┴ŽÅU╦«Š▀ėą╬█╚Š╬’ØŌČ╚Ė▀Īó╔½Č╚╔ŅĪóļy╔·╬’ĮĄĮŌĄ╚╠ž³cŻ¼ęūę²░lįSČÓŁhŠ│╬█╚Šå¢Ņ}ĪŻį┌╠ĮīżĖ▀ą¦ĪóĮøØ·Ąž╠Ä└Ē╚Š┴ŽÅU╦«Ą─ųTČÓĘĮĘ©ųąŻ¼Fentonįćä®č§╗»Ę©ę“ŲõĘ┤æ¬╦┘┬╩┐ņĪó▓┘ū„║åå╬Ą╚ā׳céõ╩▄ųžęĢĪŻĄ½╩Ūé„ĮyĄ─Fentonįćä®č§╗»¾wŽĄąĶę¬į┌▌^Ą═Ą─pHĘČć·Ż©ąĪė┌4Ż®ā╚Ę┤æ¬Ż¼ŪęĶFļxūėĄ─Ęųļx║═ųžÅ═└¹ė├ę▓╩▄ĄĮę╗Č©Ž▐ųŲĪŻ×ķ┴╦į┌Ė³īÆĄ─pHĘČć·ā╚▀MąąĘ┤æ¬▓ó╩╣┤▀╗»ä®Ą├ĄĮ│õĘų└¹ė├Ż¼Ė³ČÓĄ─蹊┐┌ģŽ“ė┌ĘŪŠ∙ŽÓFentonįćä®č§╗»Ę┤æ¬┤▀╗»ä®Ą─čąųŲĪŻė╔ė┌Feį┌ūį╚╗Įń║¼┴┐žSĖ╗Ż¼ī”ŁhŠ│¤oČŠŻ¼Fe- H2O2 ¾wŽĄ╝░Ųõ±Ņ║Ž╝╝ąg▒╗ÅVĘ║蹊┐Ż¼╚ńLuckingĄ╚ęįH2O2×ķč§╗»ä®Ż¼ęįFeĘ█Īó╩»─½Īó╗Ņąį╠┐×ķ┤▀╗»ä®ĮĄĮŌ╦«ųąĄ─4-┬╚ĘėŻ¼╦¹éāšJ×ķFeĘ█┐╔ęį┤·╠µFe¹}ū„×ķFentonįćä®č§╗»Ę┤æ¬Ą─┤▀╗»ä®ĪŻ┤╦═ŌŻ¼╬ó▓©╝╝ągę▓ÅVĘ║æ¬ė├ė┌ėąÖC╬’Ą─ĮĄĮŌųąŻ¼╬ó▓©▓╗āH─▄Ė─ūā¾wŽĄĄ─¤ß┴”īW║»öĄŻ¼ĮĄĄ═Ę┤æ¬Ą─╗Ņ╗»─▄║═ĘųūėĄ─╗»īWµIÅŖČ╚Ż¼▀Ć┐╔ęį┤┘▀Mę╗ą®ļyęį▀MąąĄ─Ę┤æ¬Ą─░l╔·Ż¼ę“┤╦╬ó▓©╝╝ągį┌╗»īW║Ž│╔ĪóŁhŠ│╣ż│╠ŅIė“Ą├ĄĮ┴╦ÅVĘ║Ą─æ¬ė├ĪŻ
▒Š╣żū„ęį┴_Ąż├„B─ŻöMÅU╦«×ķ╠Ä└Ēī”Ž¾Ż¼┐╝▓ņ╬ó▓©▌oų·Fe-H2O2ģf═¼ū„ė├ī”Ė▀ØŌČ╚┴_Ąż├„BÅU╦«Ą─├ō╔½ą¦╣¹Ż¼▓ó╠Įėæ┴╦▓╗═¼ė░Ēæę“╦žī”┴_Ąż├„B╚ź│²ą¦╣¹Ą─ė░ĒæĪŻ
1 īŹ“×▓┐Ęų
1.1 įćä®║═āxŲ„
┴_Ąż├„BŻ║Ęų╬÷╝āŻ╗ļpč§╦«Ż║┘|┴┐ĘųöĄ30%Ż¼Ęų╬÷╝āŻ╗FeĘ█Ż║▀^100─┐║YŻ¼Ęų╬÷╝āĪŻ
pH S-3Są═pHėŗŻ║╔Ž║Ż└Ē▀_āxŲ„ÅSŻ╗UV-2450ą═ūŽ═Ō-┐╔ęŖĘų╣Ō╣ŌČ╚ėŗŻ║╚š▒ŠŹuĮ“╣½╦ŠŻ╗╬ó▓©Ę┤æ¬Ų„Ż║Ė±╠m╩╦╬ó▓©ĀtūįąąĖ─čbĪŻ
1.2 īŹ“×ĘĮĘ©
╚Ī200 mLę╗Č©┘|┴┐ØŌČ╚Ą─ÅU╦«Ż¼ė├ØŌČ╚×ķ0.1mol/LĄ─HNO3╚▄ę║╗“ØŌČ╚×ķ0.1 mol/L Ą─NaOH╚▄ę║š{╣ØÅU╦«pHŻ¼╝ė╚ļFeĘ█║═┘|┴┐ĘųöĄ30%Ą─H2O2ĪŻį┌300 W╬ó▓©▌Ś╔õŽ┬Ę┤æ¬ę╗Č╬ĢrķgŻ¼╚ĪśėĘų╬÷ĪŻ£yČ©ĢrīóÅU╦«ŽĪßī10▒ČŻ¼ė┌▓©ķL552 nm╠Ä£yŲõ╬³╣ŌČ╚ĪŻ
2 ĮY╣¹┼cėæšō
2.1 ÅU╦«pHī”┴_Ąż├„B╚ź│²┬╩Ą─ė░Ēæ
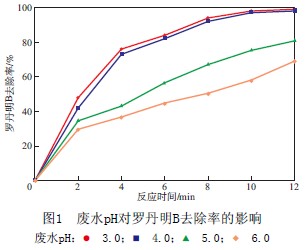
«ö│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚×ķ100 mg/LĪóFeĘ█╝ė╚ļ┴┐×ķ50 mg/LĪóH2O2╝ė╚ļ┴┐×ķ10.0 mL/LĢrŻ¼ÅU╦«pHī”┴_Ąż├„B╚ź│²┬╩Ą─ė░ĒæęŖłD1ĪŻė╔łD1┐╔ęŖŻ║«öÅU╦«pH×ķ3.0║═4.0ĢrŻ¼┴_Ąż├„B╚ź│²┬╩ļSĘ┤æ¬ĢrķgčėķLČ°čĖ╦┘į÷┤¾Ż¼ÅU╦«├ō╔½═Ļ╚½Ż╗ļSų°ÅU╦«pH╔²Ė▀Ż¼┴_Ąż├„B╚ź│²┬╩£pąĪŻ¼├ō╔½╦┘┬╩ūā┬²ĪŻ▀@╩Ūė╔ė┌ÅU╦«pHė░Ēæ┴╦Feį┌╦«╚▄ę║ųąĄ─╗»īWĘ┤æ¬ĪŻ«öÅU╦«pH▌^Ą═ĢrŻ¼Fe▒╗č§╗»│╔Fe2+Ż¼Fe2+▀MČ°┼cH2O2ū„ė├╔·│╔┴u╗∙ūįė╔╗∙Ż¼Å─Č°č§╗»╚ź│²┴_Ąż├„BŻ╗Č°į┌▌^Ė▀pHŚl╝■Ž┬Ż¼ĶFļxūėĄ─╦«ĮŌū„ė├│╔×ķų„ę¬Ę┤æ¬Ż¼FeĄ─Üõč§╗»╬’│┴ĄĒĖĮų°ė┌FeĘ█Ą─▒Ē├µŻ¼ūĶĄK┴╦Fe2+Ą─╚▄│÷ęį╝░Fe3+Ą─裣h└¹ė├ĪŻ═¼ĢrŻ¼H2O2į┌ÅŖēAąįŚl╝■Ž┬▌^ęūĘųĮŌŻ¼▓╗└¹ė┌Ųõ└¹ė├ĪŻ
ę╗░ŃšJ×ķé„ĮyFentonįćä®č§╗»Ę©Ą─ūŅ╝čpH×ķ3.0Ż¼ŪęČ╝╩Ūį┌╦ßąįŚl╝■Ž┬▓┼─▄▀MąąĪŻČ°╬ó▓©▌oų·Fe-H2O2¾wŽĄ─▄ē“į┌ÅU╦«pH×ķ4.0Ģr╚į─▄▀_ĄĮ▌^┐ņ▌^║├Ą─╠Ä└Ēą¦╣¹Ż¼Ę┤æ¬12 minĢr┴_Ąż├„BĄ─╚ź│²┬╩×ķ98.7%Ż¼╣╩į┌įō¾wŽĄŽ┬Fentonįćä®č§╗»Ę┤æ¬Ą─pHĘČć·▒╚é„ĮyĄ─Fentonįćä®č§╗»Ę┤æ¬īÆĪŻ
2.2 H2O2╝ė╚ļ┴┐ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░Ēæ
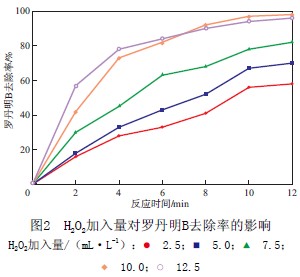
«ö│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚×ķ100 mg/LĪóÅU╦«pH×ķ4.0ĪóFeĘ█╝ė╚ļ┴┐×ķ50 mg/LĢrŻ¼H2O2╝ė╚ļ┴┐ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░ĒæęŖłD2ĪŻė╔łD2┐╔ęŖŻ║ļSų°H2O2╝ė╚ļ┴┐Ą─į÷╝ėŻ¼┴_Ąż├„B╚ź│²┬╩į÷┤¾Ż╗«öH2O2╝ė╚ļ┴┐ąĪė┌10.0 mL/LĢrŻ¼┴_Ąż├„B▓╗─▄▒╗═Ļ╚½╚ź│²Ż¼▀@ų„ę¬╩Ūė╔ė┌«öH2O2▌^╔┘ĢrÅU╦«ųąø]ėąūŃē“Ą─Fe2+«a╔·Ż¼Ą½ļSų°H2O2╝ė╚ļ┴┐į÷╝ėĄĮ12.5 mL/LĢrŻ¼┴_Ąż├„B╚ź│²┬╩▌^H2O2╝ė╚ļ┴┐×ķ10.0 mL/LĢr╬┤ėą├„’@Ė─ūāĪŻ«ö═Č╝ė▀^┴┐Ą─H2O2ĢrŻ¼H2O2 ═¼ĢrĢ■│õ«öūį╔ĒĄ─Ž¹│²ä®Ż¼Å─Č°£p╔┘┴╦ÅU╦«ųą┴u╗∙ūįė╔╗∙Ą─┴┐ĪŻę“┤╦Ż¼į┌▒ŠīŹ“×ųąŻ¼H2O2Ą─ūŅ╝č╝ė╚ļ┴┐×ķ10.0 mL/LĪŻ
2.3 FeĘ█╝ė╚ļ┴┐ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░Ēæ
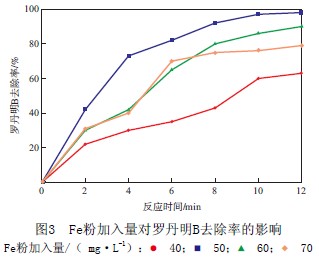
«ö│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚×ķ100 mg/LĪóÅU╦«pH×ķ4.0ĪóH2O2Ą─╝ė╚ļ┴┐×ķ10.0 mL/LĢrŻ¼FeĘ█╝ė╚ļ┴┐ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░ĒæęŖłD3ĪŻė╔łD3┐╔ęŖŻ║«öFeĘ█╝ė╚ļ┴┐×ķ40 mg/LĢrŻ¼┴_Ąż├„BĄ─╚ź│²┬╩▌^Ą═Ż╗«öFeĘ█╝ė╚ļ┴┐×ķ50 mg/LĢrŻ¼Ę┤æ¬ĢrķgŽÓ═¼ĢrŻ¼┴_Ąż├„B╚ź│²┬╩ūŅ┤¾Ż¼šf├„╚ź│²╦┘┬╩▌^┐ņŻ╗«öFeĘ█╝ė╚ļ┴┐└^└mį÷┤¾ĢrŻ¼┴_Ąż├„B╚ź│²┬╩£pąĪŻ¼╚ź│²ą¦╣¹Ž┬ĮĄĪŻ▀@ĘN¼FŽ¾ų„ę¬╩Ūę“×ķFeĘ█Ą─╝ė╚ļ┴┐▓╗═¼Ż¼ė░ĒæFe2+Ą─╚▄│÷Ż¼Č°▀^┴┐Ą─Fe2+═¼śėĢ■│╔×ķ┴u╗∙ūįė╔╗∙Ą─Ž¹│²ä®ĪŻį┌▒ŠīŹ“×ųąŻ¼FeĘ█ūŅ╝č╝ė╚ļ┴┐×ķ50 mg/LĪŻ
2.4 │§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░Ēæ
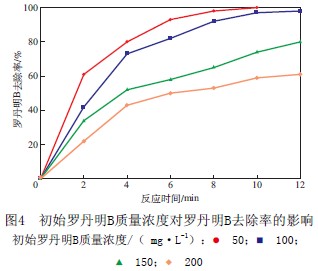
«öÅU╦«pH×ķ4.0ĪóH2O2Ą─╝ė╚ļ┴┐×ķ10.0 mL/LĪóFeĘ█╝ė╚ļ┴┐×ķ50 mg/LĢrŻ¼│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚ī”┴_Ąż├„B╚ź│²┬╩Ą─ė░ĒæęŖłD4ĪŻė╔łD4┐╔ęŖŻ║ļSų°│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚Ą─į÷╝ėŻ¼Ųõ╚ź│²┬╩£pąĪŻ╗«ö│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚×ķ50 mg/LĪóĘ┤æ¬10 minĢrŻ¼┴_Ąż├„BĄ─╚ź│²┬╩ęč▀_ĄĮ100%Ż¼«ö│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚Ęųäe×ķ100Ż¼150Ż¼200 mg/LĢrŻ¼Ę┤æ¬12 min┴_Ąż├„BĄ─╚ź│²┬╩Ęųäe×ķ98.7%Ż¼74.5%Ż¼59.8%ĪŻ▀@ų„ę¬╩Ūė╔ė┌│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚Ė▀Ż¼ÅU╦«ųą┴u╗∙ūįė╔╗∙╝░Ųõ╦¹č§╗»ä®║¼┴┐ŽÓī”▌^╔┘Ż¼═¼ĢrŻ¼ĮĄĮŌ▀^│╠ųąĄ─ųąķg«a╬’Ą─┴┐ę▓Ģ■▌^ČÓŻ¼ī¦ų┬┴_Ąż├„B╚ź│²╦┘┬╩Ž┬ĮĄĪŻ
2.5 ī”▒╚īŹ“×
į┌╔Ž╩÷ūŅ╝čīŹ“׌l╝■Ž┬Ż¼▓╗═¼Ę┤款wŽĄī”┴_Ąż├„B╚ź│²┬╩Ą─ė░ĒæęŖłD5ĪŻ
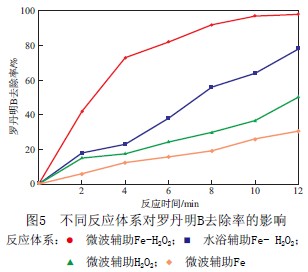
ė╔łD5┐╔ęŖŻ¼į┌╦«įĪ▌oų·Fe-H2O2Īó╬ó▓©▌oų·H2O2║═╬ó▓©▌oų·Fe¾wŽĄųąĖ„Ę┤æ¬12 min║¾Ż¼┴_Ąż├„B╚ź│²┬╩Ęųäe▀_ĄĮ78.1%Ż¼50.2%Ż¼30.8%Ż¼▀h▀hĄ═ė┌╬ó▓©▌oų·Fe-H2O2¾wŽĄī”┴_Ąż├„BzĄ─╚ź│²┬╩Ż¼┐╔ęŖ╬ó▓©ī”Fe-H2O2╠Ä└Ē┴_Ąż├„BĄ─╚ź│²Š▀ėą▌^ÅŖĄ─▌oų·ū„ė├ĪŻ
į┌╬ó▓©▌oų·Fe¾wŽĄųąŻ¼╬ó▓©ū„ė├ė┌FeĘ█─▄ę²ŲŲõ▒Ē├µčĖ╦┘╔²£žŻ¼1 min─▄▀_ĄĮ370~540 ĪµĪŻĖ▀£ž║═╦ßąįŁhŠ│Ė─ūā┴╦FeĘ█▒Ē├µąį┘|Ż¼▓ó╬³ĖĮ▓┐Ęų┴_Ąż├„BŻ¼▀@ā╔ĘĮ├µū„ė├╩╣╚▄ę║ųą┴_Ąż├„B▓┐ĘųĮĄĮŌĪŻį┌╬ó▓©▌oų· H2O2¾wŽĄŽ┬Ż¼┴_Ąż├„BĄ─╚ź│²┬╩×ķ50.2%Ż¼▀@╩Ūę“×ķH2O2į┌╬ó▓©▌Ś╔õŽ┬─▄ē“«a╔·░³└©┴u╗∙ūįė╔╗∙į┌ā╚Ą─ę╗ą®ūįė╔╗∙Ż¼┐╔╩╣┴_Ąż├„BĮĄĮŌĪŻ
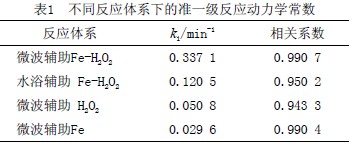
ī”▓╗═¼Ę┤款wŽĄųą┴_Ąż├„BĄ─╚ź│²Ę┤æ¬▀Mąą┴╦äė┴”īWöM║ŽŻ¼ĮY╣¹×ķ£╩ę╗╝ēäė┴”īWĪŻ▓╗═¼Ę┤款wŽĄŽ┬Ą─£╩ę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄęŖ▒Ē1ĪŻė╔▒Ē1┐╔ęŖŻ¼╬ó▓©▌oų·Fe-H2O2¾wŽĄĮĄĮŌ┴_Ąż├„BĄ─k1▀h▀h┤¾ė┌Ųõ╦¹Ę┤款wŽĄĪŻį┌╬ó▓©Ą─ū„ė├Ž┬Ż¼ĮĄĄ═┴╦╬ó▓©▌oų·Fe-H2O2¾wŽĄĄ─Ę┤æ¬╗Ņ╗»─▄Ż¼▓óŪę╩╣Fe║═H2O2Ę┤æ¬╝ė┐ņŻ¼┤┘▀M┴u╗∙ūįė╔╗∙Ą─╔·│╔Ż¼╝ė╦┘┴_Ąż├„BĄ─╚ź│²ĪŻ
2.6 FeĘ█Ą─ųžÅ═╩╣ė├
į┌╬ó▓©▌oų·Fe-H2O2¾wŽĄūŅ╝čīŹ“׌l╝■Ž┬▀MąąFeĘ█ųžÅ═└¹ė├īŹ“×ĪŻĘ┤æ¬Ģrķg×ķ12 minŻ¼├┐ę╗┤╬īŹ“×═Ļ│╔║¾Ż¼āA│÷Ę┤æ¬ę║Ż¼į┘╝ė╚ļÅU╦«║═H2O2ĪŻĮø5┤╬īŹ“ׯ¼┴_Ąż├„B╚ź│²┬╩ĮėĮ³100%Ż¼Ę┤æ¬Ų„Ąū▓┐╚įėąFeĘ█Üł┴¶ĪŻ
2.7 ╬ó▓©▌oų·Fe-H2O2¾wŽĄųą┴_Ąż├„BÅU╦«Ą─ūŽ═Ō╣ŌūV
┴_Ąż├„BŠ▀ėąę╗éĆč§ļs▌ņŁhĮYśŗŻ¼į┌ŁhĄ─ā╔▀ģ╩ŪN-ęę═ķ╗∙Ż¼▀@ĘN╠ž╩ŌĄ─ĮYśŗ╩╣╦³į┌╦«╚▄ę║ųąŽÓī”ĘĆČ©ĪŻ╬ó▓©▌oų·Fe-H2O2¾wŽĄ▓╗═¼Ę┤æ¬ĢrķgĢr┴_Ąż├„BÅU╦«Ą─ūŽ═Ō╣ŌūVūVłDęŖłD6ĪŻė╔łD6┐╔ęŖŻ║┴_Ąż├„Bį┌553 nm╠ÄŠ▀ėąūŅ┤¾╬³╩šĘÕŻ╗ļSų°Ę┤æ¬ĢrķgĄ─čėķLŻ¼ÅU╦«Ą─ūŅ┤¾╬³╩šĘÕųĄ├„’@£pąĪŻ¼ŪęūŅ┤¾╬³╩š▓©ķL░l╔·┴╦ę╗Č©Ą─╦{ęŲŻ¼ūŅ┤¾╬³╩šĘÕų▓ĮÅ─553 nmŲ½ęŲĄĮ520 nmū¾ėęŻ¼ÅU╦«Ą─Ņü╔½ę▓ė╔įŁüĒĄ─╝t╔½ųØuūā×ķ¤o╔½ĪŻHuĄ╚šJ×ķ▀@ĘN╦{ęŲ¼FŽ¾╩Ūė╔ė┌┴_Ąż├„BĮøę╗ŽĄ┴ą├ōęę╗∙Ę┤æ¬║¾«a╔·Ą─ųąķg«a╬’ą╬│╔Ą─ĪŻę“┤╦Ż¼į┌╬ó▓©▌oų·Fe-H2O2¾wŽĄųąŻ¼┴_Ąż├„BĮYśŗĄ─├ōęę╗∙▀^│╠╩Ūų„ꬥ─ĮĄĮŌ▀^│╠ĪŻ

3 ĮYšō
aŻ®╬ó▓©▌oų·Fe-H2O2¾wŽĄ┬ō║Ž╠Ä└Ē┴_Ąż├„BÅU╦«Ż¼┐╔╠ßĖ▀┴_Ąż├„B╚ź│²┬╩║═╚ź│²╦┘┬╩Ż¼═¼Ģrį┌įō¾wŽĄŽ┬Fentonįćä®č§╗»Ę┤æ¬Ą─pHĘČć·▌^é„ĮyĄ─Fentonįćä®č§╗»Ę┤æ¬ę¬īÆĪŻŠ▀¾wģóęŖhttp://www.dongaorq.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
bŻ®FeĘ█ĪóH2O2Ą─╝ė╚ļ┴┐┤µį┌ę╗éĆ┼RĮńųĄŻ¼«ö╝ė╚ļ┴┐Ė▀ė┌┼RĮńųĄĢrŻ¼┴_Ąż├„B╚ź│²┬╩▓╗į÷Ę┤ĮĄĪŻūŅ╝čīŹ“׌l╝■×ķÅU╦«pH×ķ4.0Ż¼FeĘ█╝ė╚ļ┴┐×ķ50 mg/LŻ¼H2O2╝ė╚ļ┴┐×ķ10.0 mL/LĪŻī”ė┌│§╩╝┴_Ąż├„B┘|┴┐ØŌČ╚×ķ100 mg/LĄ─ÅU╦«Ż¼į┌┤╦Śl╝■Ž┬Ę┤æ¬12 minŻ¼┴_Ąż├„BĄ─╚ź│²┬╩▀_ĄĮ98.7%ĪŻ
cŻ®FeĘ█┐╔ČÓ┤╬╩╣ė├ĪŻĮø5┤╬╩╣ė├ĢrŻ¼Ę┤æ¬12min║¾┴_Ąż├„B╚ź│²┬╩ĮėĮ³100%ĪŻ


