╦«¾wĄū─Óųą╝t├╣╦žŠ·ųĻ╚ź│²ĘĮĘ©
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2016-1-23 9:00:31
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį
ĪĪĪĪĮ³─ĻüĒŻ¼ļSų°┐╣╔·╦žĄ─┤¾┴┐╩╣ė├Ż¼Ųõį┌ŁhŠ│Įķ┘|ųąĄ─Üł┴¶ęčę²Ų╚╦éāÅVĘ║ĻPūó.ļm╚╗╦∙Öz│÷Ą─┐╣╔·╦žÜł┴¶ØŌČ╚╦«ŲĮ╬┤▀_ĄĮų┬╦└ØŌČ╚Ż¼▓╗ūŃęįęųųŲ╗“š▀Üó╦└╬ó╔·╬’Ż¼Ą½ė╔ė┌▀@ą®╬’┘|┤¾ČÓöĄ╚įŠ▀ėą▌^ÅŖĄ─╔·╬’Ę┤æ¬╗Ņąį║═Ė╗╝»Ę┼┤¾ą¦æ¬Ż¼«ö▀_ĄĮūŅĄ═ęųŠ·ØŌČ╚╦«ŲĮĢrŻ¼┐╔─▄Ģ■┤┘▀M─═╦ÄŠ·Ą─░lš╣║═é„▓źŻ¼ęčėąčąŠ┐▒Ē├„Ż¼ķLŲ┌╩®ė├║¼ėą╦─Łh╦žĄ─ži╝S╩ŪŁhŠ│ųąŠ▀ėą┐╣╦Äąįų┬▓ĪŠ·Ą─ųžę¬üĒį┤Ż¼═¼ĢrŻ¼ę▓╩Ū┤┘▀MŲõ╔·│╔Ą─ų„ę¬═Ų┴”.Ė³×ķųžę¬Ą─╩ŪŻ¼─═╦ÄŠ·╦∙öyĦĄ──═╦Ä╗∙ę“┐╔ęįķLŲ┌┤µį┌ė┌═┴╚└║═╦«╔·╝ÜŠ·Ż¼╔§ų┴┐╔─▄Ģ■é„▀fų┴ų┬▓ĪąįĖ³ÅŖĄ─╝ÜŠ·Ż¼ī”╚╦ŅÉĮĪ┐Ąįņ│╔śO┤¾═■├{Ż¼ę“┤╦Ż¼ŁhŠ│ųą┐╣╔·╦žĄ─ŁhŠ│║¾ą¦æ¬ęį╝░╔·æBą¦æ¬│╔×ķĮ³─ĻŁhŠ│ŅIė“Ą─蹊┐¤ß³cų«ę╗.╝t├╣╦ž(ErythromycinŻ¼ERY)╩Ūę╗ŅÉ┤¾Łhā╚§źŅÉÅVūV┐╣╔·╦žŻ¼Š▀ėąÅŖ┤¾Ą─╬ó╔·╬’ęųųŲū„ė├.╚╦éāęčį┌╬█╦«Īó╦«į┤╦«║═’ŗė├╦«ųąÖz£yĄĮng Īż L-1~”╠g Īż L-1ØŌČ╚Ą─╝t├╣╦ž╬█╚Š.═¼ĢrŻ¼Üł┴¶į┌ūį╚╗╦«¾wųąĄ─┐╣╔·╦žėą75%│┴Ęeį┌╦«Ąū│┴Ęe╬’ųąŻ¼┐╔ą╬│╔╦«¾wĄū─ÓĄ─┐╣╔·╦žąŅĘeąį╬█╚ŠŻ¼▀MČ°ī”Ąū─Ó╬ó╔·æBįņ│╔ė░ĒæŻ¼╔§ų┴šTī¦╔·╬’╚║¾wī”╝t├╣╦ž«a╔·─═╦Äąį.─═╦ÄŠ·Ą─┤µį┌▓╗āH┐╔╝ėäĪÜł┴¶┐╣╔·╦žĄ─ŁhŠ│ė░ĒæŻ¼Ė³×ķųžę¬Ą─╩Ū─▄┤¾┤¾ĮĄĄ═┐╣╔·╦ž╦Ä╬’╔·╬’ęųųŲĄ─ėąą¦ąį.─┐Ū░Ż¼ßśī”╝t├╣╦ž─═╦ÄąįĘĮ├µĄ─蹊┐┤¾ČÓé╚ųžė┌蹊┐─│å╬ę╗Š·ĘNĄ──═╦Äąą×ķęį╝░╝t├╣╦žī”═┴ų°╬ó╔·╬’╚║┬õĮYśŗĄ─ė░ĒæŻ¼§rėąĻPė┌─═╝t├╣╦žŠ·╚║ČÓśėąįĄ─蹊┐Ż¼Č°ĻPė┌─═╦ÄŠ·╚║Ą─蹊┐ę▓┤¾ČÓ╝»ųąį┌╗Ū░ĘŅÉ║═╦─Łh╦žŅÉ.Ą╚┐╣╔·╦ž.ū„×ķę╗ĘNŁhŠ│Üł┴¶┬╩▌^Ė▀ŪęÅVĘ║╩╣ė├Ą─┐╣╔·╦žŻ¼čąŠ┐ŁhŠ│ųą╝t├╣╦ž─═╩▄Š·╚║Ą─ĮYśŗ╠ž³cŻ¼▓╗āHėąų·ė┌╚╦éāš²┤_įuār╝t├╣╦žĄ─╔·æB’LļUŻ¼Č°Ūę┐╔×ķ╝t├╣╦ž╦Ä╬’╬█╚ŠĄ─Ę└ų╬╠ß╣®└Ēšōę└ō■.
ĪĪĪĪ2 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ2.1 ų„ę¬įćä®╝░āxŲ„
ĪĪĪĪ╝t├╣╦ž┘ÅūįÅVų▌╚AŲµ╩ó╔·╬’┐Ų╝╝╣½╦Š.┼õų├100 ”╠g Īż mL-1├ō╦«╝t├╣╦ž─Ėę║(ė├3 mol Īż L-1 H2SO4š{╣Ø╝t├╣╦ž╚▄ę║Ą─pHųĄĄĮ3.0Ż¼į┌╩ę£žŽ┬öć░Ķ4 h)Ż¼4 Īµ▒▄╣Ō▒Ż┤µ.
ĪĪĪĪĀIB╚Ō£½┼ÓB╗∙Ż║10 gĄ░░ūļ╦Ż¼5 g┼Ż╚ŌĖÓŻ¼5 g NaClŻ¼1 Lš¶s╦«Ż¼š{pH×ķ7.0Ż¼╣╠¾w┼ÓB╗∙╝ė20%Ą─Łéų¼Ę█.
ĪĪĪĪŲõ╦¹╔·╗»įćä®░³└©Ż║╝ÜŠ·╗∙ę“ĮMDNA╠ß╚Īįćä®║ą(TIANamp Bacteria DNA Kit)Ż¼┘Åūį╠ņĖ∙╔·╗»┐Ų╝╝(▒▒Š®)ėąŽ▐╣½╦Š;Taq DNAŠ█║Ž├Ė▀BĮė├Ė(BioReadyTaq Mix)Ż¼┘Åūį║╝ų▌▓®╚š┐Ų╝╝ėąŽ▐╣½╦Š;UNIQ-10ų∙╩Į─z╗ž╩šįćä®║ąŻ¼T-▌d¾wPCR«a╬’┐╦┬Īįćä®║ąŻ¼Š∙┘Åūį╔·╣ż╔·╬’╣ż│╠(╔Ž║Ż)╣╔Ę▌ėąŽ▐╣½╦Š.ŽÓĻPę²╬’║Ž│╔Ż¼ė╔╔·╣ż╔·╬’╣ż│╠(╔Ž║Ż)╣╔Ę▌ėąŽ▐╣½╦Š═Ļ│╔.
ĪĪĪĪų„ę¬āxŲ„Ż║ūŽ═ŌĘų╣Ō╣ŌČ╚ėŗ(ŹuĮ“UV-2550)Ż¼PCRāx(Bio-Rad S 1000TM Thermal Cycler);ļŖėŠāx(Bio-Rad PowerPac Basic);ąĪą═┼_╩Įļxą─ÖC(LabogeneScanSpeed mini).
ĪĪĪĪ2.2 śėŲĘ▓╔╝»
ĪĪĪĪĄū─ÓśėŲĘ▓╔ūįķLŲ┌╩▄Ą═ØŌČ╚╝t├╣╦ž╬█╚ŠĄ──ŻöM╦«╔·╔·æBŽĄĮyŻ¼įōŽĄĮyĄ─śŗĮ©ģó┐╝├└ć°Łh▒Ż╩Ą─ś╦£╩ĘĮĘ©.Ž“╩ęā╚ņo╦«Bų│Žõ(80 cmĪ┴60 cmĪ┴40 cm)ā╚╝ė╚ļ╝s20 kgĄ─│┴Ęe╬’║═60 L╦«Ż¼ų▓╚ļ╦«╠N▓▌║═░▀±R¶~.īŹ“×Ų┌ķg╩ęā╚£žČ╚┐žųŲį┌(30Ī└2)ĪµŻ¼pHųĄ┐žųŲį┌7.0Ī└0.2Īó╚▄č§> 4 mg Īż L-1.ŽĄĮyĘĆČ©║¾Ż¼├┐╠ņŽ“ŽĄĮyā╚╝ė╚ļ2.5 ”╠g Īż L-1├ō╦«╝t├╣╦ž╚▄ę║Ż¼│ų└m▀\ąą1─ĻĢrķgŻ¼▓╔╝»Ąū─ÓśėŲĘ▀MąąĘų╬÷.
ĪĪĪĪ2.3 īŹ“×ĘĮĘ©
ĪĪĪĪ2.3.1 ┐╔┼ÓB─═╝t├╣╦ž╝ÜŠ·Ą─┼ÓB║═ėŗöĄ
ĪĪĪĪĘųäe╚Ī3Ę▌1.5 gą┬§rĄū─ÓĘųäe╝ė╚ļ║¼ėą150 mL¤oŠ·╦«Ą─╚²ĮŪŲ┐ųąŻ¼ōu┤▓š±╩Ä3 hŻ¼ųŲéõ│╔Š·æęę║Ż¼╚╗║¾Ęųäe╬³╚Ī▀m┴┐Ż¼▀Mąą╗ņ║Ž.▓╔ė├ŲĮ░ÕŠ·┬õėŗöĄĘ©Ż¼╚Ī▀m┴┐╗ņ║ŽŠ∙ä“Ą─Š·æęę║▀Mąą╠▌Č╚ŽĪßī║¾Ż¼Ęųäe═┐▓╝į┌ųŲéõ║├Ą─╝t├╣╦žĮKØŌČ╚×ķ16 ”╠g Īż mL-1Ą─ĀIB╚Ō£½╣╠¾w┼ÓB╗∙╔ŽŻ¼├┐ę╗ØŌČ╚Š∙įOų├3éĆųžÅ═Ż¼30 Īµ┼ÓB48 hŻ¼▀Mąą┐╣ąį╝ÜŠ·ėŗöĄ.
ĪĪĪĪ2.3.2 ┐╔┼ÓB─═╝t├╣╦žŠ·Ą─Ęųļx┼cĶbČ©
ĪĪĪĪ▀x╚Ī2.3.1╣ØųąŽĪßīČ╚▀m«öĄ─ŲĮ░Õ╠¶╚Īå╬Š·┬õŻ¼Ęųäeį┌30 ĪµŻ¼150 r Īż min-1▀Mąąę║¾w┼ÓB24 hŻ¼į┘ŽĪßīų┴▀m«öØŌČ╚▀Mąą═┐▓╝Ż¼ųžÅ═3~4┤╬Ż¼ų▒ų┴ŲĮ░Õ╔Žų╗╔·ķLå╬ę╗Š·┬õ.
ĪĪĪĪ╠ß╚Ī╝āŠ·Ą─╝ÜŠ·╗∙ę“ĮMDNAŻ¼└¹ė├╝ÜŠ·═©ė├ę²╬’27F║═1492R▀MąąPCRöUį÷Ż¼PCR«a╬’Ą─╝ā╗»╝░£yą“Š∙ė╔╔·╣ż╔·╬’╣ż│╠(╔Ž║Ż)╣╔Ę▌ėąŽ▐╣½╦Š═Ļ│╔.
ĪĪĪĪ2.3.3 śėŲĘ┐éDNAĄ─╠ß╚Ī
ĪĪĪĪīó2.3.1╣ØųąĄ─Š·æęę║╚Ī▀m┴┐╝ė╚ļĄĮęč£ńŠ·Ą─║¼ėą16 ”╠g Īż mL-1╝t├╣╦žĄ─ĀIB╚Ō£½┼ÓB╗∙ųąŻ¼150 r Īż min-1Ż¼30 Īµ▀^ę╣┼ÓB║¾╠ß╚Ī╗∙ę“ĮMDNAŻ¼Ą├ĄĮĄ─DNAśėŲĘ×ķĄū─Óųą─═╝t├╣╦ž╬ó╔·╬’Ą─┐éDNA.
ĪĪĪĪ2.3.4 PCRöUį÷
ĪĪĪĪPCRöUį÷ę²╬’Ż║27F(5Īõ-AGAGTTTGATCCTGGCTCAG-3Īõ)╝░1492R(5Īõ-GGTTACCTTGTTACGACTT-3Īõ).
ĪĪĪĪPCRĘ┤款wŽĄ(25 ”╠L)Ż║DNA─Ż░Õ1 ”╠LŻ¼ddH2O 10.5 ”╠LŻ¼ę²╬’27F║═1492RĖ„0.5 ”╠LŻ¼Taq├Ė12.5 ”╠L.
ĪĪĪĪPCR│╠ą“Ż║95 ĪµŅAūāąį3 minŻ¼95 Īµūāąį30 sŻ¼50 Īµ═╦╗1 minŻ¼72 Īµčė╔ņ1 minŻ¼30éĆ裣hŻ¼ūŅ║¾72 Īµčė╔ņ10 minŻ¼4 Īµ▒Ż┤µ.
ĪĪĪĪīóPCR«a╬’ė├Łéų¼╠Ū─²─zļŖėŠÖz“×║¾▀MąąŪą─z╗ž╩šŻ¼ė├UNIQ-10ų∙╩ĮDNA─z╗ž╩šįćä®║ą╝ā╗»▀Mąą╝ā╗».
ĪĪĪĪ2.3.5 ┐╦┬Ī╬─ÄņĄ─śŗĮ©
ĪĪĪĪ└¹ė├╝ÜŠ·═©ė├ę²╬’27F╝░1492Rī”śėŲĘDNA▀MąąPCRöUį÷.īó╝ā╗»║¾Ą─PCR«a╬’ė├pUCm-T▌d¾w▀Mąą─┐Ą─╗∙ę“▀BĮėŻ¼╚╗║¾īóŲõ▐D╚ļ┤¾─cŚUŠ·DH5”┴Ėą╩▄æBųąŻ¼37 Īµš±╩Ä┼ÓB1 h;═Ļ║¾īóŲõ═┐į┌║¼ėąIPTG║═X-galĄ─░▒ŲSŪÓ├╣╦ž┼ÓB╗∙ŲĮ░Õ╔ŽŻ¼37 Īµ║Ń£ž┼ÓB▀^ę╣║¾╠¶╚Ī░ū╔½Ą─Ļ¢ąį┐╦┬ĪūėŻ¼į┘ė├ŽÓ═¼Ą─ĘĮĘ©▀Mąą┼ÓB;└¹ė├PstI å╬├ĖŪą▀MąąĻ¢ąį┐╦┬Ī“×ūC.“×ūC║¾Ą─Ļ¢ąį┐╦┬Īūė£yą“ė╔╔Ž║Ż╔·╣ż╔·╬’╣ż│╠╝╝ągĘ■äšėąŽ▐╣½╦Š═Ļ│╔.£yą“ĮY╣¹═©▀^CD-hit▄ø╝■╗∙ė┌ą“┴ąŽÓ╦ŲČ╚▀MąąŠ█ŅÉĘų╬÷Ż¼äØĘų▓┘ū„ĘųŅÉå╬į¬(Operational Taxonomic UnitŻ¼OTU);╩╣ė├Estimate▄ø╝■└LųŲ╬ó╔·╬’ŽĪėąąįŪ·ŠĆ.└¹ė├ŽĪėąąįŪ·ŠĆ║═╬─ÄņĖ▓╔w┬╩Cįuār╬─ÄņŻ¼╬─ÄņĖ▓╔w┬╩Cėŗ╦Ń╣½╩Į×ķ
ĪĪĪĪ
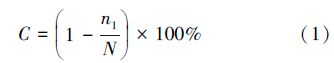
ĪĪĪĪ╩ĮųąŻ¼N┤·▒ĒĻ¢ąį┐╦┬Īūė┐éöĄŻ¼n1┤·▒ĒāH║¼å╬éĆ┐╦┬ĪūėĄ─öĄ┴┐.
ĪĪĪĪ╦∙ėą£yą“ĮY╣¹į┌GenBanköĄō■Äņ▀MąąBlast▒╚ī”║¾Ž┬▌d═¼į┤ąįą“┴ąŻ¼ŽĄĮy░lė²śõĄ─└LųŲĮĶų·MEGA5.0▄ø╝■═Ļ│╔.
ĪĪĪĪ3 ĮY╣¹┼cėæšō
ĪĪĪĪ3.1 ┐╔┼ÓB─═╝t├╣╦ž╝ÜŠ·Ą─ėŗöĄ┼cĘųļxĶbČ©
ĪĪĪĪĖ∙ō■┐╣Š·╦Ä╬’├¶ĖąąįīŹ“׳╠ąąś╦£╩Ż¼╝t├╣╦žĄ─ūŅĄ═ęųŠ·ØŌČ╚(MIC)×ķ8 ”╠g Īż mL-1Ż¼▒ŠčąŠ┐▀xō±┬įĖ▀ė┌ŲõMICųĄĄ─┐╣╔·╦žØŌČ╚Ż¼╝┤╝t├╣╦žĄ─ĮKØŌČ╚×ķ16 ”╠g Īż mL-1.└¹ė├ŲĮ░ÕŠ·┬õėŗöĄĘ©ī”┐╣ąį╝ÜŠ·Ą─ėŗöĄĮY╣¹×ķ9.86Ī┴108 CFU Īż g-1.īóŲĮ░Õ╔Žą╬æBĖ„«ÉĄ──═╦ÄŠ·ųĻ▀MąąĘ┤Å═╝ā╗»Ęųļx║¾Ż¼Ą├ĄĮ┴╦3ųĻ¬Ü┴óĄ─Š·ųĻŻ¼ŲõĖ„ūįĄ─ą╬æB╚ń▒Ē 1ųą╦∙╩Š.

▒Ē1 ┐╔┼ÓB─═╝t├╣╦žŠ·Š·┬õą╬æB
ĪĪĪĪĘųäeīó3ųĻŠ·ųĻĄ─16S rDNAą“┴ąį┌NCBI║╦╦ßöĄō■Äņųą▀MąąBLAST═¼į┤ąį▒╚ī”Ż¼┤_Č©┼cŲõūŅĮėĮ³Ą─ĘNŽĄ╚║¾w.ĮY║ŽĖ„Š·ųĻą╬æBīW╠žš„╝░16S rDNA ą“┴ąĘų╬÷Ż¼│§▓ĮĶbČ©×ķ┘ć░▒╦ßč┐µ▀ŚUŠ·(Lysinibacillus sp.)Īó═┴╚└č┐µ▀ŚUŠ·(Solibacillus silvestris)ęį╝░Ž×śėč┐µ▀ŚUŠ·(Bacillus cereus)Ż¼Ė„ūįį┌GenBankųąĄ─ĄŪõø╠¢Ęų×ķKP694229ĪóKP694230ĪóKP694231Ż¼Ūę╔Ž╩÷3ĘN┐╔┼ÓBŠ·Š∙ī┘ė┌č┐µ▀ŚUŠ·ŠV.ąĶę¬ūóęŌĄ─╩ŪŻ¼Ž×śėč┐µ▀ŚUŠ·į┌ūį╚╗ĮńĘų▓╝ÅVĘ║Ż¼╩Ūę╗ĘN╩│į┤ąįų┬▓ĪŠ·Ż¼╚▌ęūę²Ų╩│╬’ųąČŠŻ¼ī”╝t├╣╦žśOČ╚├¶ĖąŻ¼ī”ŪÓ├╣╦ž─═╦Ä.╚╗Č°Ż¼▒Š╬─Ą──═╦ÄīŹ“×░l¼FŻ¼Å─Ąū─ÓųąĘųļx│÷Ą─Ž×śėč┐µ▀ŚUŠ·GD2Cī”╝t├╣╦žęč▒Ē¼F│÷ę╗Č©Ą──═╦ÄąįŻ¼▀@┐╔─▄╩ŪŠ·ųĻĘųļxūįķLŲ┌╩▄Ą═ØŌČ╚╝t├╣╦ž╬█╚ŠĄ─ŁhŠ│Ż¼▀@ęŌ╬Čų°Ą═ØŌČ╚╝t├╣╦žĄ─šTī¦ū„ė├┐╔╩╣Ž×śėč┐µ▀ŚUŠ·Š▀éõę╗Č©Ą──═╦Äąį.
ĪĪĪĪ3.2 16S rDNA┐╦┬Ī╬─ÄņĄ─Ęų╬÷
ĪĪĪĪļSÖC╠¶╚Ī83éĆĻ¢ąį┐╦┬Īūė▀Mąą£yą“(ą“┴ąķLŠ∙×ķ1500 bpū¾ėę)Ż¼īó£yą“ĮY╣¹į┌NCBIĄ─║╦╦ßöĄō■Äņųą▀MąąBlast▒╚ī”Ż¼īóą“┴ą▒╚ī”ĮY╣¹ŽÓ╦ŲČ╚┤¾ė┌Ą╚ė┌97%Ą─Č©┴x×ķę╗éĆ▓┘ū„å╬į¬(Operational Taxonomic UnitŻ¼OTU)Ż¼╣▓Ą├ĄĮ6éĆOTUŻ¼Ųõųąėą2éĆOTUŅÉą═┤·▒Ēå╬┐╦┬ĪŻ¼ūŅČÓĄ─OTUŅÉą═░³└©36éĆ┐╦┬Īūė.ļS║¾ęį╬─ÄņĖ▓╔w┬╩C╝░ŽĪėąąįŪ·ŠĆüĒįuār╦∙śŗĮ©Ą─╬─ÄņŻ¼░l¼Fįō╬─ÄņĖ▓╔w┬╩×ķ97.6%Ż¼ŪęŽĪėąąįŪ·ŠĆ┌ģė┌ŲĮŠÅŻ¼▀@ęŌ╬Čų°╦∙śŗĮ©Ą─┐╦┬Ī╬─ÄņÄņ╚▌▌^┤¾Ż¼╦∙╠¶╚ĪĄ─┐╦┬ĪūėöĄ┴┐─▄ē“▌^×ķ═Ļš¹Ą─Ę┤ė│śėŲĘųą╬ó╔·╬’Ą─ČÓśėąį.╔Ž╩÷ā╔ĒŚĘų╬÷▒Ē├„įō┐╦┬Ī╬─Äņ╦∙║¼83éĆ┐╦┬Īūė─▄ē“▌^╚½├µĄžĘ┤ė│Ąū─Óųą─═╝t├╣╦ž╝ÜŠ·ĘN╚║ĮYśŗĄ─ČÓśėąį.
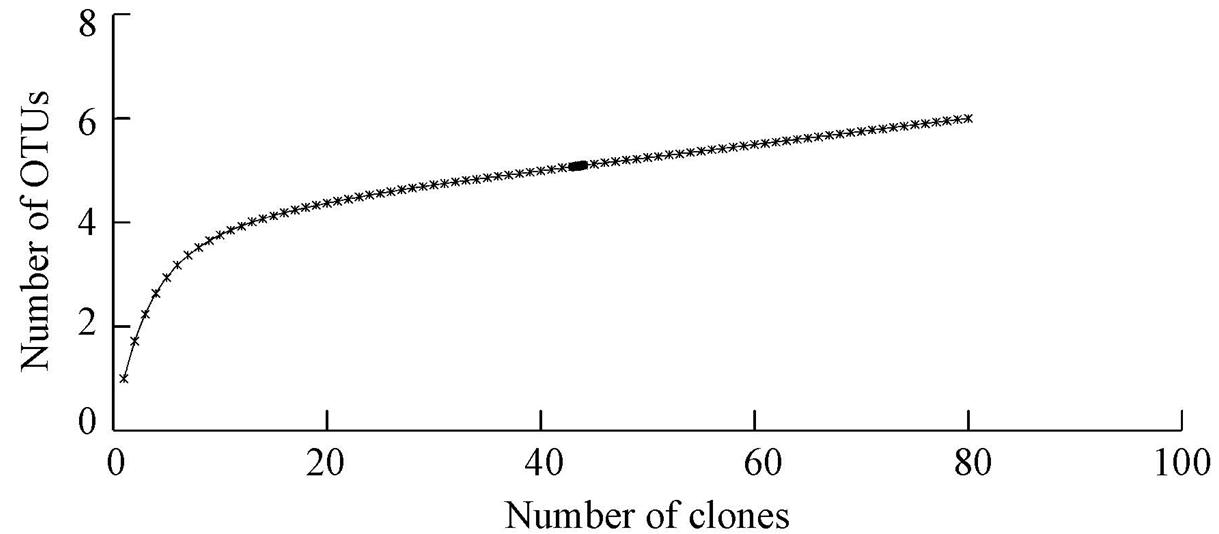
łD1 Ąū─Óųą─═╝t├╣╦ž╝ÜŠ·16S rDNA┐╦┬Ī╬─ÄņĄ─ŽĪ╚▒ąįŪ·ŠĆ
ĪĪĪĪśėŲĘųą16S rDNA┐╦┬Ī╬─ÄņĮY╣¹╚ń▒Ē 2╦∙╩ŠŻ¼Ųõųą4éĆOTUĄ─┐╦┬Īūėą“┴ą┼cNCBI║╦╦ßöĄō■Äņųąęčų¬╝ÜŠ·Ą─16S rDNAą“┴ąŽÓ╦ŲČ╚į┌97%ęį╔ŽŻ¼2éĆOTUĄ─ŽÓ╦ŲČ╚Ą═ė┌97%.ė╔▒╚ī”ĮY╣¹┐╔ų¬Ż¼ķLŲ┌╩▄Ą═ØŌČ╚╝t├╣╦ž╬█╚ŠĄ─Ąū─ÓųąŻ¼─═╝t├╣╦žĄ─╝ÜŠ·ŅÉ╚║┐╔Ęų×ķ╚²┤¾ŅÉ╚║Ż¼╝┤Ż║╬┤½@┼ÓB╝ÜŠ·(Uncultured bacterium)Īóč┐µ▀ŚUŠ·ŠV╝ÜŠ·(Bacilli)║═╦¾Š·ŠV╝ÜŠ·(Clostridia)Ż¼Ė„╔µ╝░ĄĮ2éĆOTU(54éĆ┐╦┬Īūė)Īó3éĆOTU(28éĆ┐╦┬Īūė)║═1éĆOTU(1éĆ┐╦┬Īūė).Ąū─ÓśėŲĘųą─═╝t├╣╦ž╬ó╔·╬’ųąĄ─ā×ä▌Š·╚║×ķ─│ĘN╬┤½@┼ÓBĄ─╝ÜŠ·Ż¼į┌╬─Äņųąš╝43.37%Ż¼Ųõ┤╬╩Ū╠KįŲĮč┐µ▀ŚUŠ·Ż¼š╝╬─ÄņĄ─24.10%.
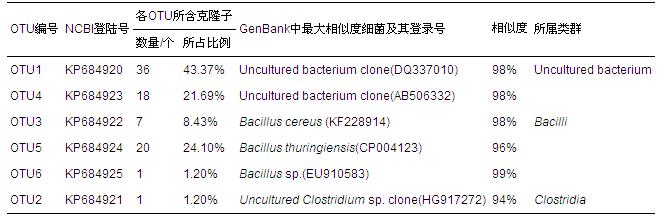
▒Ē2 Ąū─Óųą─═╝t├╣╦ž╝ÜŠ·16S rDNA┐╦┬Ī╬─ÄņĮY╣¹
ĪĪĪĪ╠KįŲĮč┐µ▀ŚUŠ·╩Ūę╗ĘNėąęµŚUŠ·Ż¼ČÓė├ū÷ÜóŽx䮯¼─┐Ū░ī”ė┌Ųõ─═╦ÄąįĄ─ł¾Ą└▌^╔┘Ż¼Ą½Å─╬─ÄņĮY╣¹üĒ┐┤Ż¼╠KįŲĮč┐µ▀ŚUŠ·ęčī”╝t├╣╦ž«a╔·┴╦ę╗Č©Ą──═╦Äąį;┴Ē═ŌŻ¼╝t├╣╦žįŁ▒Šī”╦¾ĀŅč┐µ▀ŚUŠ·ėą▌^ÅŖĄ─ęųųŲū„ė├Ż¼į┌▒ŠčąŠ┐ųąę▓▒Ē¼F│÷┴╦ę╗Č©Ą──═╦ÄąįŻ¼▀@┐╔─▄ę▓╩Ūę“×ķŁhŠ│ųąÜł┴¶Ą─Ą═ØŌČ╚╝t├╣╦žī”ŲõšTī¦Ż¼╩╣Ųõī”╝t├╣╦ž«a╔·┴╦ę╗Č©Ą─┐╣ąįŻ¼▀@ę▓▀Mę╗▓Įšf├„┴╦ŁhŠ│ųąÜł┴¶┐╣╔·╦ž┤µį┌Øōį┌ė░Ēæ.ė╔┐╦┬Ī╬─ÄņĮY╣¹┐╔ęį┐┤│÷Ż¼į┌ęčų¬Š·ī┘ųąŻ¼č┐µ▀ŚUŠ·ī┘╦∙š╝▒╚└²ūŅ┤¾Ż¼▀@┼c╔Ž╩÷╦∙║Y▀xĘųļx│÷Ą─┐╔┼ÓBĄ──═╦ÄŠ·Š∙×ķč┐µ▀ŚUŠ·ī┘╝ÜŠ·Ą─ĮY╣¹╩Ū╗źŽÓ╬Ū║ŽĄ─.
ĪĪĪĪ┴Ē═ŌŻ¼śŗĮ©Ą─16S rDNA╬─Äņųąėą25.3%(21éĆ┐╦┬Īūė)Ą─╝ÜŠ·┼cGenBankųąęčų¬╝ÜŠ·Ą─16S rDNAą“┴ą═¼į┤ąįĄ═ė┌97%Ż¼Č°į┌ą“┴ą═¼į┤ąį蹊┐ųąŻ¼ę╗░ŃšJ×ķ╝ÜŠ·16S rDNAą“┴ą═¼į┤ąįĄ═ė┌97%╝┤ī┘ė┌▓╗═¼Ą─ĘNŻ¼▀@šf├„Ąū─Óųą╠N▓žų°įSČÓ╬┤ų¬Ą──═╦Ä╝ÜŠ·Ż¼ėą┤²ė┌▀Mę╗▓Į╔Ņ╚ļ蹊┐.
ĪĪĪĪ3.3 Ąū─ÓśėŲĘ16S rDNAŽĄĮy░lė²Ęų╬÷
ĪĪĪĪĘųūėŽĄĮy░lė²Ęų╬÷Ż¼╠žäe╩Ūī”╝ÜŠ·16S rDNA╗∙ę“Ą─═¼į┤ąį▀MąąĘų╬÷ėąų·ė┌┴╦ĮŌ╬ó╔·╬’╚║┬õĮYśŗĄ─ČÓśėąį.īó▒Ē 1║═▒Ē 2ųąĄ─3ųĻå╬Š·║═6éĆOTUĄ─ēA╗∙ą“┴ą╝░ŲõŽÓæ¬Ą─═¼į┤ąįą“┴ą▀MąąŠ█ŅÉĘų╬÷║¾Ż¼ęį╩╚¤ßµ£Ū“Š·Streptococcus thermophilus(NR042778)×ķ═ŌŅÉ╚║Ż¼└LųŲ│÷Ąū─Óųą─═╝t├╣╦ž╝ÜŠ·ŽĄĮy░lė²śõŻ¼ęŖłD 2.
ĪĪĪĪė╔łD 2┐╔ęŖŻ¼═┴╚└č┐µ▀ŚUŠ·GD2BĄ─ēA╗∙ą“┴ą┼cOTU4Ą─ēA╗∙ą“┴ąų«ķgŽÓ╦ŲČ╚▌^Ė▀Ż¼Ūę┼cOTU1┤µį┌▌^║├Ą─ėHŠēĻPŽĄ.ę“Č°īóOTU1║═OTU4Ą─ą“┴ą▀Mę╗▓Įį┌RDPöĄō■Äņųą▀Mąą▒╚ī”Ż¼░l¼FŲõūŅ┤¾ŽÓ╦ŲŠ·ųĻUncultured bacterium clone(DQ337010)║═Uncultured bacterium clone(AB506332)┐╔ęį▀Mę╗▓ĮäØĘųĄĮ─│╬┤ĘųŅÉĄ─äėąįŪ“Š·ī┘(Unclassified Planococcaceae)Ż¼Č°═┴╚└č┐µ▀ŚUŠ·║═äėąįŪ“Š·ī┘Š∙ī┘ė┌äėŪ“Š·┐Ų(Planococcaceae)Ż¼╦∙ęįOTU1ĪóGD2Bęį╝░OTU4į┌ŽĄĮy░lė²śõųąŠ█╝»ĄĮę╗Ų.Ž×śėč┐µ▀ŚUŠ·GD2C┼cOTU5Ą─ūŅ┤¾ŽÓ╦ŲŠ·ųĻ╠KįŲĮč┐µ▀ŚUŠ·┤µį┌▌^║├Ą─ėHŠēĻPŽĄŻ¼▀@╩Ūė╔ė┌╠KįŲĮč┐µ▀ŚUŠ·║═Ž×śėč┐µ▀ŚUŠ·Š∙ī┘ė┌Ž×śėŚUŠ·ī┘Ż¼ā╔š▀ų«ķgŠ▀ėąĖ▀Č╚Ą─═¼į┤ąį.
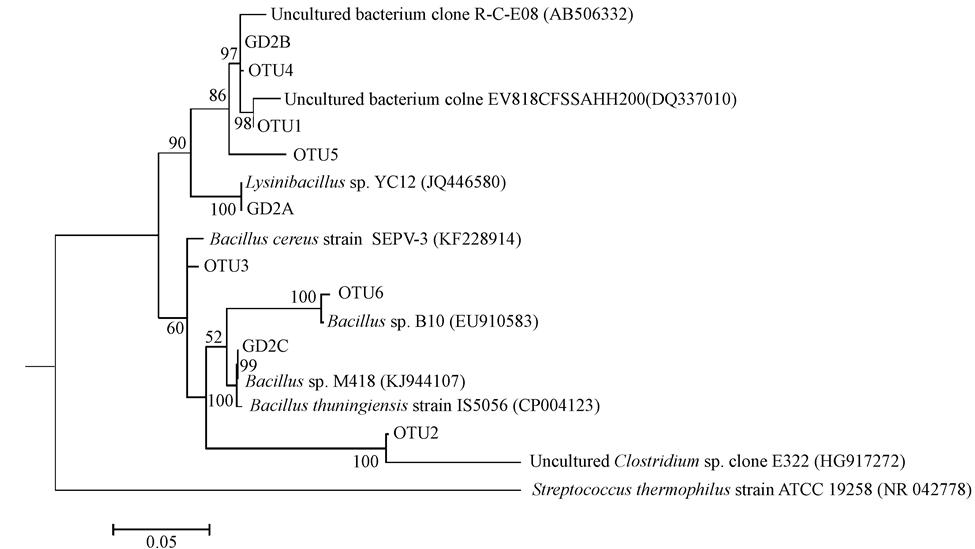
łD2 Ąū─Óųą─═╝t├╣╦ž╝ÜŠ·ŽĄĮy░lė²śõ
ĪĪĪĪ╝t├╣╦žū„×ķĄ┌ę╗┤·┤¾Łhā╚§źŅÉ┐╣╔·╦žŻ¼ūį1952─Ļæ¬ė├ė┌┼R┤▓ęįüĒŻ¼ę╗ų▒▒╗╚╦éāķLĢrķg┤¾ä®┴┐╩╣ė├Ż¼╩╣Ą├ČÓĘNįŁ▒Š├¶ĖąĄ─╬ó╔·╬’ī”Ųõ«a╔·┴╦┐╣ąį(└Ņå┤ėŅĄ╚Ż¼2013)Ż¼▒╚╚ńĘ╬čūµ£Ū“Š·ĪóĮ³S╔½ŲŽ╠čŪ“Š·Īó╝S─cŪ“Š·Ą╚.Č°▒ŠčąŠ┐░l¼FĄ─č┐µ▀ŚUŠ·Ż¼ŽÓĻPł¾Ą└╔ą▓╗ČÓęŖ.ė┌č┼ŁéĄ╚(2007)░l¼FŻ¼Ęųļxūį═┴╚└Īó’Ģ┴Ž║═Ę╩┴ŽĄ─č┐µ▀ŚUŠ·ī”┤¾Łhā╚§źŅÉ┐╣╔·╦ž▒Ē¼F│÷ę╗Č©Ą─├¶Ėąąį.▒ŠčąŠ┐’@╩ŠŻ¼Įø▀^×ķŲ┌1─ĻĄ─Ą═ØŌČ╚╝t├╣╦ž├{Ų╚Ż¼č┐µ▀ŚUŠ·ī”╝t├╣╦žęč▒Ē¼F│÷ę╗Č©Ą──═╦ÄąįŻ¼3ųĻ┐╔┼ÓBĄ─╝t├╣╦ž─═╦ÄŠ·╝░╝t├╣╦ž─═╦ÄŠ·┐╦┬Ī╬─Äņųąėą33.73%Š∙ī┘ė┌č┐µ▀ŚUŠ·.▀@┐╔─▄╩Ūė╔ė┌Ż║ó┘▓╗═¼ä®┴┐╩╣ė├┤¾Łhā╚§źŅÉ╦Ä╬’Ż¼į┌ÖC¾wā╚┤µį┌šTī¦│÷─═╦ÄųĻĄ─┐╔─▄ąį(äóņ¹Į▄Ż¼2008);ó┌╬ó╔·╬’╝Ü░¹┐╔ęį═©▀^╗∙ę“Ą─╦«ŲĮ▐DęŲ╗“š▀┐╔ęŲäė▀zé„ę“ūė½@Ą├Ąų┐╣┴”(└ŅŠ¦Ż¼2013)Ż¼═©▀^┐╣ąį╗∙ę“Ą─╦«ŲĮ▐DęŲ½@Ą├─═╩▄╝t├╣╦ž╗∙ę“Ż¼Å─Č°½@Ą├ī”╝t├╣╦žĄ─Ąų┐╣┴”.«ö╝ÜŠ·Š▀ėą┐╣╔·╦ž┐╣ąį║¾Ż¼┐╔─▄Ģ■ī”╝ÜŠ·┤·ųx«a╔·╠žČ©Ą─Ė─ūā(╚ń┐╣ųžĮī┘╬█╚ŠĄ╚╠žąį)Ż¼╔§ų┴┐╔╩╣╝ÜŠ·į┌─│ą®ŁhŠ│ųąĖ³Š▀ėą╔·┤µā×ä▌;Č°┤µį┌ė┌╗∙ę“▐DęŲå╬╬╗Ą─┐╣ąį╗∙ę“Ż¼ät┐╔ęįūį╬ęÅ═ųŲŻ¼Å─Č°ę╗ų▒┤µį┌ė┌╬ó╔·╬’╚║┬õ└’(ŚŅĘfŻ¼2010)Ż¼▀@▒žīóę²░lŠ▐┤¾Ą─Øōį┌╬Ż║”Ż¼▓ó═■├{ĄĮŁhŠ│╝░╚╦ŅÉĮĪ┐Ą.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.dongaorq.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
ĪĪĪĪ4 ĮYšō
ĪĪĪĪ1)ė├é„ĮyĘĮĘ©Å─Ąū─Óųą║Y▀x│÷Ą─3ųĻč┐µ▀ŚUŠ·ŠV─═╝t├╣╦žŠ·ųĻŻ¼ĮY║ŽĖ„Š·ųĻą╬æBīW╠žš„╝░16S rDNAą“┴ąĘų╬÷Ż¼│§▓ĮĶbČ©×ķ┘ć░▒╦ßč┐µ▀ŚUŠ·(Lysinibacillus sp.)Īó═┴╚└č┐µ▀ŚUŠ·(Solibacillus silvestris)ęį╝░Ž×śėč┐µ▀ŚUŠ·(Bacillus cereus).ŲõųąįŁ▒Šī”╝t├╣╦žśOČ╚├¶ĖąĄ─Ž×śėč┐µ▀ŚUŠ·Ż¼ė╔ė┌Ą═ØŌČ╚╝t├╣╦žĄ─±Z╗»Ż¼ī”╝t├╣╦ž«a╔·┴╦ę╗Č©Ą──═╦Äąį.
ĪĪĪĪ2)ķLŲ┌╩▄Ą═ØŌČ╚╝t├╣╦ž╬█╚ŠĄ─Ąū─ÓųąŻ¼─═╝t├╣╦žĄ─╝ÜŠ·ŅÉ╚║Ęų╚²┤¾ŅÉ╚║Ż¼╝┤Ż║╬┤½@┼ÓBĄ─╝ÜŠ·Īóč┐µ▀ŚUŠ·ŠV║═╦¾ĀŅč┐µ▀ŚUŠ·ŠV.Ųõųą╬┤½@┼ÓBĄ─╝ÜŠ·į┌š¹éĆ╬─Äņųą▒╚└²ūŅ┤¾Ż¼┐╔┼ÓBĄ──═╦ÄŠ·Ą─ā×ä▌ŅÉ╚║×ķč┐µ▀ŚUŠ·ŠV.ĮY║ŽŽĄĮy░lė²śõĄ─Ęų╬÷Ż¼░l¼F╦∙š╝▒╚└²ūŅ┤¾Ą──│╬┤½@┼ÓBĄ─╝ÜŠ·×ķ─│ĘN╬┤ĘųŅÉĄ─äėąįŪ“Š·(43.37%)Ż¼┐╔│§▓ĮäØĘųĄĮč┐µ▀ŚUŠ·ŠV(Bacilli)Ż¼╔ąąĶĖ³ČÓĄžĘųŅÉĶbČ©.į┌16S rDNA┐╦┬Ī╬─ÄņųąŻ¼ėą25.3%Ą─╝ÜŠ·┼cGenBankųąęčų¬╝ÜŠ·Ą─ą“┴ą═¼į┤ąįĄ═ė┌97%Ż¼▀@šf├„Ąū─Óųą╠N▓žų°įSČÓ╬┤ų¬Ą──═╦Ä╝ÜŠ·Ż¼ėą┤²ė┌▀Mę╗▓Į╔Ņ╚ļ蹊┐.
ĪĪĪĪ3)═©▀^ī”16S rDNA╬─Äņ蹊┐░l¼FŻ¼ī”╝t├╣╦žŠ▀ėąę╗Č©─═╦ÄąįĄ─╝ÜŠ·╝╚ėąų┬▓ĪŠ·(└²╚ńŽ×śėč┐µ▀ŚUŠ·)Ż¼ę▓ėąėąęµŠ·(└²╚ń╠KįŲĮŚUŠ·).ļSų°Ė„ĘN┐╣╔·╦ž╩╣ė├┴┐Ą─į÷╝ėŻ¼ę╗ĘĮ├µŻ¼╩╣Ą├įŁ▒Šī”┐╣╔·╦žėąę╗Č©├¶ĖąČ╚Ą─ų┬▓ĪŠ·▒Ē¼F│÷┴╦ę╗Č©Ą──═╦ÄąįŻ¼ī”╝▓▓ĪĄ─Ę└ų╬╝ė┤¾┴╦ļyČ╚;┴Ēę╗ĘĮ├µŻ¼ę▓╩╣Ą├ŁhŠ│ųą─│ą®ėąęµŠ·½@Ą├┴╦ę╗Č©Ą──═╦ÄąįŻ¼╩╣Ųõ┐╔ęįĖ³║├Ą─╔·┤µ.į┌┐╣╔·╦ž╬█╚Šå¢Ņ}įĮüĒįĮć└ųžĄ─Į±╠ņŻ¼ėąęµĄ─č┐µ▀ŚUŠ·Ą─æ¬ė├蹊┐Ż¼┐╔─▄╩ŪĮŌøQ┐╣╔·╦žå¢Ņ}Ą─ę╗éĆėąą¦ĘĮ░Ė.


