Š█┬╚ęꎮ(PVC)ļxą──Ėę║ÅU╦«
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2014-11-8 9:23:17
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ļxą──Ėę║ÅU╦«╩Ū▓╔ė├æęĖĪŠ█║Ž╣ż╦ć╔·«aŠ█┬╚ęꎮŻ©PVCŻ®▀^│╠ųą«a╔·Ą─ų„ę¬ÅU╦«ų«ę╗ĪŻįōŅÉÅU╦«Š▀ėą╦«┴┐┤¾ĪóØßČ╚▌^Ė▀ęį╝░┐╔╔·╗»ąįŻ©BOD/CODŻ®▓ŅĄ─╠ž³cŻ¼ī┘ė┌Ą═ØŌČ╚ļyĮĄĮŌėąÖCÅU╦«ĪŻÅU╦«Ą─ų„ę¬╬█╚Š│╔Ęų×ķė├ū„Ęų╔ó䮥─Š█ęꎮ┤╝Ż©PVAŻ®ĪŻPVA ī┘ė┌ėąÖCĖ▀ĘųūėŅÉ╗»║Ž╬’Ż¼ļyęį▒╗╔·╬’ĮĄĮŌĪŻį┌╦«¾wųąŻ¼PVA ═©│Żęį─z¾wĀŅæB┤µį┌Ż¼┐╔ą╬│╔┤¾┴┐┼▌─Ł▓ó┤┘▀M│┴ĘeĄ─ųžĮī┘▀węŲĪŻę“┤╦Ż¼╚¶ų▒Įė┤¾┴┐┼┼Ę┼║¼ėąPVA Ą──Ėę║ÅU╦«īóĦüĒć└ųžĄ─╦«¾w╬█╚Šå¢Ņ}ĪŻūį2006 ─Ļķ_╩╝Ż¼╬ęć°PVC «a┴┐▄SŠė╩└ĮńĄ┌ę╗Ż¼āH2011 ─Ļ╬ęć°ę“╔·«aPVCČ°«a╔·Ą──Ėę║ÅU╦«┐é«a┴┐Š═╝s×ķ5 200 ╚ftŻ¼ę“┤╦žĮąĶę╗ĘNĖ▀ą¦Īó║å▒ŃĄ──Ėę║ÅU╦«╠Ä└ĒĘĮĘ©ĪŻ¼FļAČ╬Ż¼│ŻęŖĄ──Ėę║ÅU╦«╠Ä└ĒĘĮĘ©░³└©Ż║╗ņ─²│┴ĄĒĘ©Īó╔·╬’Ę©Īó─żĘ©Ą╚ĪŻĄ½į┌æ¬ė├╔Ž╩÷ĘĮĘ©╠Ä└Ē─Ėę║ÅU╦«ĢrŠ∙ę╗Č©│╠Č╚Ąž┤µį┌ī”┐╔╚▄ąįCOD ╠Ä└Ēą¦┬╩Ą═Īó╠Ä└ĒĢrķgķL╝░╠Ä└Ē│╔▒Š▌^Ė▀Ą╚å¢Ņ}ĪŻĶF╠╝╬óļŖĮŌĘ©Ż©ėųĘQā╚ļŖĮŌĘ©Īó┴ŃārĶFĘ©Ą╚Ż®ę“Š▀ėą─▄║─Ą═Ż¼╠Ä└Ēą¦┬╩Ė▀Ż¼─▄ē“╠ßĖ▀ÅU╦«┐╔╔·╗»ąįĄ╚ā׳cŻ¼Į³Äū─Ļį┌ėĪ╚ŠĪóųŲ╦ÄĪó▐r╦ÄĪó└¼╗°ØB═Ėę║Ą╚ļyĮĄĮŌėąÖCÅU╦«Ą─╠Ä└ĒųąĄ├ĄĮ┴╦ÅVĘ║æ¬ė├ĪŻ╬óļŖĮŌĘ©Ą─īŹ┘|╩ŪįŁļŖ│žĘ┤æ¬Ż¼ŲõÖC└Ēų„ę¬░³└©č§╗»▀ĆįŁĪó╬’└Ē╬³ĖĮĪóą§─²│┴ĄĒ║═╬óļŖł÷ą¦æ¬Ą╚ČÓĘN╬’└Ē╗»īWū„ė├ĪŻ
▒Š╬─▓╔ė├ĶF╠╝╬óļŖĮŌĘ©ī”─Ėę║ÅU╦«▀MąąŅA╠Ä└Ē蹊┐Ż¼ų„ę¬┐╝▓ņĘ┤æ¬ĢrķgĪóĶFĘ█═Č╝ė┴┐ĪóFe/CŻ©┘|┴┐▒╚Ż®ĪópH ęį╝░ŲžÜŌ╦┘┬╩ī”ÅU╦«ųąCOD ╝░PVA ╠Ä└Ēą¦╣¹Ą─ė░ĒæŻ¼▓ó═©▀^š²Į╗īŹ“×┤_Č©─Ėę║ÅU╦«Ą─ūŅ╝č╠Ä└ĒŚl╝■ĪŻ▀@į┌─Ėę║ÅU╦«Ą─╠Ä└Ēųą▀Ć╬┤ęŖł¾Ą└ĪŻ
1 ▓─┴Ž║═ĘĮĘ©
1.1 ÅU╦«Ą─╦«┘|╠žš„
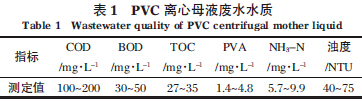
▒ŠīŹ“×╦∙ė├ÅU╦«▓╔ūį─│┤¾ą═┬╚ēA╗»╣żŲ¾śIĄ─PVC Š█║Ž╣żČ╬ĪŻįōŲ¾śI▓╔ė├Ąõą═Ą─ļŖ╩»Ę©æęĖĪŠ█║Ž╣ż╦ć▀MąąPVC ╔·«aĪŻÅU╦«Ą─▓┐Ęųųžę¬╦«┘|ųĖś╦╚ń▒Ē1╦∙╩ŠĪŻ
1.2 ų„ę¬āxŲ„╝░Ęų╬÷ĘĮĘ©
āxŲ„Ż║COD ┐ņ╦┘£yČ©āxŻ©├└ć°╣■ŽŻŻ¼DRB200Ż®Ż╗BOD ┐ņ╦┘£yČ©āxŻ©├└ć°╣■ŽŻŻ¼Trak ó“Ż®Ż╗▒Ńöy╩ĮĘų╣Ō╣ŌČ╚ėŗŻ©├└ć°╣■ŽŻŻ¼DB2800Ż®Ż╗┐éėąÖC╠╝Ęų╬÷āxŻ©╚š▒ŠŹuĮ“Ż¼TOC-L CPHŻ®Ż╗pH ėŗŻ©PHS-3CŻ®ĪŻ
Ęų╬÷ĘĮĘ©Ż║COD ║═BOD ▓╔ė├┐ņ╦┘£yČ©āx£yČ©ĪŻPVA ▓╔ė├Ęų╣Ō╣ŌČ╚Ę©£yČ©ĪŻTOC ▓╔ė├┐éėąÖC╠╝Ęų╬÷āx£yČ©ĪŻØßČ╚ĪóNH3-N ║═┐éĶFĘųäe▓╔ė├APHA ś╦£╩ĘĮĘ©ųąĄ─#2130BĪó#4500C ║═#3500B£yČ©ĪŻ
1.3 īŹ“×ĘĮĘ©
īŹ“×▓╔ė├ų▒ÅĮ×ķ50 mmŻ¼Ė▀×ķ450 mmĄ─ėąÖC▓Ż┴¦╣▄▀MąąĶF╠╝╬óļŖĮŌĘ©Ą─ņoæBå╬ę“╦žīŹ“×Īóš²Į╗īŹ“×╝░“×ūCīŹ“×ĪŻīŹ“×ķ_╩╝Ū░Ż¼īó▀BĮėėą─z╣▄Ą─ŲžÜŌ╔░Ņ^ų├ė┌ėąÖC▓Ż┴¦╣▄Ąū▓┐Ż¼─z╣▄┴Ēę╗Č╦ę└┤╬▀BĮė┴„┴┐ėŗ╝░┐šÜŌ▒├ĪŻīŹ“×čbų├╚ńłD1╦∙╩ŠĪŻ
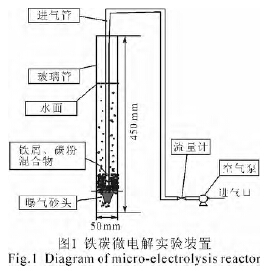
īŹ“×▓╔ė├ĶFĘ█ū„×ķ║Ļė^Ļ¢śOŻ¼┤¾Ņw┴Ż╗Ņąį╠┐ū„×ķ║Ļė^ĻÄśOĪŻīŹ“×Ū░Ż¼╗Ņąį╠┐ė├ŽĪ┴“╦ßĮ■┼▌12h ║¾ė├╚źļxūė╦«Ę┤Å═ŪÕŽ┤Ųõ▒Ē├µ╬█╚Š╬’Ż¼╚╗║¾▀Mąą’¢║═╬³ĖĮęį┼┼│²╬³ĖĮū„ė├ī”─┐ś╦╬’┘|╚ź│²┬╩£yČ©ĮY╣¹Ą─Ė╔ö_ĪŻ
1.3.1ņoæBå╬ę“╦žīŹ“×
┐╝▓ņĘ┤æ¬ĢrķgĪóĶFĘ█═Č╝ė┴┐ĪóFe/CĪópHĪóŲžÜŌ╦┘┬╩ī”─┐ś╦╬’┘|╠Ä└Ēą¦╣¹Ą─ė░ĒæĪŻ├┐ĮMīŹ“×ŲĮąąųžÅ═3┤╬ĪŻŠ▀¾wīŹ“×▀^│╠×ķŻ║īóę╗Č©┴┐Ą─ĶFĘ█║═╗Ņąį╠┐Ą─╗ņ║Ž╬’╝░500 mL ęčš{╣ØpH ║¾Ą──Ėę║ÅU╦«ė╔╔ŽĘĮ╝ė╚ļ▓Ż┴¦╣▄ā╚ĪŻīó┴„┴┐ėŗš{╣Øų┴ųĖČ©ŲžÜŌ╦┘┬╩║¾ķ_╩╝ėŗĢrĪŻ«ö▀_ĄĮŅAČ©Ą─Ę┤æ¬Ģrķg║¾Ż¼š{╣ØÅU╦«Ą─pH ų┴ēAąį▀Mąąą§─²│┴ĄĒĪŻņoų├30 min ║¾╚Ī╔ŽŪÕę║▀^×V£yČ©│÷╦«COD ║═PVA ║¼┴┐ĪŻ╦∙┤_Č©Ą─Ė„ę“╦žĄ─│§╩╝Śl╝■×ķŻ║ĶFĘ█═Č╝ė┴┐×ķ30 g/LĪópH ųĄ=3ĪóFe/C ×ķ1Ī├1ĪóŲžÜŌ╦┘┬╩×ķ0.6 L/minĪŻī”├┐éĆė░Ēæę“╦ž▀Mąąā×╗»ĢrŻ¼╩ūŽ╚╣╠Č©Ųõ╦¹ę“╦žŻ¼═©▀^£yČ©įōę“╦ž╚Ī▓╗═¼öĄųĄĢrŽÓæ¬ÅU╦«Ą─COD ║═PVA ╚ź│²┬╩Ż¼Å─Č°┤_Č©įōę“╦žĄ─ūŅ╝čųĄŻ¼į┘ė├┤╦ųĄ╚Ī┤·│§╩╝Śl╝■ųąįōę“╦žĄ─ŽÓæ¬ųĄŻ¼īóą▐ėå║¾Ą─Śl╝■ū„×ķŽ┬ę╗éĆę“╦žā×╗»ĢrĄ─│§╩╝Śl╝■Ż¼ų▒ų┴═Ļ│╔╦∙ėąę“╦žĄ─ā×╗»ĪŻĖ„ė░Ēæę“╦ž╚ĪųĄ╚ńŽ┬ĪŻĘ┤æ¬ĢrķgŻ║1Īó2Īó3Īó4Īó5Īó6hŻ╗ĶFĘ█═Č╝ė┴┐Ż║2Īó4Īó10Īó21Īó30Īó40Īó50 g/LŻ╗Fe/CŻ║3Ż║1Īó2Ż║1Īó3Ż║2Īó1Ż║1Īó2Ż║3Īó1Ż║2Īó1Ż║3Ż╗pHŻ║1Īó2Īó3Īó4Īó5Īó6Īó7Ż╗ŲžÜŌ╦┘┬╩Ż║0.2Īó0.4Īó0.6Īó0.8Īó1 L/minĪŻ
1.3.2š²Į╗īŹ“×
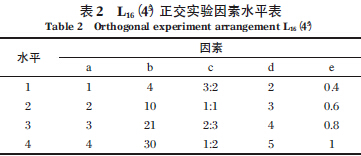
×ķ½@Ą├ūŅ╝čĄ─╠Ä└Ēą¦╣¹Ż¼š²Į╗īŹ“×Ė„ė░Ēæę“╦žĄ─╚ĪųĄ³cį┌å╬ę“╦žīŹ“×╦∙┤_Č©Ą─ŲĮ║Ō³cĖĮĮ³▀xō±ĪŻ▓╔ė├L16 Ż©45Ż®Ą─š²Į╗īŹ“×▒Ē2 蹊┐aŻ║Ę┤æ¬ĢrķgŻ©hŻ®ĪóbŻ║ĶFĘ█═Č╝ė┴┐Ż©g/LŻ®ĪócŻ║Fe/CĪódŻ║pHĪóeŻ║ŲžÜŌ╦┘┬╩Ż©L/minŻ®ī”COD╚ź│²ą¦┬╩Ą─ŠC║Žė░ĒæĪŻ├┐ĮMīŹ“×ŲĮąą▀Mąą3 ┤╬ĪŻš²Į╗īŹ“×ę“╦ž╝░╦«ŲĮęŖ▒Ē2ĪŻ
1.3.3“×ūCīŹ“×
īóš²Į╗īŹ“×┤_Č©Ą─ūŅ╝čĘ┤æ¬Śl╝■ųžÅ═▀Mąą4 ┤╬Ż¼Ęųäe£yČ©įō╠Ä└ĒŚl╝■Ž┬CODĪóPVAĪóTOCĪóNH3-NĪóØßČ╚Ą─╚ź│²┬╩╝░┐éĶF║¼┴┐ĪŻ
2 ĮY╣¹┼cėæšō
2.1 ņoæBå╬ę“╦žė░ĒæīŹ“×
2.1.1Ę┤æ¬ĢrķgĄ─ė░Ēæ
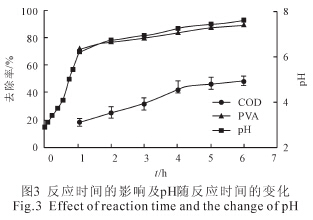
Ę┤æ¬Ģrķgī”─Ėę║ÅU╦«COD ║═PVA ╚ź│²┬╩Ą─ė░Ēæ╚ńłD3 ╦∙╩ŠĪŻ«öĘ┤æ¬Ģrķg▀_ĄĮ4h ų«Ū░Ż¼Č■š▀╚ź│²┬╩ļSĘ┤æ¬ĢrķgĄ─į÷╝ėŠ∙│╩¼F’@ų°į÷╝ė┌ģä▌Ż¼ų«║¾ät┌ģė┌ŠÅ┬²ĪŻįōĮY╣¹┼cŲõ╦¹Ą─蹊┐ĮY╣¹ŽÓ╦ŲĪŻ
╚ńłD2 ╦∙╩ŠŻ¼PVA Ą─ĮĄĮŌęį[H]▀ĆįŁ×ķų„Ż¼ĪżOHč§╗»×ķ▌oĪŻį┌[H]╗“ĪżOH Ą─ū„ė├Ž┬Ż¼PVA ╩ūŽ╚├ōĄ¶ę╗ĘųūėH2 ╗“H2O öÓµ£×ķ║¼RĪżĄ─ąĪĘųūė╬’┘|ĪŻRĪżĮø▀Mę╗▓ĮĄ─Ųń╗»╗“Į╗╗źū„ė├┐╔╔·│╔═¬╗“Ž®┤╝Ż¼▓óūŅĮKĄV╗»ĪŻ
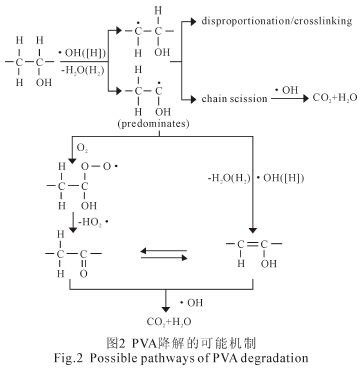
«öĘ┤æ¬Ģrķg▌^Č╠ĢrŻ¼¾wŽĄā╚▓┐«a╔·Ą─[H]ĪóĪżOH ęį╝░Fe2+Ą─öĄ┴┐▌^╔┘ĪŻ┤╦ĢrŻ¼¾wŽĄā╚č§╗»▀ĆįŁū„ė├╝░║¾└mĄ─ą§─²│┴ĄĒū„ė├Š∙▓╗’@ų°Ż¼ę“┤╦ī”─┐ś╦╬’┘|Ą─╚ź│²┬╩▌^Ą═ĪŻļSų°Ę┤æ¬ĢrķgĄ─čėķLŻ¼COD ║═PVA Ą─╚ź│²┬╩┌ģė┌ĘĆČ©ĪŻ▀@ų„ę¬╩Ūę“×ķļSų°Ę┤æ¬▀MąąŻ¼¾wŽĄųØuį÷┤¾Ą─pH ╝ė┐ņ┴╦ĶF▒Ē├µ┴u╗∙╗»║Ž╬’Ą─ą╬│╔Ż¼▀MČ°ūĶĄK┴╦ĶFå╬┘|┼cÅU╦«ų«ķgĄ─ļŖūė▀węŲĪŻ┤╦ĢrŻ¼└^└mčėķLĘ┤æ¬ĢrķgŻ¼─┐ś╦╬’┘|Ą─╚ź│²┬╩īó▓╗į┘’@ų°į÷╝ėĪŻė╔łD3 ┐╔ų¬Ż¼PVA Ą─╚ź│²┬╩├„’@Ė▀ė┌CODĪŻ▀@┐╔─▄╩Ūė╔ė┌ŽÓ▒╚ė┌Ųõ╦¹ąĪĘųūėėąÖC╬’┘|Č°čįŻ¼[H] Ė³ęūė┌┼cPVA ▀Mąą├ōH2 Ę┤æ¬ĪŻ┤╦═ŌŻ¼ŽÓ▒╚ė┌╚▄ĮŌæBĄ─ėąÖC╬’Č°čįŻ¼ĶFļxūėĄ─┴u╗∙Įj║Ž╬’ī”─z¾wæBPVA Ą─ą§─²│┴ĄĒą¦╣¹ę▓Ė³║├ĪŻ┐╝æ]ĄĮ╔Ž╩÷ę“╦žŻ¼ų«║¾īŹ“ץ─Ę┤æ¬ĢrķgŠ∙▀x╚Ī4hĪŻ
2.1.2ĶFĘ█═Č╝ė┴┐Ą─ė░Ēæ
ĶFĘ█═Č╝ė┴┐ī”COD ║═PVA Ą─╚ź│²┬╩Ą─ė░Ēæ╚ńłD4 ╦∙╩ŠĪŻCOD ║═PVA Ą─╚ź│²┬╩ļSų°ĶFĘ█═Č╝ė┴┐Ą─į÷╝ėŠ∙│╩¼FŽ╚į÷╝ė║¾ĘĆČ©Ą─┌ģä▌ĪŻ«öŲõ═Č╝ė┴┐│¼▀^10 g/L ĢrŻ¼COD ║═PVA Ą─╚ź│²┬╩┌ģė┌ĘĆČ©Ż¼Ęųäe×ķ41%║═78%ĪŻįōĮYšō┼cŲõ╦¹čąŠ┐ĮY╣¹ŽÓ╦ŲĪŻ
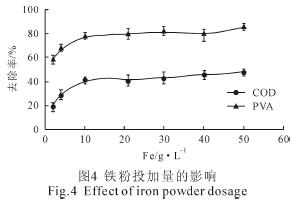
ĶFå╬┘|═Č╝ė┴┐╩Ūė░ĒæįōĘĮĘ©╚ź│²┬╩Ą─ųžę¬ę“╦žų«ę╗ĪŻĶFå╬┘|│²┐╔ęį┼cH+ū„ė├«a╔·[H]═ŌŻ¼▀Ć┐╔ęįū„×ķ─┐ś╦╬█╚Š╬’┘|Ą─č§╗»▀ĆįŁł÷╦∙ĪŻ«öĶFĘ█═Č╝ė┴┐▀^ąĪĢrŻ¼¾wŽĄā╚«a╔·Ą─[H]ĪóĶFļxūėöĄ┴┐ęį╝░╦∙─▄╠ß╣®Ą─č§╗»▀ĆįŁł÷╦∙Š∙▌^╔┘Ż¼ī”PVA Ą─├ōÜõĪóą§─²│┴ĄĒ╝░č§╗»▀ĆįŁū„ė├Š∙▌^╚§ĪŻę“┤╦Ż¼į┌┤╦Śl╝■Ž┬PVA Ą─╚ź│²┬╩▌^Ą═ĪŻė╔Ę┤款wŽĄCOD/TOC ųĄ▌^┤¾Ż©COD/TOC=5.1Ż®┐╔ų¬Ż¼¾wŽĄųą▀Ć┐╔─▄┤µį┌▌^ČÓĄ─║¼’¢║═¤Nµ£Ą─╬’┘|ĪŻę“┤╦Ż¼į┌[H]▌^╔┘Ą─ŪķørŽ┬Ż¼š¹éĆ¾wŽĄCOD Ą─╚ź│²ą¦┬╩ę▓▌^Ą═ĪŻ«öĶFĘ█═Č╝ė┴┐▀^┤¾ĢrŻ¼¾wŽĄ┐╔į┌Č╠Ģrķgā╚«a╔·▀^┴┐Ą─[H]ĪŻė╔ė┌[H]ų«ķg┐╔ą╬│╔H2Ż¼ę“┤╦īó£p╚§ī”¾wŽĄā╚▓┐Ą─├ōÜõū„ė├[6]ĪŻ┤╦═ŌŻ¼╦▓ķgĘeŠ█Ą─▀^┴┐Fe2+┐╔ęį║═ĪżOH Ę┤æ¬Ż¼▀MČ°£p╚§ī”─┐ś╦╬’┘|Ą─č§╗»ĪŻčąŠ┐▒Ē├„Ż¼▀^┴┐Ą─ĶFå╬┘|┐╔ī¦ų┬Ę┤款wŽĄ░ÕĮYŻ¼▀MČ°ĮĄĄ═╠Ä└Ēą¦┬╩[6]ĪŻŠC╔Ž╦∙╩÷Ż¼į┌║¾└mīŹ“×ųąĶFĘ█Ą─ė├┴┐▀x×ķ10 g/LĪŻ
2.1.3 Fe/C Ą─ė░Ēæ
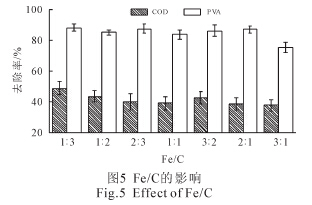
Fe/C ī”Ę┤æ¬Ą─ė░Ēæ╚ńłD5 ╦∙╩ŠĪŻļSų°╗Ņąį╠┐║¼┴┐Ą─į÷╝ėŻ¼COD ║═PVA Ą─╚ź│²┬╩š¹¾w╔ŽČ╝│╩¼Fį÷╝ėĄ─┌ģä▌ĪŻ
Fe/C ų„ę¬ė░Ēæ╬óļŖĮŌĘ┤æ¬ųą║Ļė^įŁļŖ│žĄ─ą╬│╔╝░ĶFļxūėĄ─╚▄│÷╦┘┬╩ĪŻ«öFe/C ▌^┤¾ĢrŻ¼å╬╬╗¾wĘeā╚ĶFĘ█║═╗Ņąį╠┐╗ņ║Ž▓╗Š∙Ż¼ą╬│╔Ą─įŁļŖ│žöĄ┴┐▌^╔┘Ż¼ļŖ╗»īWū„ė├▌^╚§ĪŻę“┤╦Ż¼COD ║═PVA Ą─╚ź│²┬╩▌^Ą═ĪŻčąŠ┐▒Ē├„Ż¼«ö▓╔ė├╬┤╠Ä└ĒĄ─╗Ņąį╠┐Ą─║¼┴┐į÷╝ėĄĮę╗Č©│╠Č╚ĢrŻ¼╗Ņąį╠┐ī”ėąÖC╬’Ą─╬³ĖĮ│╔×ķų„ī¦ū„ė├ĪŻ╬³ĖĮū„ė├│²┴╦ī”ėąÖC╬’Ą─╚ź│²┬╩ąĪė┌╬óļŖĮŌū„ė├═ŌŻ¼▀Ć─▄ęųųŲ╬óļŖĮŌĘ┤æ¬ĪŻę“┤╦Ż¼╗Ņąį╠┐Ą─║¼┴┐▓╗ę╦▀^Ė▀ĪŻ▓╗═¼ė┌Ųõ╦¹čąŠ┐ĮY╣¹Ż¼▒ŠīŹ“×į┌Fe/C ▌^ąĪĢr╠Ä└Ēą¦╣¹▌^║├ĪŻ▀@┐╔─▄ų„ę¬╩Ūė╔ė┌▒ŠčąŠ┐▓╔ė├ĶFĘ█×ķĻ¢śOČ°ī¦ų┬Ą─ĪŻŽÓī”ė┌ŽÓ═¼┘|┴┐Ą─ĶFą╝Č°čįŻ¼ĶFĘ█Ą─▒╚▒Ē├µĘeĖ³┤¾Ż¼ę“┤╦«a╔·Ą─║Ļė^įŁļŖ│žĖ³ČÓĪŻĶbė┌╔Ž╩÷įŁę“Ż¼║¾└mīŹ“×ųąFe/C ▀x×ķ1Ī├2ĪŻ
2.1.4 pH Ą─ė░Ēæ
pH ī”Ę┤æ¬Ą─ė░Ēæ╚ńłD6 ╦∙╩ŠĪŻ«öpH<2 ĢrŻ¼COD║═PVA Ą─╚ź│²┬╩▌^Ė▀ĪŻļSų°pH ųĄĄ─į÷┤¾Ż¼COD ║═PVA ╚ź│²┬╩│╩¼FųØu£pąĪĄ─┌ģä▌ĪŻįōĮY╣¹┼cŲõ╦¹čąŠ┐ĮYšōŽÓ╦Ų[13Ż¼25]ĪŻ
╚ń╩ĮŻ©1Ż®╦∙╩ŠŻ¼H+ų▒Įėģó┼cĶF╠╝╬óļŖĮŌĘ┤æ¬Ż¼ę“┤╦Ųõ┤¾ąĪī”─┐ś╦╬█╚Š╬’╚ź│²┬╩Ą─ė░Ēæų┴ĻPųžę¬ĪŻ
O2Ż©gŻ®+4H+Ż©aqŻ®+4eĪ·2H2OŻ©E=+1.23 VŻ®Ż©1Ż®
O2Ż©gŻ®+2H+Ż©aqŻ®+2eĪ·2H2O2Ż©aqŻ®Ż©E=+0.68 VŻ®Ż©2Ż®
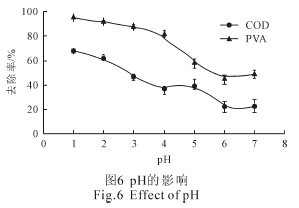
┤╦═ŌŻ¼pH Ą─┤¾ąĪė░ĒæPVA Ą─┤µį┌ą╬æBĪóĻ¢śOĶFļxūėĄ─╚▄│÷╦┘┬╩╝░[H]Ą─öĄ┴┐ĪŻ«öpH ▌^Ą═ĢrŻ¼PVA ╚▄ĮŌČ╚▌^Ą═[11Ż¼ 26]ĪŻ┤╦ĢrŻ¼Fe2+Ą─╚▄│÷╦┘┬╩▌^┐ņ▓ó┐╔«a╔·┤¾┴┐Ą─[H][20]ĪŻę“┤╦Ż¼¾wŽĄā╚▓┐Ą─├ōÜõū„ė├║═ą§─²│┴ĄĒū„ė├▌^×ķ’@ų°ĪŻ┤╦═ŌŻ¼▌^Ą═Ą─pH ┐╔£p╚§ĶFļxūėĄ─┴u╗∙Įj║Ž╬’ī”ĶF▒Ē├µĄ─Ė¶ļxū„ė├Ż¼×ķėąÖC╬’╠ß╣®Ė³ČÓĄ─č§╗»▀ĆįŁł÷╦∙ĪŻĄ½╩ŪŻ¼pH ę▓▓╗╩ŪįĮĄ═įĮ║├ĪŻ«öpH ▀^Ą═ĢrŻ¼įōĘĮĘ©ī”─┐ś╦╬’┘|Ą─╚ź│²┬╩┌ģė┌ĘĆČ©ĪŻ┤╦ĢrŻ¼└^└mĮĄĄ═pHųĄīóŽ¹║─┤¾┴┐Ą─╦߯¼▓óī¦ų┬Ļ¢śOĶFĄ─▀^┴┐╚▄ĮŌĪŻ▓╗╣▄╩Ū╦ߥ─Ž¹║─Ż¼Ļ¢śOĄ─Ž¹║─Ż¼▀Ć╩Ūė╔ė┌Ļ¢śOFe ▀^┴┐╚▄ĮŌČ°į┌ļS║¾▀^│╠ųą«a╔·Ą─▀^┴┐FeŻ©OHŻ®2 ╝░FeŻ©OHŻ®3 │┴ĄĒĄ─╠Ä└ĒŻ¼Č╝īóį÷╝ė╠Ä└ĒĄ─│╔▒ŠŻ¼▀MČ°ĮĄĄ═įōĘĮĘ©Ą─ąįār▒╚ĪŻŠC║Ž┐╝æ]╠Ä└Ēą¦┬╩╝░│╔▒ŠŻ¼║¾└mīŹ“×▀xō±į┌pH=2 Ą─Śl╝■Ž┬▀MąąĪŻ
2.1.5ŲžÜŌ╦┘┬╩Ą─ė░Ēæ
ŲžÜŌ╦┘┬╩ī”COD ║═PVA ╚ź│²┬╩Ą─ė░Ēæ╚ńłD7╦∙╩ŠĪŻCOD Ą─╚ź│²┬╩ļSų°ŲžÜŌ╦┘┬╩Ą─į÷╝ė│╩¼FŽ╚į÷╝ė║¾ĮĄĄ═Ą─┌ģä▌ĪŻ«öŲžÜŌ╦┘┬╩×ķ0.8 L/min ĢrŻ¼Ųõ╚ź│²┬╩×ķ67%ĪŻPVA ╚ź│²┬╩ļSų°ŲžÜŌ╦┘┬╩Ą─į÷╝ė│╩¼FŽ╚į÷╝ė║¾ĘĆČ©Ą─┌ģä▌Ż¼«öŲžÜŌ╦┘┬╩▀_ĄĮ0.6 L/min ū¾ėęĢrŻ¼Ųõ╚ź│²┬╩×ķ94%ĪŻ
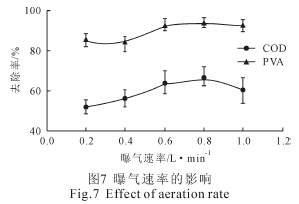
ė╔╩ĮŻ©1Ż®ĪóŻ©2Ż®ų¬Ż¼ŲžÜŌ▓╗āH┐╔ęį╠ßĖ▀¾wŽĄĄ─č§╗»ąįŻ©E=1.23 VŻ®Ż¼▀Ć┐╔«a╔·╔┘┴┐Ą─H2O2ĪŻė╔ė┌Fe2+Ą─┤µį┌Ż¼¾wŽĄā╚▓┐┐╔ęįą╬│╔╔┘┴┐Ą─Fenton įć䮯¼▀MČ°«a╔·Š▀ėąĖ³ÅŖč§╗»ąįĄ─ĪżOHŻ©E=2.80 VŻ®ĪŻŲžÜŌ▀Ć┐╔╝ė╦┘Fe3+Ą─ą╬│╔ĪŻ┼cFe2+ŽÓ▒╚Ż¼Fe3+Š▀ėąĖ³║├Ą─ą§─²│┴ĄĒą¦╣¹[11]ĪŻ╚╗Č°Ż¼«öŲžÜŌ╦┘┬╩▀^┤¾ĢrŻ¼│²┐šÜŌųąĄ─O2 īó£p╚§[H]ī”ėąÖC╬’Ą─▀ĆįŁū„ė├═ŌŻ¼¾wŽĄā╚HCO3-Ą╚ĪżOHūįė╔╗∙ŪÕ│²ä®Ą─öĄ┴┐ę▓īóį÷╝ėŻ¼▀MČ°£p╚§¾wŽĄā╚▓┐Ą─č§╗»ū„ė├[2]ĪŻę“┤╦Ż¼«öŲžÜŌ╦┘┬╩│¼▀^0.8 L/min ĢrŻ¼COD╚ź│²┬╩│╩¼F┴╦ĮĄĄ═Ą─┌ģä▌ĪŻŠC╔Ž╦∙╩÷Ż¼ŲžÜŌ╦┘┬╩æ¬▀xō±0.8 L/minĪŻ
2.2 ūŅ╝čīŹ“׌l╝■Ą─┤_Č©
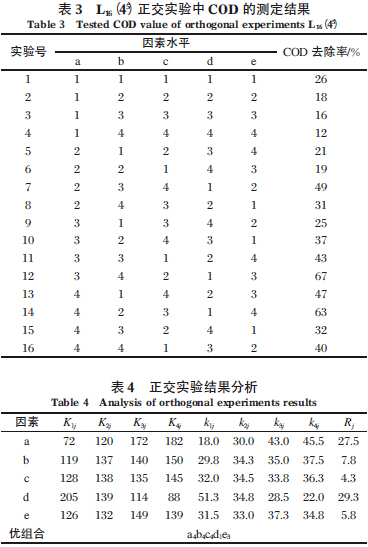
ė╔L16Ż©45Ż®š²Į╗▒Ē╦∙Ą├Ą─Ė„īŹ“׌l╝■Ž┬COD Ą─╚ź│²┬╩┴ąė┌▒Ē3 ųąĪŻĖ∙ō■▒Ē3 ┐╔ėŗ╦Ń│÷KijĪókij ╝░RjŻ¼Š▀¾wĮY╣¹┴ąė┌▒Ē4 ųąĪŻŲõųąŻ¼Kij ×ķĄ┌j ┴ąę“╦žĄ┌i ╦«ŲĮ╦∙ī”æ¬Ą─COD ╚ź│²┬╩ų«║═Ż©Ųõųąi=1Ż¼2Ż¼3Ż¼4Ż╗j=aŻ¼bŻ¼cŻ¼dŻ¼eŻ®Ż╗ kij ×ķKij Ą─ŲĮŠ∙ųĄŻ╗Rj ×ķĄ┌j ┴ąę“╦žĄ─śO▓ŅĪŻė╔▒Ē4┐╔ų¬Ż¼▒ŠīŹ“×╦∙ā×╗»Ą─5 éĆė░Ēæę“╦žį┌╦∙▀xō±Ą─╚ĪųĄĘČć·ā╚ī”─Ėę║ÅU╦«COD ╚ź│²┬╩ė░ĒæĄ─Ēśą“×ķRd=29.3>Ra=27.5>Rb=7.8>Re=5.8>Rc=4.3Ż¼╝┤pH ī”COD╚ź│²┬╩Ą─ė░ĒæūŅ┤¾Ż¼Ųõ┤╬╩ŪĘ┤æ¬ĢrķgĪŻĶFĘ█═Č╝ė┴┐ĪóŲžÜŌ╦┘┬╩ęį╝░Fe/C ī”COD ╚ź│²┬╩Ą─ė░ĒæŽÓī”▌^ąĪĪŻį┌▒ŠīŹ“×╦∙▀xĄ─ā×╗»ģóöĄųąŻ¼ūŅ╝čę“╦žĮM║Ž×ķa4b4c4d1e3Ż¼╝┤Ę┤æ¬Ģrķg×ķ4hŻ¼ĶFĘ█═Č╝ė┴┐×ķ30 g/LŻ¼Fe/C ×ķ1Ī├2Ż¼pH ųĄ×ķ2Ż¼ŲžÜŌ╦┘┬╩×ķ0.8 L/minĪŻŠ▀¾wģóęŖhttp://www.dongaorq.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
2.3 ūŅ╝čŚl╝■Ž┬Ą─╠Ä└ĒĮY╣¹
į┌╔Ž╩÷ūŅ╝č╠Ä└ĒŚl╝■Ž┬Ż¼╠Ä└Ē║¾─Ėę║ÅU╦«ųąCODĪóPVA ║═TOC Ą─ŲĮŠ∙╚ź│²┬╩Ęųäe×ķŻ©67Ī└2Ż®%ĪóŻ©98Ī└1Ż®%║═Ż©55Ī└3Ż®%Ż¼BOD/COD ųĄÅ─0.3 ╠ßĖ▀ĄĮ0.5Ż¼┐╔╔·╗»ąįĄ├ĄĮ┴╦’@ų°╠ßĖ▀ĪŻ┤╦═ŌŻ¼ė╔╠Ä└ĒŪ░║¾ÅU╦«Ą─COD/TOCųĄė╔5.1 ĮĄĄĮ3.8 ┐╔ęį┐┤│÷Ż¼įō╠Ä└ĒŚl╝■ī”║¼ėą’¢║═¤Nµ£ŅÉ╬’┘|╗“Ųõ╦¹H į¬╦ž║¼┴┐▌^Ė▀Ą─ŅÉ╦Ų╬’┘|ėą║▄║├Ą─╚ź│²ą¦╣¹Ż¼▀@ę▓┐╔─▄╩Ū¾wŽĄ┐╔╔·╗»ąį╠ßĖ▀Ą─įŁę“ų«ę╗[28]ĪŻ┤╦═ŌŻ¼─Ėę║ÅU╦«ųąĄ─NH3-N ║═ØßČ╚ę▓═¼ĢrĄ├ĄĮ┴╦ę╗Č©│╠Č╚Ą─╚ź│²Ż¼Ųõ╚ź│²┬╩×ķ45%║═100%ĪŻļm╚╗įōĘĮĘ©ųąĶFå╬┘|Ą─╚▄ĮŌĢ■ī¦ų┬│÷╦«ųą║¼ėąĶFļxūėŻ¼Ą½£yČ©ĮY╣¹▒Ē├„Ż¼Įø▀^│┴ĄĒ║¾│÷╦«ųą┐éĶF║¼┴┐║▄Ą═ĪŻ┼c¼FļAČ╬æ¬ė├▌^×ķÅVĘ║Ą──żĘ©ęį╝░é„Įy╔·╬’Ę©ŽÓ▒╚Ż¼ĶF╠╝╬óļŖĮŌĘ©│²Š▀ėą╠Ä└ĒĢrķgČ╠Īó╠Ä└Ē│╔▒ŠĄ═Ą─ā׳c═ŌŻ¼▀Ć┐╦Ę■┴╦į┌▓╔ė├╔Ž╩÷2 ĘNĘĮĘ©╠Ä└Ē─Ėę║ÅU╦«Ģr┤µį┌Ą──żČ┬╚¹ęį╝░╬ó╔·╬’▓╗ęū┼ÓBĄ─╚▒³cĪŻ┤╦═ŌŻ¼ĶF╠╝╬óļŖĮŌĘ©▀Ć┐╔ęį┼cFenton Ę©╝░O3 č§╗»Ę©┬ō║Ž╩╣ė├Ż¼▀Mę╗▓Į╠ßĖ▀ī”─┐ś╦╬█╚Š╬’Ą─╠Ä└Ēą¦┬╩Ż¼ĮĄĄ═╠Ä└Ē│╔▒ŠĪŻ


