į§├┤╠ßĖ▀╬█─ÓģÆ觎¹╗»ę║ųą┴ūĄ─╗ž╩šą¦┬╩
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2016-9-24 9:10:11
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį
ĪĪĪĪ┴ū╩Ūę╗ĘNųžę¬Ą─╗»╣żįŁ┴Ž║═ĄV«a┘Yį┤Ż¼ÅVĘ║æ¬ė├ė┌╗»╣żĪó▌p╣żĄ╚ąąśIŻ¼Å─ĄV╬’ųąģó┼cĄĮ╦«¾wĪó═┴╚└Īó╔·╬’┼c╚╦¾wĄ─裣hųąŻ¼│╔×ķįņ│╔╦«¾wĖ╗ĀIB╗»Ą─ųžę¬╬█╚Š╬’ų«ę╗Ż¼═¼Ģr┴ūėų╩Ūę╗ĘN▓╗┐╔į┘╔·┘Yį┤Ż¼į┌ūį╚╗ĮńųąĮ³║§å╬Ž“裣hŻ¼ę“Č°┴ū┘Yį┤├µ┼Rų°ŁhŠ│╬█╚Š║═┘Yį┤ģTĘ”ā╔┤¾žĮ┤²ĮŌøQĄ─å¢Ņ}.Į³─ĻüĒŻ¼├└ć°Īó╚š▒ŠĪóÜWų▐Ą╚Ąžī”┴ūĄ─┐╔│ų└m└¹ė├Ė▀Č╚ųžęĢŻ¼Å─╔·╬’╝S▒Ń║═╬█╦«Īó╬█─Óųą╚ź│²║═╗ž╩š┴ūęč│╔×ķ¤ß³c蹊┐šnŅ}.│Ū╩ą╬█─ÓųąĖ╗║¼┴ūį¬╦žŻ¼į┌│Ū╩ą╬█╦«╠Ä└Ē▀^│╠ųąŻ¼│§│┴╬█─ÓĪó╗Ņąį╬█─Óųą┴ūĄ─║¼┴┐(ęįP2O5ėŗ)Ęųäe×ķ1%~3%Īó0.78%~4.3%Ż¼Įø╔·╬’╠Ä└Ē▀^│╠«a╔·Ą─╬█─Ó┤²│Ż£žģÆ觎¹╗»║¾Ż¼ŲõģÆ觎¹╗»ę║ųąš²┴ū║═░▒Ą¬ØŌČ╚┐╔▀_20~300 mg Īż L-1║═330~780 mg Īż L-1Ż¼×ķ┴ū╗ž╩š╠ß╣®┴╦žSĖ╗Ą─┘Yį┤Ż¼▀m║Žęį┴ū╦ßŌ}(CP)│┴ĄĒĘ©║═┴ū╦ßõ@µV(MAP)ĮYŠ¦Ę©╚ź│²║═╗ž╩š┴ū.蹊┐▒Ē├„Ż¼ęįCP║═MAPą╬╩Į╚ź│²║═╗ž╩š┴ūĄ─╣ż╦ć╩ŪūŅėąŪ░Š░Ą─═ŠÅĮŻ¼ę▓╩Ū─┐Ū░æ¬ė├ūŅČÓĄ─ĘĮĘ©.
ĪĪĪĪĮYŠ¦│²┴ūĄ─įŁ└Ē╩Ū▓╗═¼pHųĄŚl╝■Ž┬┐žųŲ╗»īW╬’┘|Ą─▐D╗»║═ŲĮ║Ō.─┐Ū░Ż¼ć°ā╚═ŌīWš▀ī”pHųĄĪó┴ū╦ß¹}ØŌČ╚ĪóŽÓĻPļxūėØŌČ╚╝░Š¦ĘNĄ╚ę“╦žī”┴ū╚ź│²ą¦╣¹Ą─ė░Ēæ▀Mąą┴╦┤¾┴┐Ą─蹊┐Ż¼▓óįOėŗčą░l▓╗═¼ĮYŠ¦Ę┤æ¬Ų„▀Mąą╣ż│╠īŹ█`æ¬ė├Ż¼Ą½╚į┤µį┌│┴ĄĒĘ┤æ¬Ą─┐žųŲå¢Ņ}ĪóĮYŠ¦«a╬’Ą─┘|┴┐Īóą╬æB╝░╗žė├å¢Ņ}.ĻPė┌MAPĘ©╠Ä└ĒģÆ觎¹╗»ę║Ą─蹊┐ł¾Ą└▌^ČÓŻ¼Ą½į┌Ca2+┼cCO2-3═¼Ģr┤µį┌Ą─Å═ļs¾wŽĄųąŻ¼ā╔š▀╣▓┤µī”┴ū│┴ĄĒą╬╩Į╝░MAPĘ┤æ¬ė░ĒæĄ─蹊┐▌^╔┘.
ĪĪĪĪ╬█─ÓģÆ觎¹╗»ę║ųą╝s║¼ėą20 mmol Īż L-1(ęįCėŗ)Ą─╠╝╦ß¹}Ż¼▀h▀h│¼▀^╬█╦«ųąĄ─║¼┴┐Ż¼Ūę«öpHųĄ┤¾ė┌9.0ĢrŻ¼╦«ųąĄ─╠╝╦ß¹}ēAČ╚ČÓęįCO2-3ą╬╩Į┤µį┌Ż¼ī”┴ū╚ź│²║═╗ž╩š▀^│╠«a╔·▓╗└¹ė░ĒæŻ¼┼cPO3-4ĖéĀÄĘ┤æ¬Ż¼ĮĄĄ═P╚ź│²┬╩.▒Š╬─蹊┐┴╦└¹ė├MAPĮYŠ¦Ę©╚ź│²╬█─ÓģÆ觎¹╗»ę║ųą┴ūĄ─ė░Ēæę“╦žŻ¼░³└©ā╔éĆ┐žųŲę“╦žĪ¬Ī¬╚▄ę║pHųĄ╝░n(Mg)/n(P)Ż¼2éĆĖ╔ö_ę“╦žĪ¬Ca2+ØŌČ╚ĪóCO2-3ØŌČ╚╝░ā╔š▀╣▓┤µī”MAPĮYŠ¦Ę┤æ¬Ą─ą¦┬╩╝░«a╬’ą╬æBĄ─ė░ĒæŻ¼ų╝į┌×ķÅ─ģÆ觎¹╗»ę║ųą╚ź│²║═╗ž╩š┴ū▀xō±ėąą¦╣ż╦ć║═Ę┤æ¬Śl╝■╠ß╣®ģó┐╝.
ĪĪĪĪ2 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ2.1 įć“×įŁ└Ē
ĪĪĪĪMAPĮYŠ¦¾wŽĄģó┼cĘ┤æ¬Ą─ų„ę¬ļxūėėąŻ║NH+4ĪóPO3-4ĪóMg2+Ż¼į┌╦«╚▄ę║¾wŽĄųąŻ¼╦³éā┐╔ęįH2PO-4ĪóHPO2-4ĪóPO3-4ĪóNH3ĪóMgOH+ĪóMgPO-4ĪóMgH2PO4+Ą╚ļxūėą╬æB┤µį┌Ż¼═©▀^ļxĮŌĪóĮj║ŽĪó│┴ĄĒ║═ĮYŠ¦Ę┤æ¬Ż¼ą╬│╔MgNH4PO4 Īż 6H2O║═Mg(OH)2Š¦¾w║═│┴ĄĒ.
ĪĪĪĪ┴ū╦ßŌ}¹}│┴ĄĒą╬╩ĮČÓśėŻ¼ų„ę¬░³└©CaHPO4 Īż 2H2O(┴ū╦ßÜõŌ}Ż¼Dicalcium phosphate dihydrateŻ¼DCPD)Ż¼Ca3(PO4)2(┴ū╦ß╚²Ō}Ż¼Tricalcium phosphateŻ¼TCP)Ż¼Ca4H(PO4)3 Īż 2.5H2O(┴ū╦ß╦─Ō}Ż¼Octacalcium phosphateŻ¼OCP)Ż¼Ca5(PO4)3OH(┴u╗∙┴ū╗ę╩»Ż¼HydroxyapatiteŻ¼HAP)║═Ca3(PO4)2ĪżnH2O(¤oČ©ą╬┴ū╦ßŌ}Ż¼Amorphous calcium phosphateŻ¼ACP)Ż¼ŲõųąHAPį┌¤ß┴”īW╔ŽūŅĘĆČ©.
ĪĪĪĪį┌╚▄ę║ųą╠╝╦ß¹}ų„ę¬ęįHCO-3║═CO2-3ā╔ĘNą╬╩Į┤µį┌Ż¼▓╗═¼pHųĄ¾wŽĄŽ┬ļxūėą╬æBį┌HCO-3ĪóCO2-3┼cH2CO3╚²š▀ų«ķgŽÓ╗ź▐D╗»Ż¼ęį20 mmol Īż L-1(ęįCėŗ)╠╝╦ß¹}ØŌČ╚×ķ└²Ż¼└¹ė├MINTEQ▄ø╝■─ŻöM▓╗═¼pHųĄŚl╝■Ž┬╠╝╦ß¹}Ą─┤µį┌ą╬╩ĮŻ¼ĮY╣¹╚ńłD 1╦∙╩Š.Å─łDųą┐╔ęį┐┤│÷Ż¼pHųĄį┌8.0~9.0ĢrŻ¼╠╝╦ß¹}ų„ę¬ęįHCO-3Ą─ą╬╩Į┤µį┌;pH┤¾ė┌9.0ĢrŻ¼╠╝╦ß¹}ķ_╩╝Ž“CO2-3ą╬╩Į▐D╗»Ż¼HCO-3║¼┴┐ųØu£p╔┘Ż¼CO2-3┼cPO3-4ĖéĀÄCa2+ĪóMg2+Ż¼╔·│╔CaCO3║═MgCO3│┴ĄĒŻ¼Å─Č°ĮĄĄ═┴ū╚ź│²┬╩Ż¼ė░Ē抦¾w╝āČ╚║═ą╬æB.
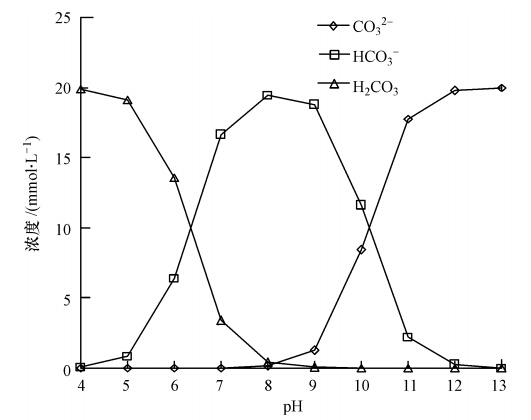
ĪĪĪĪłD 1 ▓╗═¼pHųĄŽ┬╠╝╦ß¹}Ą─┤µį┌ą╬æB
ĪĪĪĪ2.2 ā”éõę║Ą─┼õųŲ
ĪĪĪĪīóę╗Č©┴┐Ą─KH2PO4ĪóNH4ClĪóMgCl2 Īż 6H2OĪóCaCl2 Īż 2H2O║═NaHCO3Ęųäe╚▄ė┌╚źļxūė╦«ųąŻ¼┼õ│╔0.323 mol Īż L-1 PO3-4Īó2.064 mol Īż L-1 NH+4Īó1.290 mol Īż L-1 Mg2+Īó1.000 mol Īż L-1 Ca2+║═1.000 mol Īż L-1 CO2-3Ą─ā”éõę║.īŹ“×ųą╦∙ė├įć䮊∙×ķĘų╬÷╝ā.
ĪĪĪĪ2.3 īŹ“×▀^│╠
ĪĪĪĪ╩ę£ž(20~25Īµ)Śl╝■Ž┬į┌┴∙┬ōöć░ĶŲ„╔Ž▀MąąĘųĮM¤²▒ŁīŹ“ׯ¼öć░Ķ╦┘Č╚×ķ150 r Īż min-1.│²╠ž╩Ōšf├„Ż¼╬─ųą╦∙ųĖĄ─ØŌČ╚▒╚ųĄŠ∙×ķ─”Ā¢▒╚.
ĪĪĪĪīŹ“×ųą╣╠Č©┴ūĄ─┘|┴┐ØŌČ╚×ķ20 mg Īż L-1(Cp=0.645 mmol Īż L-1).░┤īŹ“×╦∙ąĶĄ─n(Mg)/n(N)/n(P)─”Ā¢▒╚2 : 8 : 1┼c6 : 8 : 1Ż¼Ž╚┐╝▓ņ▓╗═¼pHųĄŽ┬ā╔ĘN▓╗═¼─”Ā¢▒╚╝āMAPĘ┤æ¬Ą─┴ū╚ź│²ą¦╣¹Ż¼×ķ╠Į╦„Ca2+║═CO2-3ļs┘|ī”MAPĘ┤æ¬ė░Ēæ╠ß╣®║Ž▀mĄ─īŹ“×pHųĄ;╚╗║¾į┌╦∙▀xpHųĄŚl╝■Ž┬Ż¼┐╝▓ņļs┘|å╬¬Ü┤µį┌║═░┤šš1 : 1▒╚└²╣▓┤µĢrī”MAPĘ┤æ¬Ą─ė░ĒæŻ¼▒ŠīŹ“×ųą▀x╚Ī┴╦pH=7.8║═pH=9.5▀Mąą╔Ž╩÷ļs┘|ė░ĒæīŹ“×.Ė∙ō■┐╔─▄░l╔·Ą─╗»īW│┴ĄĒĘ┤æ¬Ż¼īó║¼PO3-4║═CO2-3ā”éõę║Ž╚╝ė╚ļĄĮ┤¾¤²▒ŁųąŻ¼╝ė╚ļ▀m┴┐╚źļxūė╦«ŽĪßīų┴Į³1.0 LŻ¼į┘ę└ō■īŹ“×įOČ©ųĄ╝ė╚ļ║¼Mg2+ĪóCa2+║═NH+4Ą─ā”éõę║Ż¼┤╦Ģr╚▄ę║¾wĘe×ķ1.0 LŻ¼čĖ╦┘Ą╬╝ė5.0 mol Īż L-1(╗“1.0 mol Īż L-1)NaOH║═5.0 mol Īż L-1(╗“1.0 mol Īż L-1)HClš{╣Ø╚▄ę║pHųĄų┴īŹ“×įOČ©ųĄŻ¼▓óęį┐ņ╦┘öć░Ķū„×ķĘ┤æ¬ķ_╩╝Ą─Ų³c.įOČ©Ę┤æ¬Ģrķg×ķ2.0 hŻ¼Ę┤æ¬▀^│╠ųąŻ¼Ą╬╝ė0.1 mol Īż L-1 NaOHš{╣Ø╚▄ę║Ą─pHųĄŻ¼╩╣╚▄ę║pHųĄŠS│ųį┌ęÄČ©ĘČć·ā╚(Ī└0.02).×ķ┐╝▓ņ▓╗═¼īŹ“׌l╝■Ž┬Ą─ĮYŠ¦Ę┤æ¬╦┘Č╚Ż¼į┌Ę┤æ¬ķ_╩╝║¾Ą─1Īó2Īó5Īó10Īó15Īó20Īó25Īó30Īó45Īó60Īó90Īó120 minĢrķg³c╚ĪśėŻ¼├┐┤╬╚Īśė10 mL.
ĪĪĪĪ2.4 ╦«śė┼c╣╠¾wśėŲĘŅA╠Ä└Ē
ĪĪĪĪįć“×ųą╦∙╚Ī╦«śėčĖ╦┘ė├0.45 ”╠mĄ─×V─ż▀^×VŻ¼▓ó┴ó╝┤╝ė╚ļ20 ”╠L(12 mol Īż L-1)Ą─HClŻ¼ĮKų╣│┴ĄĒ╗“ĮYŠ¦Ę┤æ¬Ż¼╦«śė┴¶┤²Ęų╬÷£yČ©.Ę┤æ¬╔·│╔Ą─╣╠¾w«a╬’Įø0.45 ”╠mĄ─╗ņ║Ž└wŠS×V─ż▀Mąą╣╠ę║ĘųļxŻ¼į┌╩ę£žŽ┬ūį╚╗’LĖ╔┴¶┤²Ęų╬÷£yČ©.
ĪĪĪĪ2.5 Ęų╬÷ĘĮĘ©║═āxŲ„
ĪĪĪĪ╦«śėĘų╬÷Ż║Š∙░┤šš╝ęŁhŠ│▒Żūo┐éŠų▀Mąą.Ca2+ĪóMg2+Ą─£yČ©▓╔ė├╗čµįŁūė╬³╩šĘ©(╚š┴óZ2000);š²┴ū╦ß¹}Ą─£yČ©▓╔ė├ŃfõR┐╣Ęų╣Ō╣ŌČ╚Ę©;░▒Ą¬Ą─£yČ©▓╔ė├Ōc╩Žįćä®Ęų╣Ō╣ŌČ╚Ę©.
ĪĪĪĪ╣╠¾w«a╬’ą╬æB║═│╔ĘųĘų╬÷Ż║└¹ė├XRD(Ą┬ć°BrukerŻ¼D8 Advance DMAX2RB)ĪóSEM-EDS(Ą┬ć°ZeissŻ¼EVO18)║═FTIR(├└ć°NICOLETŻ¼NEXUS870)Ęų╬÷Ę©ī”Ą├ĄĮĄ─ŽĄ┴ą«a╬’▀MąąĘų╬÷.
ĪĪĪĪ3 ĮY╣¹┼cėæšō
ĪĪĪĪ3.1 ▓╗═¼pHųĄī”MAPĮYŠ¦Ę┤æ¬Ą─ė░Ēæ
ĪĪĪĪģóšš─│╦«ÅSīŹļHģÆ觎¹╗»╔ŽŪÕę║Ą─│╔ĘųŻ¼īŹ“×įOČ©─ŻöM╦«śėųąCP=0.645 mmol Īż L-1Ż¼│§╩╝n(Mg): n(N): n(P)Ęųäe×ķ2 : 8 : 1┼c6 : 8 : 1Ż¼į┌pHųĄ×ķ8.0Īó8.5Īó9.0Īó9.5Īó10.0Śl╝■Ž┬▀MąąĘ┤æ¬Ż¼Ę┤æ¬2.0 h║¾┴ū╚ź│²┬╩ĮY╣¹╚ńłD 2a╦∙╩Š.łD 2a▒Ē├„Ż¼į┌īŹ“×ĘČć·ā╚Ż¼ļSų°pHųĄ╔²Ė▀Ż¼PĄ─╚ź│²┬╩’@ų°╠ßĖ▀Ż¼«öpHųĄ╔²Ė▀ĄĮ10.0ĢrŻ¼n(Mg)/n(P)=6 : 1Śl╝■Ž┬P╚ź│²┬╩┐╔▀_95.43%Ż¼┐╔┐┤│÷PĄ─│┴ĄĒ┴┐┼c╚▄ę║pHųĄ│╩š²ŽÓĻP.Ą½«öpH>9.5ĢrŻ¼P╚ź│²┬╩┼cpH=10.0Ą─╚ź│²┬╩▓ŅŠÓ▓╗┤¾Ż¼╠ßĖ▀▓╗ĄĮ10%Ż¼╝┤┤╦║¾į÷┤¾pHųĄī”╠ßĖ▀P╚ź│²┬╩Ą─žĢ½I▓╗┤¾.┤╦═ŌŻ¼ėąčąŠ┐▒Ē├„pHųĄ╩Ūė░Ēæ«aŲĘ┘|┴┐║═│┴ĄĒĘ┤æ¬ą¦╣¹Ą─ųžę¬ę“╦žŻ¼═§│ń│╝Ą╚ę▓ųĖ│÷pHųĄī”MAPŠ¦¾wĄ─ą╬│╔ė╚×ķĻPµIŻ¼▓óŪęŲõ╝āČ╚┼cpHųĄ│╩žōŽÓĻPŻ¼į┌│¼╝ā╦«¾wŽĄųąĘ┤æ¬Śl╝■pH>9.5Ż¼│┴ĄĒ«a╬’XRDĘų╬÷łDūVųąįļę¶ĘÕ│÷¼Fį÷ČÓŻ¼MAP╠žš„ĘÕ£p╚§Ż¼pH╔Ž╔²ų┴10.5ęį║¾Ż¼MAP╠žš„ĘÕÄū║§═Ļ╚½Ž¹╩¦.═©▀^Visual MINTEQ▄ø╝■▀Mąą┴╦▓╗═¼pHųĄŽ┬Ą─Ca2+ĪóMg2+ą╬æB╝░╗»īWŲĮ║Ō─ŻöMŻ¼─ŻöMėŗ╦ŃĢrMg2+ĪóCa2+ØŌČ╚Š∙×ķ5 mmol Īż L-1Ż¼Ca2+ĪóMg2+│┴ĄĒŲĮ║Ō─ŻöMĮY╣¹╚ńłD 2b╦∙╩ŠŻ¼Mg2+į┌pH>9.0Śl╝■Ž┬ķ_╩╝▐D╗»×ķMg(OH)2│┴ĄĒŻ¼▓óį┌pH=10.0ĢrŻ¼│┴ĄĒ┬╩▀_ĄĮ58.20%Ż¼Č°Ca2+ätį┌pH>12.0ęį║¾▓┼ķ_╩╝▐D╗»×ķCa(OH)2│┴ĄĒ.ę“Č°Ż¼pHųĄ▀^Ė▀▓ó▓╗▀mę╦ė┌MAPĮYŠ¦Ę┤æ¬Ą─▀MąąŻ¼Mg2+Ą─└¹ė├┬╩╝░MAPŠ¦¾w╝āČ╚Ģ■ļSų°pHųĄĄ─╔²Ė▀Č°ųØuĮĄĄ═.
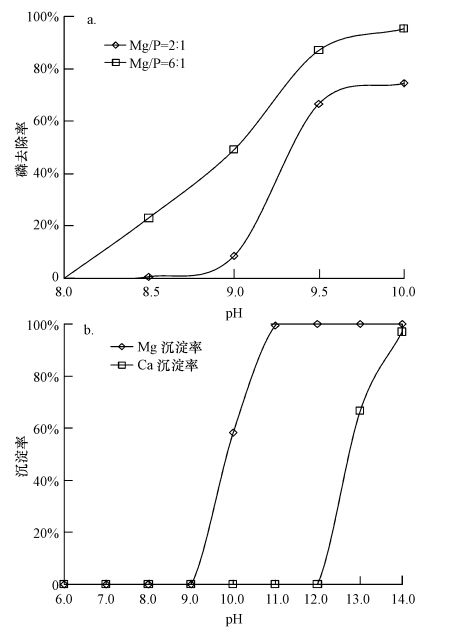
ĪĪĪĪłD 2 ▓╗═¼pHųĄĪó▓╗═¼n(Mg)/n(P)Śl╝■Ž┬┴ūĄ─╚ź│²┬╩(a)╝░▓╗═¼pHųĄŽ┬Ca2+ĪóMg2+│┴ĄĒ┬╩(b)
ĪĪĪĪ╚▄ę║ųąCP=0.645 mmol Īż L-1Īón(Mg):n(N):n(P)=2 : 8 : 1┼c6 : 8 : 1ĪópHųĄį┌9.5║═7.8Śl╝■Ž┬Ż¼MAPĮYŠ¦Ę┤æ¬▀^│╠ųą┴ūĄ─ØŌČ╚ūā╗»ŪķøręŖłD 3.ė╔łD 3┐╔ęį┐┤│÷Ż¼ļSų°Ę┤æ¬Ą─▀MąąŻ¼pH=9.5Śl╝■Ž┬Ż¼ā╔ĘN▓╗═¼n(Mg)/n(P)Ę┤款wŽĄųąPĄ─╚ź│²┬╩ųØu╔²Ė▀Ż¼Ūęn(Mg):n(P)=6 : 1Ą─Ę┤款wŽĄĘ┤æ¬╦┘┬╩▌^┤¾.WangĄ╚▓╔ė├PHREEQC│╠ą“ī”MAPĮYŠ¦Ę©╬█╦«╠Ä└Ē╣ż╦ć▀Mąą─Żą═╗»čąŠ┐Ż¼čąŠ┐▒Ē├„Ż║į┌Ą═Mg2+ØŌČ╚Śl╝■Ž┬Ż¼ę╗Č©pHųĄŽ┬MAPĄ─SIųĄśOęū╩▄Mg2+ØŌČ╚ūā╗»Ą─ė░ĒæŻ¼SIųĄŽ╚į÷┤¾║¾ĮĄĄ═Ż¼Ūęį┌Ą═pHųĄŚl╝■Ž┬Ż¼Mg2+ØŌČ╚ī”MAPĄ─SIųĄę▓ėą▌^┤¾ė░Ēæ.┤╦═ŌŻ¼į┌ĮYŠ¦šTī¦Ų┌š{╣ØpHųĄ┐╔ėąą¦┐žųŲ│╔║╦šTī¦ĢrķgŻ¼╣╩pHųĄ╩Ūė░ĒæĘ┤æ¬╦┘┬╩Ą─ųžę¬ę“╦ž.Å─łD 3ųąę▓┐╔┐┤│÷į┌īŹļHģÆ觎¹╗»╔ŽŪÕę║pH=7.8Ą─Śl╝■Ž┬Ż¼MAPĮYŠ¦Ę┤æ¬Äū║§¤oĘ©▀Mąą.ĮY║ŽÅ─ÅU╦«ųą╗ž╩š┴ū╦ß¹}Ą─╣ż│╠īŹ█`┐╔ų¬Ż¼š{╣Ø╚▄ę║pHųĄ╩Ū╠ßĖ▀P╚ź│²┬╩Ą─ėąą¦╩ųČ╬.ŠC║Žęį╔ŽpHųĄī”MAPĮYŠ¦Ę┤æ¬Ą─ė░ĒæŻ¼▒ŠīŹ“×║Y▀x│÷pH=9.5ū„×ķ┐╝▓ņļs┘|ī”Ę┤æ¬ą¦╣¹ė░ĒæīŹ“ץ─ūŅ╝čpHųĄ.
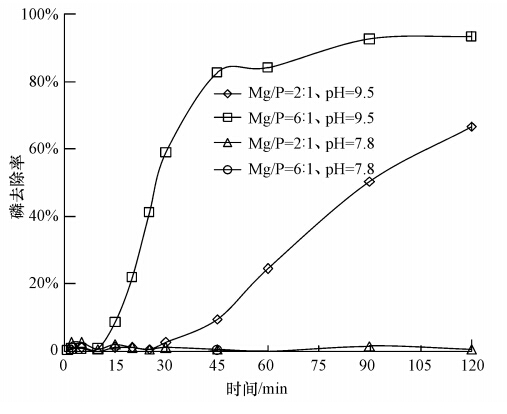
ĪĪĪĪłD 3 ▓╗═¼pHųĄĪó▓╗═¼n(Mg)/n(P)Śl╝■Ž┬┴ūØŌČ╚ļSĘ┤æ¬ĢrķgĄ─ūā╗»
ĪĪĪĪ3.2 ╠╝╦ßĖ∙ØŌČ╚ī”MAPĮYŠ¦Ę┤æ¬Ą─ė░Ēæ
ĪĪĪĪīŹ“×įOČ©CP=0.645 mmol Īż L-1Īó│§╩╝n(Mg)/n(P)Ęųäe×ķ2 : 1┼c6 : 1Ż¼ī”CO2-3ØŌČ╚×ķ2.5Īó5.0Īó10.0 mmol Īż L-1Ą──ŻöM╦«śėŻ¼į┌pH=9.5Śl╝■Ž┬▀MąąMAPĮYŠ¦Ę┤æ¬Ż¼Ę┤æ¬ĮY╩°║¾¾wŽĄP╚ź│²┬╩╝░n(Mg)/n(P)=6 : 1╩ŻėÓ┴ūØŌČ╚ęŖłD 4.Å─łDųą┐┤│÷Ż¼ļSų°CO2-3ØŌČ╚Ą─į÷╝ėŻ¼¤ošō║╬ĘNn(Mg)/n(P)¾wŽĄŻ¼Š∙│÷¼FP╚ź│²┬╩Ž┬ĮĄĄ─┌ģä▌Ż¼▀@┼cį¼∙iĄ╚(Ą─蹊┐ĮY╣¹ę╗ų┬Ż¼Ūę¾wŽĄųąCMgįĮąĪ▀@ĘNė░ĒæŠ═įĮ├„’@Ż¼ŪęŽÓ▒╚ė┌╝āMAPĮYŠ¦Ę┤æ¬Ż¼Ę┤æ¬│÷¼Fčė▀tŻ¼¾wŽĄ╝sį┌30 minū¾ėęķ_╩╝╝ė╦┘Ę┤æ¬.į┌n(Mg)/n(P)=2 : 1¾wŽĄųąŻ¼▓╗═¼CO2-3ØŌČ╚Śl╝■Ž┬Ż¼MAPĮYŠ¦Ę┤æ¬ī”P║═MgĄ─╚ź│²Ūķør╚ń▒Ē 1╦∙╩Š.Å─▒Ēųąėŗ╦ŃĮY╣¹┐╔ęį┐┤│÷Ż¼n(Mg)/n(P)Š∙┤¾ė┌1.0Ż¼╝┤ģó┼cĘ┤æ¬Ą─Mg2+▓ó▓╗╩Ū╚½▓┐┼cPO3-4ĮY║Ž╔·│╔MAP.═©▀^ī”FTIRĮY╣¹(łD 5)Ą─Ęų╬÷┐╔ų¬Ż¼į┌1431 cm-1╠ÄÖz£yĄĮCO2-3Ą─▌^ÅŖ╠žš„╬³╩šĘÕŻ¼šf├„ «a╬’ųą┤µį┌CO2-3ĮMĘųĄ─╬’┘|Ż¼ŪęĘÕĖ▀ļSų°CO2-3ØŌČ╚Ą─╔²Ė▀ėą┬į╬óĄ─į÷┤¾Ż¼╝┤įō╬’┘|║¼┴┐ėą╦∙į÷╝ėŻ¼Ą½PO3-4¹}ĮMĘųĘÕÅŖČ╚ūā╗»▓╗┤¾.ę└šš╚▄ę║ĮM│╔┼ąöÓįō╬’┘|×ķMgCO3│┴ĄĒ.ę“Č°CO2-3Ą─┤µį┌ĮĄĄ═┴╦Mg2+Ą─└¹ė├┬╩Ż¼Ą½▓╗ė░ĒæMAPĄ─╝āČ╚.
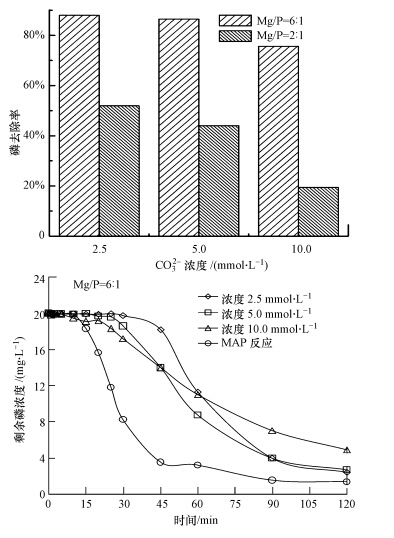
ĪĪĪĪłD 4 ▓╗═¼CO2-3ØŌČ╚ī”┴ū╚ź│²Ą─ė░Ēæ
ĪĪĪĪ▒Ē1 ▓╗═¼CO2-3ØŌČ╚Ž┬P║═MgĄ─╚ź│²Ūķør(n(Mg)/n(P)=6 : 1)
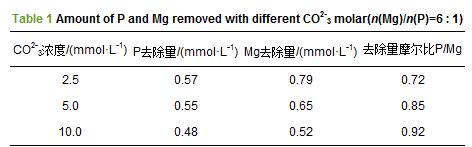
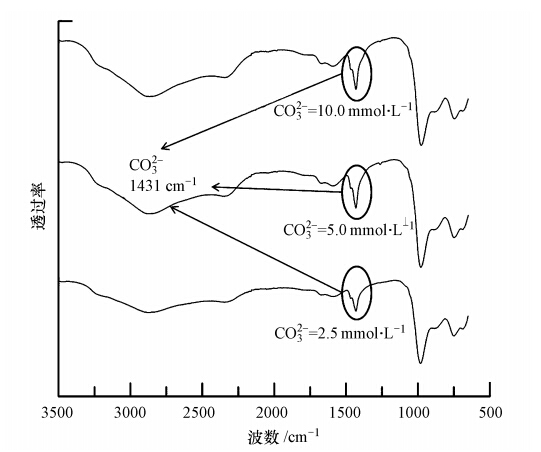
ĪĪĪĪłD 5 ▓╗═¼CO2-3ØŌČ╚│┴ĄĒ«a╬’Ą─FTIRĮY╣¹(n(Mg)/n(P)=6 : 1)
ĪĪĪĪįō¾wŽĄ╦∙Ą├│┴ĄĒ«a╬’Ą─SEMššŲ¼ĪóXRDłDūV┼c╝āMAPĮYŠ¦Ę┤欫a╬’Ą─ššŲ¼▀Mąąī”▒╚Ęų╬÷Ż¼ĮY╣¹╚ńłD 6╦∙╩Š.ė╔ė┌ļs┘|CO2-3ļxūėĄ─┤µį┌Ż¼│┴ĄĒŠ¦ą╬×ķą▒ĘĮą═╗“╣„ĀŅŻ¼┼cMAPĘ┤欫a╬’ŽÓ▒╚│▀┤ń┬į╬ó┤ų┤¾Ż¼Ūę«a╬’XRDłDūV┼cMAPś╦£╩ĘÕ╬Ū║ŽČ╚▌^Ė▀Ż¼╣╩CO2-3ļs┘|Ą─┤µį┌▓óø]ėąĖ─ūāMAPŠ¦¾wĄ─ą╬æB╝░╝āČ╚Ż¼ų╗╩Ū┼cPO3-4ĖéĀÄĘ┤æ¬Å─Č°ĮĄĄ═┴╦P╚ź│²┬╩.
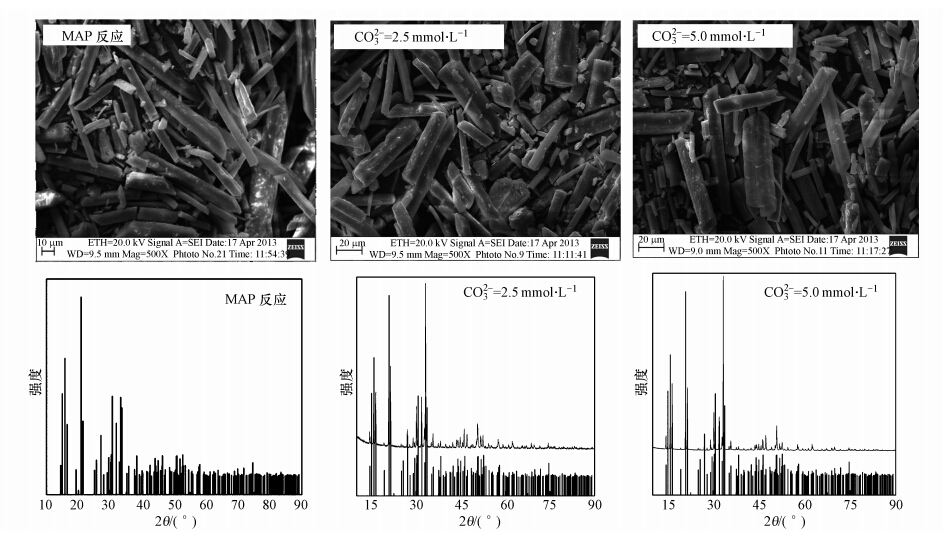
ĪĪĪĪłD 6 ▓╗═¼CO2-3ØŌČ╚│┴ĄĒ«a╬’SEMłD╝░XRDłDūV(Ī┴500)(n(Mg)/n(P)=6 : 1)
ĪĪĪĪ3.3 Ō}ļxūėØŌČ╚ī”MAPĮYŠ¦Ę┤æ¬Ą─ė░Ēæ
ĪĪĪĪįOČ©CP=0.645 mmol Īż L-1Īó│§╩╝n(Mg)/n(P)Ęųäe×ķ2 : 1┼c6 : 1Ż¼ī”CO2-3ØŌČ╚×ķ2.5Īó5.0Īó10.0 mmol Īż L-1 Ą──ŻöM╦«śėŻ¼į┌pH=9.5Śl╝■Ž┬▀MąąMAPĮYŠ¦Ę┤æ¬Ż¼Ę┤æ¬ĮY╩°║¾¾wŽĄP╚ź│²┬╩╝░n(Mg)/n(P)=6 : 1╩ŻėÓ┴ūØŌČ╚ęŖłD 7Ż¼┐╔ų¬PO3-4╦▓ķgģó╝ėĘ┤æ¬▓óį┌30 minū¾ėę▀_ĄĮŲĮ║Ō.į┌¤oCa2+╝░CO2-3Ą╚ļs┘|┤µį┌Ą─Śl╝■Ž┬Ż¼n(Mg)/n(P)×ķ2 : 1║═6 : 1Ą─╝āMAPĮYŠ¦Ę┤æ¬Ą─ūŅĮK┴ū╚ź│²┬╩Ęųäe×ķ74.55%║═95.43%Ż¼Ca2+Ą─┤µį┌Ę┤Č°╠ßĖ▀┴╦¾wŽĄP╚ź│²┬╩.Å─łD 7┐╔ęį┐┤│÷Ż¼į┌ėąCa2+┤µį┌ĢrPĄ─╚ź│²┬╩Š∙▒Ż│ųį┌95%ęį╔Ž.
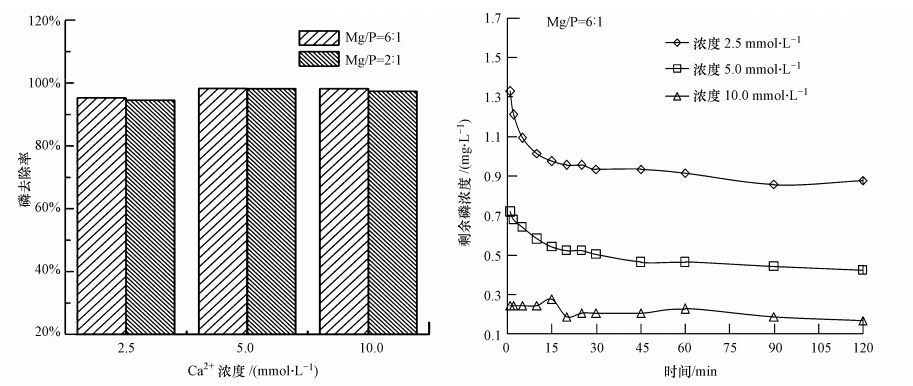
ĪĪĪĪłD 7 ▓╗═¼Ca2+ØŌČ╚ī”┴ū╚ź│²Ą─ė░Ēæ
ĪĪĪĪ═©▀^ī”│┴ĄĒ«a╬’Ą─SEMššŲ¼(łD 8)Ęų╬÷┐╔ų¬Ż¼│┴ĄĒ«a╬’▓óĘŪßśĀŅČ°╩ŪēKĀŅŻ¼│§▓Į┼ąöÓ«a╬’×ķ┴ū╦ßŌ}¹}.ī”«a╬’▀MąąXRDĘų╬÷(łD 8)Ż¼ŲõĘų╬÷ĮY╣¹ūCīŹ┴╦╔Ž╩÷┼ąöÓŻ¼łDūVųąø]ėąMAPŠ¦¾wĄ─ī”æ¬ĘÕŻ¼Č°╩Ū¤oČ©ą╬┴ū╦ßŌ}łDūV.HAPĄ─Ksp(4.7Ī┴10-55.9)▒╚MAPĄ─Ksp(10-12.6)ꬹĪ║▄ČÓŻ¼└Ēšō╔ŽHAP▒╚MAPĖ³╚▌ęū░l╔·│┴ĄĒĘ┤æ¬Ż¼Ūę¾wŽĄųąCa/Mg=0.65~2.58Ż¼ę“Č°Ca2+Ė³╚▌ęūōīš╝PO3-4Ę┤æ¬╬╗³c╔·│╔ HAPŻ¼ī”MAPĮYŠ¦Ę┤欫a╔·ęųųŲū„ė├.║┬ĢįĄžĄ╚ę▓ųĖ│÷Ca2+Ą─┤µį┌Ģ■ī¦ų┬«a╬’ųą╔·│╔Ė³ČÓĄ─║¼Ō}╗»║Ž╬’Ż¼Å─Č°ė░ĒæMAPĄ─╝āČ╚╝░╗ž╩š┬╩.Č°šµīŹĄ─╬█╦«ųą═©│ŻČ╝║¼ėąę╗Č©öĄ┴┐Ą─Ca2+Ż¼╦∙ęįīŹļHĘ┤æ¬▀^│╠ųąÄū║§▓╗┐╔─▄½@Ą├Ė▀╝āČ╚Ą─MAP.Le CorreĄ╚Ą─蹊┐═¼śė▒Ē├„Ż¼Ca2+Ą─┤µį┌Ģ■ī”MAPĄ─ą╬│╔įņ│╔ė░Ēæ.
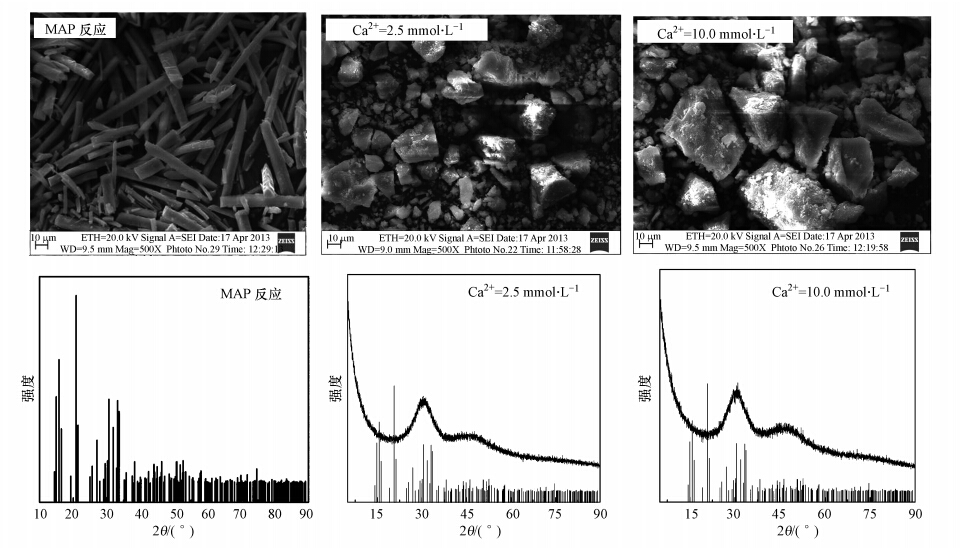
ĪĪĪĪłD 8 ▓╗═¼Ca2+ØŌČ╚│┴ĄĒ«a╬’SEMłD(Ī┴500)╝░XRDłDūV(n(Mg)/n(P)=6 : 1)
ĪĪĪĪ3.4 Ca2+ĪóCO2-3╣▓┤µī”MAPĮYŠ¦Ę┤æ¬Ą─ė░Ēæ
ĪĪĪĪCa2+║═CO2-3╩Ū╬█╦«ųą│ŻęŖĮMĘųŻ¼ā╔š▀═∙═∙╣▓═¼┤µį┌ė┌╦«¾wųą.īŹ“×įOČ©CP=0.645 mmol Īż L-1Īó│§╩╝n(Mg)/n(P)Ęųäe×ķ2 : 1┼c6 : 1Ż¼▓óįOČ©n(Ca): n(CO2-3)=1 : 1Ż¼ØŌČ╚Ęųäe×ķ2.5Īó5.0Īó10.0 mmol Īż L-1Ą──ŻöM╦«śėŻ¼į┌pH=9.5Śl╝■Ž┬▀MąąMAPĮYŠ¦Ę┤æ¬Ż¼Ę┤æ¬ĮY╩°║¾¾wŽĄP╚ź│²┬╩ęŖ▒Ē 2.Å─▒Ēųą┐╔ęį┐┤ │÷Ż¼įōįć“׌l╝■┼cCa2+å╬¬Ü┤µį┌ī”MAPĮYŠ¦Ę┤æ¬Ą─╚ź│²ą¦╣¹┤¾ų┬ŽÓ═¼Ż¼╚ź│²┬╩Š∙ŠS│ųį┌94%ęį╔Ž.ī”¾wŽĄn(Mg)/n(P)×ķ2 : 1Ą─│┴ĄĒ«a╬’▀MąąXRDĘų╬÷(łD 9)Ż¼ĮY╣¹▒Ē├„Ż║«ön(Mg): n(Ca): n(CO2-3)=1 : 2 : 2ĢrŻ¼«a╬’ų„ę¬ęį¤oČ©ą╬┴ū╦ßŌ}¹}×ķų„;«ön(Mg): n(Ca): n(CO2-3)Ī▌1:4:4ĢrŻ¼│²┴╦Öz£y│÷ūŅ├„’@Ą─CaCO3╠žš„ĘÕęį═ŌŻ¼«a╬’ųąķ_╩╝│÷¼FMAPĄ─╠žš„ĘÕ.
ĪĪĪĪ▒Ē2 Ca2+┼cCO2-3╣▓┤µī”┴ū╚ź│²Ą─ė░Ēæ
ĪĪĪĪė╔ė┌¾wŽĄCO32-ØŌČ╚▌^┤¾Ż¼ę“Č°┤µį┌Ą─╗»īWĘ┤æ¬▓╗āHāH┼cPO43-ėąĻPŻ¼CO2-3ę▓į┌ĖéĀÄĘ┤æ¬.¾wŽĄųąĄ─Ca2+ĪóMg2+ģó╝ėĄ─Ę┤æ¬╔·│╔CaCO3ĪóCa(PO4)3ĪóMgNH4PO4Ą╚.蹊┐▒Ē├„Ż¼CO2-3Ą─┤µį┌ī”HAPĘ┤æ¬┤µį┌ęųųŲū„ė├.Cao║═Harrisßśī”CO2-3┼cMg2+ī”HAPĘ┤æ¬Ą─ė░Ēæ▀Mąą┴╦ŽĄĮy蹊┐Ż¼įOėŗ┴╦Ė▀Ą═ā╔éĆ▓╗═¼Ą─pHųĄ¾wŽĄŻ¼Ųõųąę╗éĆpHųĄ×ķ9.2(systemó“).į┌systemó“pH=9.2ėąCO2-3┤µį┌Ą─Śl╝■Ž┬Ż¼═¼å╬╝āĄ─HAP│┴ĄĒĘ┤欎Ó▒╚Ż¼HAP│┴ĄĒĘ┤æ¬╦┘┬╩│ŻöĄĮĄĄ═┴╦╝s86%Ż¼┤╦ĮY╣¹šf├„CO2-3┤µį┌ĢręųųŲHAPĘ┤æ¬Ą─▀Mąą.Cao║═Harris(ī”│┴ĄĒ«a╬’▀Mąą┴╦XRD║═į¬╦žĘų╬÷Ż¼ĮY╣¹▒Ē├„│┴ĄĒųąn(Ca)/n(P)Å─1.47╔²Ė▀ų┴3.44Ż¼ŪęXRDę▓Öz£y│÷CaCO3Ą─ÅŖĘÕ.Č°CO2-3Ą─┤µį┌▓╗ė░ĒæMAPĄ─Š¦ą╬║═╝āČ╚Ż¼╝┤ī”MAPė░Ēæ▌^ąĪ.ę“Č°╝┤╩╣į┌Ė▀n(Ca)/n(Mg)Śl╝■Ž┬Ż¼HAP╚į¤oĘ©Ēś└¹╔·│╔Ż¼┤╦ĢrPO3-4ų„ę¬ęįMAPĄ─ą╬╩Į╚ź│²Ż¼Ą½Š¦¾wą╬æB╩▄ė░Ēæ▌^┤¾Ż¼ą╬ĀŅ▓╗ęÄät│╔ēKĀŅ(╚ńłD 9).Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.dongaorq.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
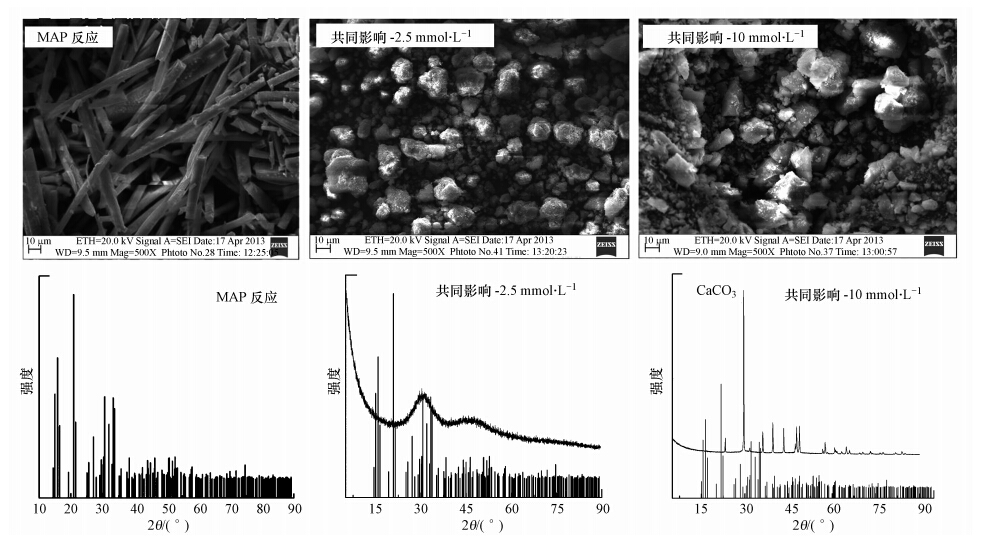
ĪĪĪĪłD 9 ▓╗═¼Ca2+╝░CO2-3ØŌČ╚│┴ĄĒ«a╬’SEMłD(Ī┴500)╝░XRDłDūV(n(Mg)/n(P)=6 : 1)
ĪĪĪĪ4 ĮYšō
ĪĪĪĪ1)į┌ę╗Č©ĘČć·ā╚Ż¼ļSų°pHųĄ╔²Ė▀Ż¼┴ūĄ─╚ź│²┬╩’@ų°╠ßĖ▀Ż¼į┌īŹ“׌l╝■Ž┬Ż¼MAPĮYŠ¦Ę┤æ¬Ą─ūŅ╝čpHųĄ×ķ9.5Ż¼Ą├ĄĮĄ─MAPŠ¦¾w│╩ßśĀŅŻ¼Š▀ėą┴╝║├Ą─│┴ĮĄąį─▄.
ĪĪĪĪ2)CO2-3Ą─┤µį┌Ģ■╩╣┴ū╚ź│²┬╩╝░Mg2+Ą─ėąą¦└¹ė├┬╩ĮĄĄ═Ż¼Ą½▓ó▓╗Ė─ūāMAPŠ¦¾wą╬æB║═╝āČ╚;Č°Ca2+┤µį┌ät┐╔ęį╠ßĖ▀P╚ź│²┬╩Ż¼Ą½ī”MAPĮYŠ¦Ę┤æ¬ęųųŲū„ė├’@ų°Ż¼«ö¾wŽĄųąn(Ca)/n(Mg)>0.65Ż¼«a╬’ų„ę¬ęį¤oČ©ą╬┴ū╦ßŌ}¹}×ķų„.
ĪĪĪĪ3)į┌Ca2+┼cCO2-3╣▓┤µĄ─¾wŽĄųąŻ¼Ca2+┐╔ėąą¦ĄžŽ¹│²CO2-3ī”│²┴ūą¦╣¹Ą─ė░Ēæ.«ön(Mg): n(Ca): n(CO2-3)=1 : 2 : 2ĢrŻ¼«a╬’ęį¤oČ©ą╬┴ū╦ßŌ}¹}×ķų„;«ön(Mg): n(Ca): n(CO2-3)Ī▌1 : 4 : 4ĢrŻ¼«a╬’ųąķ_╩╝│÷¼FMAPĄ─╠žš„ĘÕ.ę“Č°į┌CO2-3ØŌČ╚▌^┤¾Ą─¾wŽĄųąŻ¼Ca2+Ą─═╗│÷žĢ½I×ķĮĄĄ═¾wŽĄēAČ╚Ż¼┴ū╦ß¹}ätų„ę¬ęįMAPą╬╩Į│┴ĄĒ.


