╬ęć°╩Ū╦««aBų│śI┤¾ć°Ż¼Bų│╦«╗žė├┼c╬▓╦«┼┼Ę┼ęč│╔×ķąąśIųž³cĻPūóĄ─Łh▒Żå¢Ņ}ĪŻ│¶č§č§╗»Ę©┐╔ėąą¦£ń╗Ņė░ĒæBų│Ą─▓ĪįŁ╬ó╔·╬’Ż¼═¼Ģr┐╔ĮĄĄ═╦«ųą╣╠¾wæęĖĪ╬’║¼┴┐▓óč§╗»ĮĄĮŌ▓┐ĘųėąÖC╬’Ż¼╩ŪīŹļH╔·«aųąæ¬ė├ą¦╣¹┴╝║├Ą─╠Ä└ĒĘĮĘ©ĪŻ╚╗Č°į┌╠Ä└Ē▀^│╠ųąŻ¼│¶č§Ą─╩╣ė├┴┐ļyęįŠ½£╩š{┐žŻ¼▀^┴┐═Č╝ėĢ■ī¦ų┬╦«ųą│¶č§Üł┴¶Ż¼ī”╦«╔·╔·╬’«a╔·ČŠąįŻ¼ė░Ēæč└÷ę¶~Ą╚Bų│äė╬’╔·ķLŻ¼ę“┤╦ėą▒žę¬ī”╠Ä└Ē║¾Bų│╦«ųąÜł┴¶Ą─│¶č§▀Mąą╠Ä└ĒĪŻ
╦«ųąÜł┴¶│¶č§┐╔═©▀^┤▀╗»Ę©ĘųĮŌŻ¼─┐Ū░┼c│¶č§ŽÓĻPĄ─┤▀╗»ä®čąŠ┐ų„ę¬╝»ųąį┌┤▀╗»│¶č§ĮĄĮŌ╦«ųą╬█╚Š╬’ĘĮ├µŻ¼Č°ų▒Įė┤▀╗»ĘųĮŌ│¶č§Ą─蹊┐ätŽÓī”▌^╔┘Ż¼āHėą”┴-FeOOH╝░Č■č§╗»ŌŗĄ╚║åå╬Įī┘č§╗»╬’ū„×ķ┤▀╗»ä®ĪŻĮ³─ĻüĒŻ¼Įī┘č§╗»╬’┤▀╗»ä®▒Ē├µĮYśŗ╚▒Ž▌ū„×ķ┤▀╗»╗Ņąį³c╬╗Ą─蹊┐ųØu┼dŲŻ¼čąŠ┐¤ß³c░³└©č§┐š╬╗║═Š¦¾w▀ģŠē╚▒Ž▌Ą╚ĪŻŲõųąč§┐š╬╗ę“Š▀ėą┤▀╗»╗ŅąįĖ▀ĪóśŗĮ©ĘĮĘ©ČÓĪóĘĮ▒Ńš{┐žĄ╚╠ž³cŻ¼į┌│¶č§┤▀╗»▓─┴ŽįOėŗ▀^│╠ųą▒╗ÅVĘ║╠ß╝░Ż¼Ą½╬┤ęŖīóŲõæ¬ė├ė┌╦«ųą│¶č§ĘųĮŌĄ─ŽÓĻPł¾Ą└Ż¼ę“┤╦╠ĮŠ┐ęįč§┐š╬╗×ķų„ę¬╗Ņąį³c╬╗Ą─Įī┘č§╗»╬’į┌│¶č§ĘųĮŌųąĄ─┤▀╗»╗Ņąįū„ė├Š▀ėąųžę¬ęŌ┴xĪŻ
╣Pš▀ęį”┴-MnO2×ķģ󚚯¼═©▀^┴“╦ß╬g┐╠Ę©ųŲéõ┴╦Ė╗║¼č§┐š╬╗Ą─”┴-MnOŻ©2”┴-MnO2-OVŻ®Ż¼▓óė├ė┌│¶č§ĘųĮŌŻ¼Ųõ▒Ē¼F│÷┴╦Ė▀┤▀╗»│¶č§ĘųĮŌ╗Ņąį║═ĘĆČ©ąįŻ¼═¼Ģr═©▀^ŽÓĻP▒Ēš„ĘĮĘ©╠Įėæ┴╦č§┐š╬╗į┌│¶č§ĘųĮŌųąĄ─ū„ė├ĪŻ┤╦═ŌŻ¼▀Ćī”ė░Ēæ│¶č§ĘųĮŌĄ─Śl╝■ę“╦žŻ©£žČ╚ĪópHĪó┤▀╗»ä®═Č┴┐Īó│¶č§ØŌČ╚ĪóĻÄļxūėŻ®▀Mąą┴╦ŽĄĮy┐╝▓ņŻ¼ų╝į┌×ķ│¶č§č§╗»║¾╦«ųąÜł┴¶│¶č§ĘųĮŌå¢Ņ}╠ß╣®ĮŌøQĘĮ░ĖĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 īŹ“×įćä®
īŹ“×įćä®░³└©ĄÕ╦{ĪóÜõč§╗»ŌcĪó¹}╦ßĪóĖ▀┬╚╦ßĪó30%▀^č§╗»ÜõĪóŽ§╦ßÕiĪó┴“╦ߥ╚ĪŻ
1.2 ┤▀╗»ä®Ą─ųŲéõ
”┴-MnO2Ą─ųŲéõĘĮĘ©Ż║īó50mL║¼ėą0.6mol/LNaOH║═2mol/LH2O2Ą─╚▄ę║┼c50mL║¼ėą0.3mol/LMnŻ©NO3Ż®2Ą─╚▄ę║čĖ╦┘╗ņ║ŽŻ¼ė┌╩ę£žŽ┬öć░Ķ25min║¾Ą├ĄĮ║┌ūž╔½æęĖĪę║Ż¼ĻÉ╗»1hĪŻīó×V║¾│┴ĄĒ╦«Ž┤║¾Ęų╔óė┌2mol/LNaOH╚▄ę║ųąŻ¼į┘▐DęŲų┴╦«¤ßĘ┤æ¬Ė¬ųąŻ¼ė┌150ĪµŚl╝■Ž┬├▄ķ]╦«¤ß16hĪŻīó╦«¤ß╠Ä└Ē║¾Ą─æęĖĪę║▀Mąą▀^×VĪó╦«Ž┤ĪóĖ╔į’ĪŻīóĖ╔į’║¾Ą─║┌╔½╣╠¾wĘų╔óė┌0.1mol/LHCl╚▄ę║ųąŻ¼ė┌╩ę£žŽ┬╠Ä└Ē3dĪŻīó╠Ä└Ē║¾Ą─æęĖĪę║▀^×VĪó╦«Ž┤ĪóĖ╔į’Ż¼╝┤┐╔Ą├ĄĮ”┴-MnO2ĪŻ
”┴-MnO2-OVĄ─ųŲéõĘĮĘ©Ż║īó”┴-MnO2Ę█─®╝ė╚ļĄĮH2SO4ųąŻ¼ŲõųąH2SO4┼c”┴-MnO2Ą─╬’┘|Ą─┴┐ų«▒╚×ķ14.4Ż¼į┌±RĖŻĀtųąęį2Īµ/minĄ─╦┘┬╩╝ė¤ßų┴110Īµ▒║¤²2hĪŻīó╦∙Ą├║┌╔½╣╠¾wė├š¶s╦«Ž┤£ņ║¾Ę┼╚ļ60Īµ║µŽõųąĖ╔į’Ż¼ųŲĄ├”┴-MnO2-OVĪŻ
1.3 ┤▀╗»ä®Ą─▒Ēš„
└¹ė├X╔õŠĆč▄╔õāxŻ©XRDŻ®Ęų╬÷┤▀╗»ä®Ą─╬’ŽÓĮYśŗŻ╗└¹ė├Æ▀├ĶļŖūė’@╬óńRŻ©SEMŻ®ė^▓ņ┤▀╗»ä®Ą─ą╬├▓ĮYśŗŻ╗└¹ė├X╔õŠĆ╣ŌļŖūė─▄ūVāxŻ©XPSŻ®Ęų╬÷į¬╦žāræBŻ╗└¹ė├ĖĄ└’╚~ūāōQ╝t═Ō╣ŌūVāxŻ©FTIRŻ®Ęų╬÷┤▀╗»ä®▒Ē├µ╣┘─▄łFŻ╗└¹ė├ļŖūėĒś┤┼╣▓š±Ż©EPRŻ®£yČ©┤▀╗»ä®║¼ėąĄ─č§┐š╬╗ĪŻ
1.4 īŹ“×ĘĮĘ©
īóĖ▀╝āč§ÜŌ═©╚ļ│¶č§░l╔·Ų„║¾«a╔·│¶č§Ż¼į┘īó│¶č§ÜŌ¾w═©╚ļĄ═£ž│¼╝ā╦«ųąųŲĄ├Ė▀ØŌČ╚│¶č§╚▄ę║Ż¼▓óų├ė┌│¶č§ā”┤µ╚▌Ų„ųąĪŻ╚▌Ų„ųą║¼ėą1.5L╚źļxūė╦«Ż¼ė╔║Ń£ž▓█īó╚▌Ų„£žČ╚▒Ż│ųį┌277KĪŻ
▓╔ė├ņoæBīŹ“×ĘĮĘ©£yČ©│¶č§ĘųĮŌą¦─▄ĪŻīŹ“×į┌150mLÕFą╬Ų┐ųą▀MąąŻ¼īóę╗Č©┴┐Ą─╚źļxūė╦«║═┤▀╗»ä®ę└┤╬╝ė╚ļÕFą╬Ų┐ųąŻ¼═©▀^╠Ē╝ėĖ▀┬╚╦ß╗“Üõč§╗»ŌcüĒš{š¹╚▄ę║pHŻ¼Å─│¶č§ā”┤µ╚▌Ų„ųą╚Ī│÷ę╗Č©¾wĘeĄ─│¶č§╦«╝ė╚ļÕFą╬Ų┐ųąŻ¼╗ņ║ŽŠ∙ä“║¾åóäėīŹ“×ĪŻį┌įOČ©Ą─▓╔śėĢrķg³c▓╔╝»╦«śėŻ¼▓ó┴ó╝┤ė├0.22”╠mŠ█╦─Ę·ęꎮ▀^×VŲ„▀Mąą▀^×VĪŻ×Vę║┼cĄÕ╦{╚▄ę║╗ņ║Ž║¾╝ėų┴╩»ėó▓Ż┴¦▒╚╔½├¾ā╚Ż¼į┌610nm╠Äė├ūŽ═ŌĘų╣Ō╣ŌČ╚ėŗ£yČ©╬³╣ŌČ╚Ż¼▓óėŗ╦ŃŽÓæ¬Ą─│¶č§ØŌČ╚ĪŻÕFą╬Ų┐ųąĄ─┤▀╗»ä®į┌Ę┤æ¬║¾═©▀^│ķ×V╩š╝»Ż¼ė├╚źļxūė╦«Ž┤£ņ3┤╬║¾ė├ė┌ĘĆČ©ąį£yįćĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 ┤▀╗»ä®Ą─╬’╗»ąį┘|
2.1.1 ▒Ē├µą╬├▓
═©▀^SEMī””┴-MnO2║═”┴-MnO2-OV┤▀╗»▓─┴ŽĄ─ą╬├▓╠žš„▀Mąą▒Ēš„Ż¼░l¼F”┴-MnO2║═”┴-MnO2-OVŠ∙×ķČč»BĄ─╝{├ū░¶ĮYśŗŻ¼Įø▀^┴“╦ß╠Ä└ĒĄ─”┴-MnO2-OVŽÓ▌^ė┌”┴-MnO2’@╩Š│÷Ė³īÆĄ─ų▒ÅĮŻ¼Ūę╝{├ū░¶▒Ē├µūāĄ├┤ų▓┌Ż¼▀@▒Ē├„”┴-MnO2-OV┤▀╗»ä®▒Ē├µėą═¹▒®┬ČĖ³ČÓĄ─┤▀╗»╗Ņąį³c╬╗ĪŻ
2.1.2 Š¦¾wĮYśŗ
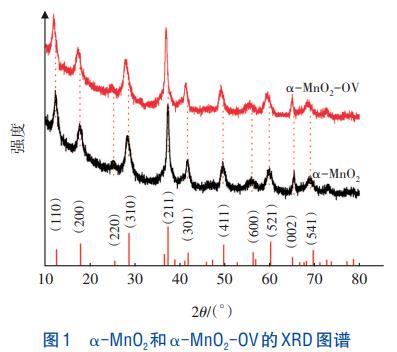
łD1×ķ”┴-MnO2║═”┴-MnO2-OVĄ─XRDłDūVĪŻ┐╔ų¬Ż¼śėŲĘį┌2”╚Ęųäe×ķ12.6ĪŃĪó17.8ĪŃĪó25.22ĪŃĪó28.7ĪŃĪó37.5ĪŃĪó41.88ĪŃĪó49.8ĪŃĪó55.96ĪŃĪó60.1ĪŃĪó65.1ĪŃĪó69.12ĪŃ╠Ä┤µį┌č▄╔õĘÕŻ¼Ęųäe┼c”┴-MnOŻ©2JCPDS44-0141Ż®ųąĄ─Ż©110Ż®ĪóŻ©200Ż®ĪóŻ©220Ż®ĪóŻ©310Ż®ĪóŻ©211Ż®ĪóŻ©301Ż®ĪóŻ©411Ż®ĪóŻ©600Ż®ĪóŻ©521Ż®ĪóŻ©002Ż®ĪóŻ©541Ż®Š¦├µę╗ę╗ī”æ¬Ż¼ŪęūVłDųą¤oļsĘÕ┤µį┌Ż¼▒Ē├„”┴-MnO2ųŲéõ│╔╣”ĪŻĮø▀^┴“╦ß╬g┐╠║¾Ż¼”┴-MnO2-OV┤▀╗»▓─┴ŽŻ©211Ż®Š¦├µĄ─╠žš„č▄╔õĘÕŽ“▌^Ą═ĮŪČ╚Ų½ęŲŻ¼═Ų£yįōŠ¦Ė±ĮYśŗĄ─ūā╗»╩Ūė╔č§┐š╬╗Ą─┤µį┌╦∙ī¦ų┬ĪŻ
2.1.3 ▒Ē├µį¬╦žĮM│╔
”┴-MnO2║═”┴-MnO2-OVĄ─XPS╣ŌūV╚ńłD2╦∙╩ŠĪŻė╔łD2Ż©aŻ®┐╔ų¬Ż¼ā╔ĘN┤▀╗»ä®ų„ę¬╩Ūė╔Mn║═Oā╔ĘNį¬╦žĮM│╔Ż¼Ūęį┌84Īó529║═642eV╠Ä▒Ē¼F│÷├„’@Ą─╠žš„ĘÕŻ¼Ęųäeī”æ¬ė┌Mn3sĪóO1s║═Mn2pĄ─ĮY║Ž─▄ĪŻ
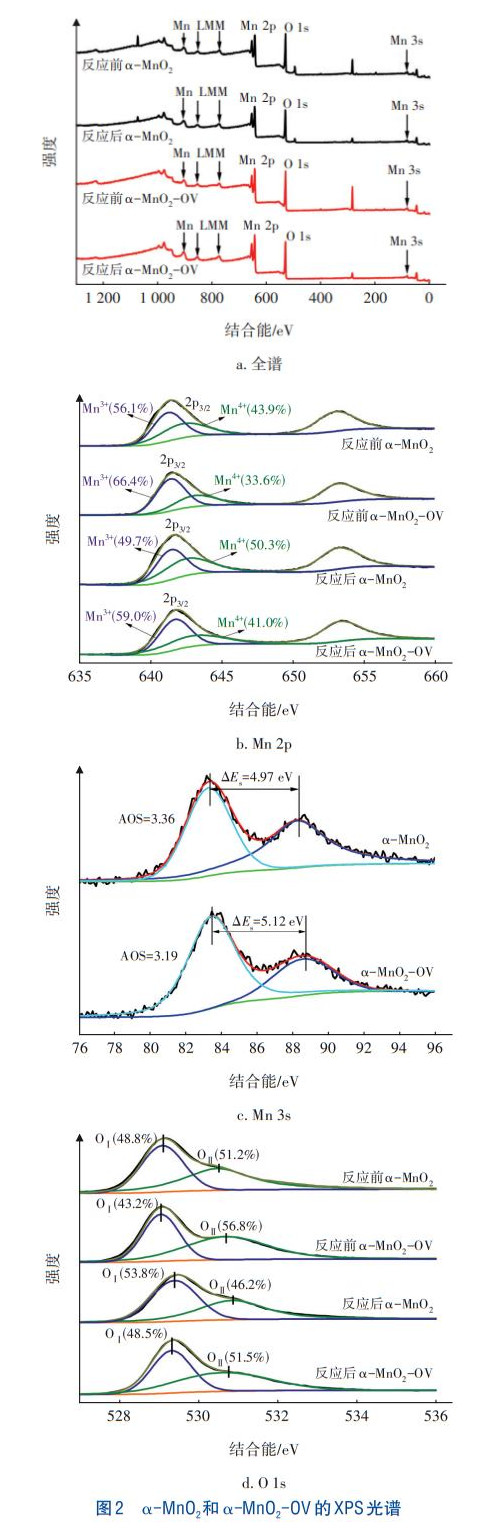
ė╔łD2Ż©bŻ®┐╔ų¬Ż¼▓╗ī”ĘQĄ─Mn2p3/2ĘÕį┌641.5║═642.7eV╠Ä┐╔ęįĮŌŠĒĘe│╔ā╔éĆĘÕŻ¼ĘųäeÜwī┘ė┌▒Ē├µĄ─Mn3+║═Mn4+ĪŻ”┴-MnO2-OVĄ─Mn3+/Mn4Ż©+╬’┘|Ą─┴┐ų«▒╚Ż¼1.98Ż®┤¾ė┌”┴-MnO2Ą─Ż©1.28Ż®ĪŻ«öMn3+║¼┴┐į÷╝ėĢrŻ¼ė╔ļŖųą║═įŁ└Ē┐╔ų¬Ż¼×ķ┴╦▒Ż│ųļŖ║╔ŲĮ║ŌŻ¼MnO2╩¦╚ź┴╦▓┐Ęų觯¼č§įŁūė╩▄¤ßÅ─Õič§╗»╬’Ą─ĮYśŗųą├ōļx│÷üĒŻ¼ī¦ų┬┤▀╗»ä®Ą─ĮYśŗ«a╔·┴╦Ė³ČÓĄ─č§┐š╬╗Ż¼Č°▀@ą®č§┐š╬╗ėą└¹ė┌│¶č§┼c┤▀╗»ä®Ą─ĮY║Ž▓ó░l╔·Ę┤æ¬ĪŻ
MnĄ─č§╗»æB┼c┤▀╗»ä®ųąĄ─č§┐š╬╗║¼┴┐├▄ŪąŽÓĻPŻ¼į┌MnO2ųąŻ¼č§╗»æBĄ─ĮĄĄ═┐╔─▄Ģ■ī¦ų┬č§┐š╬╗Ą─į÷ČÓĪŻĮY║ŽłD2Ż©cŻ®║═╬─½Iėŗ╦Ń┐╔ų¬Ż¼”┴-MnO2-OVųąMnĄ─ŲĮŠ∙č§╗»æBŻ©AOSŻ®×ķ3.19Ż¼ąĪė┌”┴-MnO2Ą─AOSŻ©3.36Ż®Ż¼▒Ē├„”┴-MnO2-OV┤▀╗»ä®▒Ē├µĄ─č§┐š╬╗║¼┴┐Ė▀ė┌”┴-MnO2Ż¼▀@┼cMn3+/Mn4+Ą─ĮY╣¹ŽÓę╗ų┬ĪŻ
═©▀^łD2Ż©dŻ®┐╔ęįģ^Ęųā╔ĘN▒Ē├µč§Ż¼529.1eVĄ─ĘÕųĄ┐╔Üwę“ė┌Š¦Ė±č§Ż©O󱯮Ż¼Č°▌^Ė▀Ą─ĮY║Ž─▄530.5~530.7eV┐╔Üwę“ė┌č§┐š╬╗Ż©Oó“Ż®ĪŻ”┴-MnO2Ą─Oó“║¼┴┐×ķ51.2%Ż¼”┴-MnO2-OVĄ─Oó“║¼┴┐×ķ56.8%Ż¼▀Mę╗▓ĮūC├„┴“╦ß╬g┐╠║¾”┴-MnO2▒Ē├µ║¼ėąĖ³žSĖ╗Ą─č§┐š╬╗ĪŻėąčąŠ┐▒Ē├„Ż¼č§┐š╬╗öĄ┴┐Ą─į÷ČÓėą└¹ė┌╠ßĖ▀┤▀╗»ä®Ą─│¶č§ĘųĮŌ╗ŅąįĪŻ
2.1.4 ▒Ē├µ╣┘─▄łF┼cč§┐š╬╗
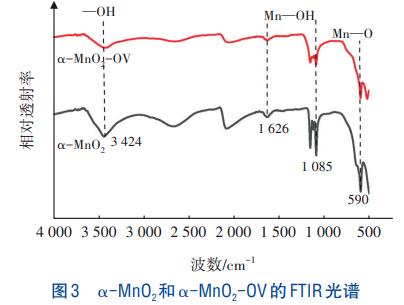
”┴-MnO2║═”┴-MnO2-OVĄ─FTIR╣ŌūV╚ńłD3╦∙╩ŠĪŻ┐╔ų¬Ż¼”┴-MnO2║═”┴-MnO2-OVį┌3424cm−1╠Äėąę╗éĆīÆČ°ÅŖĄ─╬³╩šĘÕŻ¼▀@╩Ūė╔ė┌Ī¬OHĄ─╔ņ┐sš±äėĪŻ1626║═1085cm−1╠Ä×ķMnĪ¬OHĄ─ÅØŪ·š±äėŻ¼▒Ē├„”┴-MnO2║═”┴-MnO2-OV╩Ū▒Ē├µ║¼ėą┤¾┴┐┴u╗∙Ą─Õič§╗»╬’ĪŻ590cm−1×ķMnĪ¬OĄ─ÅØŪ·š±äėŻ¼▒Ē├„┤µį┌MnO2ĘųūėŠ¦░¹ĪŻĮø▀^┴“╦ß╬g┐╠║¾Ż¼”┴-MnO2-OVį┌1085║═590cm−1╠ÄĄ─ĘÕÅŖČ╚├„’@ūāąĪŻ¼3424cm−1╠ÄĄ─ĘÕūāĄ├ŲĮ╗¼Ż¼▒Ē├„Ī¬OHĪóMnĪ¬OHĪóMnĪ¬O┐╔─▄ģó┼c┴╦┴“╦ß╬g┐╠▀^│╠ųąč§┐š╬╗Ą─śŗįņĪŻ
EPR╣ŌūVĘų╬÷▒Ē├„Ż¼ā╔ĘN┤▀╗»ä®▓─┴Žį┌┤┼ł÷ÅŖČ╚×ķ2.003Ī┴10-4T╠ÄČ╝Öz£y│÷┴╦EPRą┼╠¢Ż¼▀@╩Ūė╔č§┐š╬╗▓Č½@Ą─╬┤┼õ╬╗ļŖūėę²ŲĄ─ĪŻ┤▀╗»▓─┴Žč§┐š╬╗║¼┴┐┼cįō╠ÄEPRą┼╠¢ĘÕĄ─ÅŖČ╚├▄ŪąŽÓĻPŻ¼ę“┤╦ŽÓ▌^ė┌”┴-MnO2Ż¼”┴-MnO2-OVŠ▀ėąĖ³Ė▀║¼┴┐Ą─č§┐š╬╗Ż¼▀@ę╗ĮY╣¹┐╔┼cXPSĘų╬÷ĮY╣¹ŽÓ╗źšōūCĪŻ
2.2 ┤▀╗»ä®╗Ņąįįuār
2.2.1 ▓╗═¼┤▀╗»ä®ĘųĮŌ│¶č§Ą─ą¦─▄
į┌pH×ķ7Īó£žČ╚×ķ4ĪµĪó┤▀╗»ä®═Č┴┐×ķ0.05g/LĪó│¶č§ØŌČ╚×ķ3mg/LĄ─Śl╝■Ž┬Ż¼▓╗═¼┤▀╗»ä®ī”│¶č§Ą─ĘųĮŌą¦╣¹╚ńłD4╦∙╩ŠĪŻ
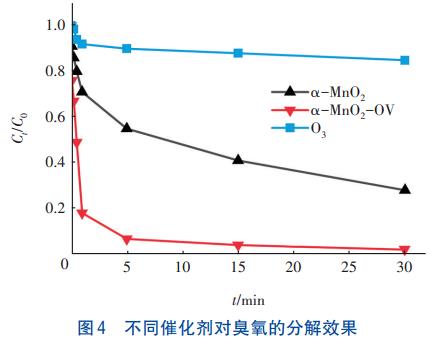
ė╔łD4┐╔ęį┐┤│÷Ż¼Ę┤æ¬30minęį║¾”┴-MnO2║═”┴-MnO2-OVī”│¶č§Ą─ĘųĮŌ┬╩Ęųäe×ķ71.9%║═98.0%Ż¼Č°å╬ę╗│¶č§¾wŽĄĄ─│¶č§ĘųĮŌ┬╩āH×ķ15.1%ĪŻ═©▀^öMę╗╝ēäė┴”īWĘĮ│╠öM║Ž│¶č§ĘųĮŌŪ·ŠĆ░l¼FŻ¼│¶č§Ą─ĘųĮŌį┌ėą¤o┤▀╗»ä®Ą─ŪķørŽ┬Č╝▌^║├Ąžū±čŁę╗╝ēäė┴”īWŻ¼Ųõųą”┴-MnO2-OVĄ─öMę╗╝ēäė┴”īWĮY╣¹▒Ē¼F×ķā╔Č╬╩ĮŻ¼īó┤▀╗»ä®ĘNŅÉ░┤öMę╗╝ēäė┴”īWĘ┤æ¬╦┘┬╩│ŻöĄ▀Mąą┼┼ą“Ż║”┴-MnO2-OVŻ©1.6323min−1Ż®>”┴-MnOŻ©20.0391min−1Ż®>¤o┤▀╗»ä®Ż©0.0047min−1Ż®Ż¼╝┤”┴-MnO2-OV¾wŽĄĄ─│¶č§ĘųĮŌ╦┘┬╩Ęųäe▒╚”┴-MnO2¾wŽĄ║═ų▒Įė│¶č§¾wŽĄ╠ßĖ▀┴╦42║═347▒ČĪŻė╔┤╦┐╔ų¬Ż¼”┴-MnO2-OVĘųĮŌ│¶č§Ą─╦┘┬╩▀hĖ▀ė┌”┴-MnO2┤▀╗»│¶č§¾wŽĄ║═å╬ę╗│¶č§¾wŽĄŻ¼šf├„”┴-MnO2-OVŠ▀éõĖ▀ą¦┤▀╗»│¶č§ĘųĮŌĄ──▄┴”ĪŻ
2.2.2 ┤▀╗»ä®═Č┴┐ī”│¶č§ĘųĮŌĄ─ė░Ēæ
×ķ┐╝▓ņ┤▀╗»ä®═Č┴┐ī”│¶č§ĘųĮŌĄ─ė░ĒæŻ¼į┌£žČ╚×ķ4ĪµĪópH×ķ7Īó│¶č§ØŌČ╚×ķ3mg/LĄ─Śl╝■Ž┬Ż¼┐╝▓ņ┤▀╗»ä®═Č┴┐ī”│¶č§ĘųĮŌĄ─ė░ĒæŻ¼ĮY╣¹╚ńłD5╦∙╩ŠĪŻ┐╔ų¬Ż¼Ę┤æ¬30min║¾Ż¼╬┤═Č╚ļ┤▀╗»ä®ĮMĄ─│¶č§ĘųĮŌ┬╩×ķ15.1%Ż¼Č°╝ė╚ļ0.01g/LĄ─”┴-MnO2╗“”┴-MnO2-OV┤▀╗»ä®║¾Ż¼│¶č§ĘųĮŌ┬╩╝┤┐╔╠ßĖ▀ų┴59.1%║═90.0%ĪŻ▀Mę╗▓Įį÷╝ė┤▀╗»ä®═Č┴┐Ż¼│¶č§ĘųĮŌ┬╩ųØu╔²Ė▀Ż¼Ą½ą¦╣¹ėąŽ▐ĪŻ┴Ē═ŌŻ¼ųĄĄ├ūóęŌĄ─╩ŪŻ¼”┴-MnO2-OVį┌0.05g/L═Č┴┐Ž┬Ą─│¶č§ĘųĮŌ┬╩ęč▀_98.0%Ż¼└^└mį÷╝ė┤▀╗»ä®═Č┴┐ī”│¶č§ĘųĮŌ┬╩ø]ėą’@ų°╠ßĖ▀ą¦╣¹ĪŻŠC║Ž┐╝æ]┤▀╗»ą¦╣¹║═ĮøØ·│╔▒ŠŻ¼┤_Č©┤▀╗»ä®Ą─ūŅ╝č═Č┴┐×ķ0.05g/LĪŻ
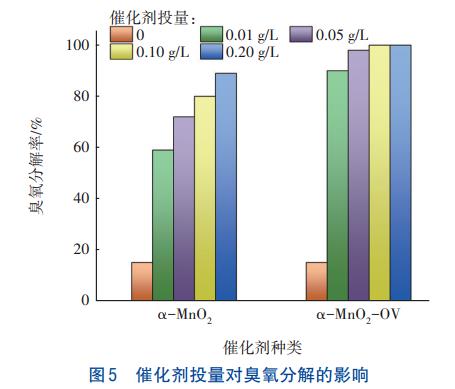
2.2.3 £žČ╚ī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░Ēæ
ę╗░ŃČ°čįŻ¼£žČ╚Ą─╔²Ė▀ėą└¹ė┌┤▀╗»Ę┤æ¬Ą─▀MąąĪŻį┌pH×ķ7Īó│¶č§ØŌČ╚×ķ3mg/LĪó┤▀╗»ä®═Č┴┐×ķ0.05g/LĄ─Śl╝■Ž┬Ż¼┐╝▓ņ£žČ╚ī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░ĒæŻ¼ĮY╣¹╚ńłD6╦∙╩ŠĪŻ
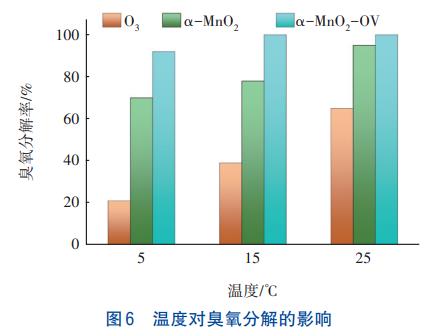
ė╔łD6┐╔ęį┐┤│÷Ż¼į┌Ę┤æ¬30minā╚Ż¼”┴-MnO2║═”┴-MnO2-OVī”│¶č§Ą─ĘųĮŌ┬╩ļSų°£žČ╚Ą─╔²Ė▀Č°į÷┤¾ĪŻĄ½╩ŪŻ¼£žČ╚ī”┤▀╗»ä®”┴-MnO2-OVĘųĮŌ│¶č§Ą─ė░Ēæ▓ó▓╗’@ų°Ż¼į┌5Īó15Īó25ĪµŽ┬ī”│¶č§Ą─ĘųĮŌ┬╩Ęųäe×ķ92.1%Īó100%║═100%Ż¼Ūę▓╗═¼£žČ╚Ž┬│¶č§Ą─ĘųĮŌČ╝▌^×ķčĖ╦┘Ż¼▀@šf├„”┴-MnO2-OV┤▀╗»│¶č§ĘųĮŌ╩▄£žČ╚Ą─ė░Ēæ▌^ąĪĪŻ
2.2.4 pHī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░Ēæ
į┌£žČ╚×ķ4ĪµĪó┤▀╗»ä®═Č┴┐×ķ0.05g/LĪó│¶č§ØŌČ╚×ķ3mg/LĄ─Śl╝■Ž┬Ż¼┐╝▓ņpHī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░ĒæŻ¼ĮY╣¹╚ńłD7╦∙╩ŠĪŻ
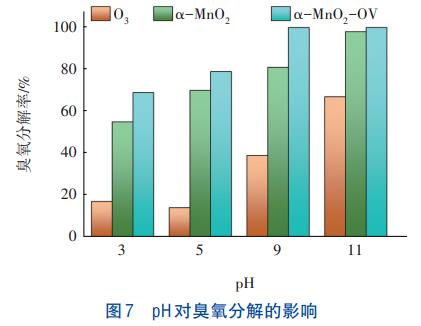
Å─łD7┐╔ęį┐┤│÷Ż¼Ę┤æ¬30minęį║¾Ż¼┼cųąąįŁhŠ│ŽÓ▒╚Ż¼╦ßąįŚl╝■Ž┬ī”│¶č§Ą─ĘųĮŌŲĄĮęųųŲū„ė├Ż¼ēAąįŁhŠ│ät┐╔ęį┤┘▀M│¶č§Ą─ĘųĮŌĪŻį┌pH×ķ3Ą─Śl╝■Ž┬Ż¼”┴-MnO2Īó”┴-MnO2-OVĪóå╬ę╗│¶č§¾wŽĄī”│¶č§Ą─ĘųĮŌ┬╩Ęųäe×ķ55.0%Īó69.0%║═17.1%ĪŻ┤╦Ģr┤▀╗»ä®▓óø]ėą▒Ē¼F│÷▌^ÅŖĄ─┤▀╗»╗ŅąįŻ¼▀@┐╔─▄╩Ūė╔ė┌”┴-MnO2║═”┴-MnO2-OVį┌╦ßąįŚl╝■Ž┬▒Ē├µ▒╗┘|ūė╗»│╠Č╚▌^ÅŖŻ¼│¶č§ĘųūėėHļŖ╠žąį╩╣Ųõ▓╗╚▌ęū▒╗╬³ĖĮĄĮ┤▀╗»ä®Ą─▒Ē├µŻ¼ę“Č°ęųųŲ”┴-MnO2Īó”┴-MnO2-OVģó┼c┤▀╗»Ę┤æ¬ĪŻ╚╗Č°Ż¼īŹ“×▀^│╠ųąŻ¼į┌pH×ķ9Ą─Śl╝■Ž┬Ż¼”┴-MnO2Īó”┴-MnO2-OVĪóå╬ę╗│¶č§¾wŽĄī”│¶č§Ą─ĘųĮŌ┬╩Ęųäe×ķ81.2%Īó100%║═39.0%ĪŻ▀@╩Ūę“×ķ╚▄ę║│╩ēAąįĢrŻ¼OHŻŁĢ■┼c│¶č§ĮY║Ž▓ó┤┘╩╣ŲõĘųĮŌŻ¼ę“Č°ēAąįŚl╝■Ž┬Ą─│¶č§ĘųĮŌ╦┘Č╚ŽÓī”ė┌ųąąį║═╦ßąįŚl╝■Ė³┐ņĪŻ
2.2.5│¶č§ØŌČ╚ī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░Ēæ
į┌┤▀╗»ä®═Č┴┐×ķ0.05g/LĪó£žČ╚×ķ4ĪµĪópH×ķ7Ą─Śl╝■Ž┬Ż¼┐╝▓ņ│¶č§ØŌČ╚ī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░ĒæŻ¼ĮY╣¹╚ńłD8╦∙╩ŠĪŻ┐╔ęį┐┤│÷Ż¼į┌5mg/LĄ─│¶č§ØŌČ╚Ž┬Ż¼═Č╚ļ”┴-MnO2-OVĄ─¾wŽĄĘ┤æ¬30min║¾ī”│¶č§Ą─ĘųĮŌ┴┐Ė▀▀_4.75mg/LĪŻ┐╔ęŖŻ¼╝┤▒Ńį┌Ė▀ØŌČ╚│¶č§Śl╝■Ž┬Ż¼”┴-MnO2-OVę└╚╗▒Ē¼F│÷┴╦ā׫ɥ─┤▀╗»ąį─▄Ż¼šf├„”┴-MnO2-OV┐╔ęįė├ė┌ĘųĮŌ╦«ųąĖ▀ØŌČ╚Ą─│¶č§ĪŻ
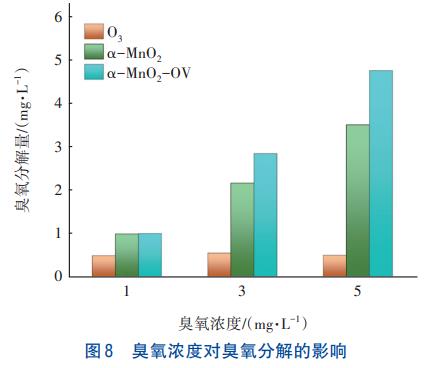
2.2.6 ╦«ųą│ŻęŖĻÄļxūėī”┤▀╗»ä®ĘųĮŌ│¶č§Ą─ė░Ēæ
Bų│ÅU╦«ųą═©│Ż║¼ėąŽ§╦ß¹}Īó╠╝╦ßÜõ¹}Īó┬╚¹}Ą╚¤oÖCĻÄļxūėŻ¼┐╔─▄Ģ■ī”│¶č§Ą─ĘųĮŌ«a╔·ė░ĒæĪŻ×ķ┤╦Ż¼▀Mę╗▓Į┐╝▓ņ┴╦Cl−ĪóNO3−ĪóHCO3−╚²ĘN╦«ųą│ŻęŖ¤oÖCĻÄļxūėī”│¶č§ĘųĮŌ┬╩Ą─ė░ĒæĪŻ«öpH×ķ7Īó£žČ╚×ķ4ĪµĪó│¶č§ØŌČ╚×ķ3mg/LĪó┤▀╗»ä®═Č┴┐×ķ0.05g/LĪóĻÄļxūėØŌČ╚×ķ10”╠mol/LĢrŻ¼3ĘN¤oÖCĻÄļxūėĄ─ę²╚ļŠ∙ī””┴-MnO2Īó”┴-MnO2-OV┤▀╗»│¶č§ĘųĮŌ«a╔·┴╦┤┘▀Mū„ė├Ż¼Ųõ┤┘▀Mą¦╣¹Ą─┼┼ą“×ķŻ║HCO3−>NO3−>Cl−ĪŻ«öĻÄļxūėØŌČ╚▀Mę╗▓Į╠ßĖ▀ų┴50”╠mol/LĢrŻ¼ė░Ēæą¦╣¹║═┌ģä▌┐é¾w▒Ż│ų▓╗ūāŻ¼šf├„┤▀╗»ä®┤▀╗»│¶č§ĘųĮŌĄ─ą¦╣¹ļSĻÄļxūėØŌČ╚ūā╗»Ą─│╠Č╚▓ó▓╗’@ų°Ż¼▀@ęŌ╬Čų°į┌īŹļH╦«¾wųą”┴-MnO2Īó”┴-MnO2-OV┤▀╗»ä®Š▀ėą▌^×ķĘĆČ©Ą─┤▀╗»ĘųĮŌ│¶č§ą¦─▄ĪŻ
2.3 │¶č§ĘųĮŌÖC└Ē
ęčėą┤¾┴┐蹊┐▒Ē├„Ż¼č§┐š╬╗╩Ū│¶č§ĘųĮŌĄ─Ę┤欳c╬╗Ż¼Å─łD2Ż©dŻ®┐╔ų¬Ż¼”┴-MnO2┤▀╗»ä®Ę┤æ¬Ū░║¾Ą─Oó“š╝▒╚Ęųäe×ķ51.2%║═46.2%Ż¼”┴-MnO2-OV┤▀╗»ä®Ę┤æ¬Ū░║¾Ą─Oó“š╝▒╚Ęųäe×ķ56.8%║═51.5%ĪŻŪę”┴-MnO2║═”┴-MnO2-OVĄ─│¶č§ĘųĮŌ╦┘┬╩│ŻöĄ┼cOó“║¼┴┐Ż©č§┐š╬╗Ż®ų«ķg│╩š²ŽÓĻPŻ¼╝┤č§┐š╬╗Ą─į÷ČÓĢ■ī¦ų┬Ųõ┤▀╗»╗Ņąį╔²Ė▀ĪŻĮY║ŽXPS║═EPRĄ─ĮY╣¹░l¼FŻ¼│¶č§Ą─ĘųĮŌÖCųŲū±čŁ┤▀╗»ä®╔Žč§┐š╬╗Ą─ģó┼c║═į┘裣hĪŻ«öę╗éĆO3Ęųūė▒╗╬³ĖĮį┌č§┐š╬╗Ż©VoŻ®╔ŽĢrŻ¼ę╗éĆO2Ęųūėīó▒╗ßīĘ┼│÷üĒŻ¼ę“┤╦į┌č§┐š╬╗╔Ž┴¶Ž┬ę╗éĆ╗Ņąįč§įŁūėŻ¼ęŖ╩ĮŻ©1Ż®ĪŻļS║¾Ż¼┴Ēę╗éĆO3ĘųūėĢ■┼c╗Ņąįč§įŁūė░l╔·Ę┤æ¬Ż¼ßīĘ┼│÷┴Ēę╗éĆO2ĘųūėŻ¼Å─Č°ą╬│╔▀^č§╗»╬’Ż©O22−Ż®Ż¼ęŖ╩ĮŻ©2Ż®ĪŻ▀^č§╗»╬’▀Mę╗▓ĮĘųĮŌ×ķO2Ż¼Å─Č°╗ųÅ═┴╦č§┐š╬╗Ż¼ęŖ╩ĮŻ©3Ż®Ż¼▀@ą®č§┐š╬╗ėų┐╔ęįģó┼cŽ┬ę╗éĆ裣hĘųĮŌ│¶č§ĪŻ
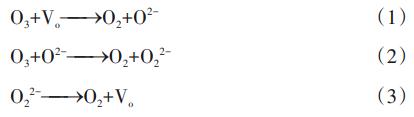
2.4 ┤▀╗»ä®Ą─ĘĆČ©ąį║═┐╔ųžÅ═╩╣ė├ąį
į┌ŽÓ═¼Ą─Śl╝■Ž┬▀Mąą4┤╬裣h╗ž╩šīŹ“ׯ¼ęįĘų╬÷”┴-MnO2║═”┴-MnO2-OVĄ─┐╔ųžÅ═╩╣ė├ąįĪŻ╩ū┤╬īŹ“×ĢrŽ╚Ž“Ę┤款wŽĄųą═Č╝ė0.05gą┬§r┤▀╗»ä®Ż¼Ę┤æ¬ĮY╩°║¾▀Mąą│ķ×V╩š╝»╩ŻėÓ┤▀╗»ä®Ż¼ė├╚źļxūė╦«ČÓ┤╬Ž┤£ņ║¾Ż¼ų├ė┌60Īµ║µŽõųą║µĖ╔ĘQ┘|┴┐Ż¼▓╗ūŃ0.05gĄ─┘|┴┐ė╔ą┬§r┤▀╗»ä®ča²R║¾į┘ķ_š╣Ž┬ę╗┤╬裣hīŹ“×ĪŻĮø▀^4┤╬裣h║¾Ż¼”┴-MnO2ī”│¶č§Ą─ĘųĮŌ┬╩ė╔71.9%ĮĄų┴63.0%Ż¼”┴-MnO2-OVät▒Ż│ųį┌95.1%~98.0%ų«ķgĪŻ”┴-MnO2▒Ē¼F│÷▌p╬ó╩¦╗ŅŻ¼▀@╩Ūė╔╗Ņąįųąą─║═║¼ėąÖC╬’▒Ē├µĄ─▓╗┐╔─µūā╗»╦∙ų┬ĪŻī”▒╚üĒ┐┤Ż¼”┴-MnO2-OV¾wŽĄĄ─│¶č§ĘųĮŌ┬╩į┌裣hŪ░║¾╗∙▒Š▒Ż│ų▓╗ūāŻ¼▒Ē├„”┴-MnO2-OV┤▀╗»ä®Š▀ėą┴╝║├Ą─┐╔ųžÅ═╩╣ė├ąįĪŻ
ī”ųžÅ═╩╣ė├4┤╬║¾Ą─”┴-MnO2║═”┴-MnO2-OV▀MąąXRD║═XPS▒Ēš„Ż¼ęį╠ĮŠ┐┤▀╗»ä®▒Ē├µĮYśŗĄ─ĘĆČ©ąįĪŻĮY╣¹▒Ē├„Ż¼Ę┤æ¬Ū░║¾”┴-MnO2║═”┴-MnO2-OVĄ─XRDūVłDųą│╩¼FĄ─ĘÕ╬╗ų├║═ĘÕą═Š∙╬┤░l╔·├„’@ūā╗»Ż¼ę▓╬┤╔·│╔ą┬Ą─Š¦├µŻ¼▀@ūC├„į┌┤▀╗»│¶č§ĘųĮŌĄ─▀^│╠ųąŻ¼ā╔ĘN┤▀╗»ä®Ą─ĮYśŗŠ∙Š▀ėąā׫ɥ─ĘĆČ©ąįĪŻĘ┤æ¬Ū░║¾”┴-MnO2║═”┴-MnO2-OVĄ─XPSłDūV▒Ē├„Ż¼Ę┤æ¬║¾”┴-MnO2║═”┴-MnO2-OVĄ─ĘÕ╬╗ų├║═ĘÕųĄŠ∙┼cĘ┤æ¬Ū░╗∙▒ŠŽÓ═¼Ż¼į¬╦žĮM│╔║═āræB╗∙▒Š▓╗ūāĪŻŠC╔Ž╦∙╩÷Ż¼”┴-MnO2║═”┴-MnO2-OVį┌┤▀╗»│¶č§ĘųĮŌ¾wŽĄųąŠ▀ėą▒Ē├µĮYśŗ║═Š¦¾wĮYśŗĄ─ļpųžĘĆČ©ąįĪŻ
3ĪóĮYšō
ó┘═©▀^ØŌ┴“╦ß╬g┐╠Ę©ųŲéõ┴╦Ė╗║¼č§┐š╬╗Ą─”┴-MnO2╝{├ū▓─┴ŽŻ©”┴-MnO2-OVŻ®Ż¼īó”┴-MnO2║═”┴-MnO2-OVė├ė┌┤▀╗»│¶č§ĘųĮŌŻ¼ĮY╣¹▒Ē├„”┴-MnO2║═”┴-MnO2-OVŠ∙Š▀ėąā׫ɥ─┤▀╗»│¶č§ĘųĮŌą¦╣¹Ż¼Ųõųą”┴-MnO2-OV▒╚”┴-MnO2Š▀ėąĖ³║├Ą─┤▀╗»ąį─▄Ż¼▀@╩Ūę“×ķ”┴-MnO2-OVĄ─ĮYśŗųą«a╔·┴╦Ė³ČÓĄ─č§┐š╬╗Ż¼┐╔╠ß╣®Ė³ČÓĘ┤欳c╬╗ĪŻā╔ĘN┤▀╗»ä®Ą─┤▀╗»ąį─▄Š∙ļS┤▀╗»ä®═Č┴┐ĪópHĪóĘ┤欣žČ╚Ą─╔²Ė▀Č°╔Ž╔²ĪŻ╦«ųą¤oÖCĻÄļxūėī”│¶č§ĘųĮŌŲ┤┘▀Mū„ė├Ż¼┤┘▀Mą¦╣¹┼┼ą“×ķŻ║HCO3−>NO3−>Cl−ĪŻ
ó┌”┴-MnO2-OV▒Ē¼F│÷┴╝║├Ą─│ųŠ├┤▀╗»╗ŅąįŻ¼▀Mąą4┤╬ųžÅ═ąįīŹ“×║¾Ż¼Ųõī”│¶č§Ą─ĘųĮŌ┬╩╗∙▒Š▒Ż│ų▓╗ūāŻ¼Ūę┤▀╗»ä®▒Ē├µĮYśŗ║═Š¦¾wĮYśŗį┌Ę┤æ¬▀^│╠ųąŠ∙▒Ż│ųĘĆČ©ĪŻŻ©üĒį┤Ż║šŃĮŁ╣żśI┤¾īWŁhŠ│īWį║šŃĮŁ╩Ī╣żśI╬█╚Š╬ó╔·╬’┐žųŲ╝╝ągųž³cīŹ“×╩ęŻ¼╣■Ā¢×I╣żśI┤¾īWŁhŠ│īWį║│Ū╩ą╦«┘Yį┤┼c╦«ŁhŠ│ć°╝ęųž³cīŹ“×╩꯮



