╬ó╔·╬’╚╝┴ŽļŖ│žŻ©MicrobialfuelcellŻ¼MFCŻ®╩Ūęį╬ó╔·╬’×ķ┤▀╗»ä®Ż¼īóėąÖC╬’ųąĄ─╗»īW─▄▐D╗»×ķļŖ─▄Ą─╔·╬’ļŖ╗»īW╗ņ║ŽŽĄĮyŻ¼Š▀ėąįŁ┴ŽüĒį┤ÅVĪóŪÕØŹŁh▒ŻĄ╚ā׳cĪŻį┌MFCŽĄĮy═Ļš¹Ą─╔·╬’ļŖ╗»īW▀^│╠ųąŻ¼ėąÖCĄū╬’Ż©ļŖūė╣®¾wŻ®į┌╬ó╔·╬’┤·ųx▀^│╠ųąč§╗»ĮĄĮŌŻ¼«a╔·ļŖūė║═┘|ūėŻ¼ļŖūė╩ūŽ╚Įø║¶╬³µ£é„▀fĄĮ╝Ü░¹─żŻ¼į┘ė╔░¹═ŌļŖūė▐DęŲÖCųŲ▐DęŲĄĮĻ¢śOŻ¼ūŅĮK═©▀^═ŌļŖ┬Ęé„▀fĄĮĻÄśOŻ¼┘|ūė═©▀^Į╗ōQ─żé„▀fĄĮĻÄśO╩ęŻ¼ļŖūėĪó┘|ūė┼cļŖūė╩▄¾wŻ©O2ĪóĶFŪĶ╗»ŌøĄ╚Ż®░l╔·▀ĆįŁĘ┤æ¬Ż¼ą╬│╔═Ļš¹Ą─╗ž┬ĘĪŻ─┐Ū░Ż¼MFCęč▒╗æ¬ė├ė┌ÅU╦«╠Ä└ĒĪóŁhŠ│ą▐Å═Īó╔·╬’é„ĖąŲ„Ą╚ŅIė“ĪŻ
ųŲ╦ÄÅU╦«Š▀ėą│╔ĘųÅ═ļsĪóėąÖC╬’║¼┴┐Ė▀Īó┐╔╔·╗»ąį▓ŅĄ╚╠ž³cŻ¼ī┘ė┌ļy╠Ä└ĒĄ─╣żśIÅU╦«Ż¼╗»īWĪó╬’└ĒĄ╚é„Įy╠Ä└ĒĘĮĘ©ļyęįĒśæ¬«öĮ±ŠG╔½ĪóĄ═╠╝Ą─░lš╣┌ģä▌ĪŻ└¹ė├╔·╬’Ę©╠Ä└ĒųŲ╦ÄÅU╦«Š▀ėąĮøØ·Ė▀ą¦Īó▓╗«a╔·Č■┤╬╬█╚ŠĄ─ā׳cĪŻHongyiZHUĄ╚śŗĮ©ļp╩ęMFC═¼▓Į╠Ä└Ē║¼Č„ųZ╔│ąŪĪóCu║═ZnĄ─║Ž│╔ÅU╦«Ż¼įōMFCĄ─ūŅ┤¾╣”┬╩├▄Č╚×ķŻ©244.2Ī└20.3Ż®mW/m2Ż¼Č„ųZ╔│ąŪĮĄĮŌ┬╩×ķŻ©67.6Ī└7.1Ż®%Ż¼COD╚ź│²┬╩×ķŻ©87.3Ī└1.5Ż®%ĪŻć└éźĖ╗Ą╚═©▀^śŗĮ©ą“┼·╩Įļp╩ęMFC╠Ä└Ē10mg/LĄ─č§╦─Łh╦ž╚╦╣żÅU╦«Ż¼č§╦─Łh╦žĄ─ūŅĖ▀╚ź│²┬╩┐╔▀_99.0%Ż¼MFCĄ─ūŅ┤¾▌ö│÷ļŖē║×ķ0.55Vū¾ėęĪŻ┐╔ęŖŻ¼═©▀^MFCĄ╚╔·╬’ļŖ╗»īWŽĄĮy╠Ä└ĒųŲ╦ÄÅU╦«Š▀ėąīóÅU╦«ųą╠N▓žĄ──▄į┤ęįļŖ─▄ą╬╩Į▌ö│÷Ą─Øō┴”Ż¼ī”╬█ÅU╦«ā¶╗»┼c─▄į┤╗ž╩šŠ▀ėąųžę¬ęŌ┴xĪŻ
╔·╬’ÅŖ╗»╝╝ąg═©▀^Ž“╬█─ÓĪóÅU╦«Ą╚╬ó╔·╬’╚║┬õųą╝ė╚ļ╣”─▄ąįŠ·ųĻŻ¼Ė─╔ŲįŁėąŽĄĮyĄ─ą¦─▄ĪŻ╔·╬’ÅŖ╗»╝╝ągæ¬ė├ė┌╬█╦«╠Ä└ĒŽĄĮyĄ─ā׳cŻ║1Ż®ā×╗»╬ó╔·╬’╚║┬õĮYśŗŻ╗2Ż®Ė─╔ŲļyĮĄĮŌ╬█╚Š╬’Ą─ĮĄĮŌą¦╣¹Ż╗3Ż®╠ßĖ▀ŽĄĮyæ¬ī”ČÓūāø_ō¶žō║╔Ą──▄┴”ĪŻ╚ń║╬ę²╚ļ╣”─▄ąįŠ·ųĻŻ¼▓ó╩╣Ųõį┌ŽĄĮyųąėąą¦Č©ų│╩Ū╔·╬’ÅŖ╗»╝╝ągĄ─ĻPµI▓Į¾EĪŻģŪ║ŃĄ╚└¹ė├╬█─ÓÆņ─ż║═Š·ä®Æņ─żĘĮ╩Į╠Ä└Ēą¾Ū▌Bų│ÅU╦«Ż¼▓╗═¼╔·╬’ÅŖ╗»ĘĮ╩Įą╬│╔Ą─╔·╬’─ż┤µį┌▓Ņ«ÉŻ¼Š·ä®Æņ─żĘĮ╩Į├„’@┐sČ╠┴╦ŽĄĮyĄ─åóäėĢrķgŻ¼╝ė┤¾┴╦ī”CODĪóNH4+-NĪóTNĄ─╚ź│²┬╩ĪŻ└Ņµ├Ą╚į┌Į╣╗»ÅU╦«A2O╣ż╦ćųą▓╔ė├╔·╬’ÅŖ╗»╝╝ągŻ¼╠Ē╝ėĖ▀ą¦ĮĄĮŌŠ·╝tŪ“Š·║¾Ż¼CODĪóÓŁ▀°Īó▀┴ÓżĄ─╚ź│²┬╩├„’@į÷╝ėŻ¼ŽĄĮyā╚ėąÖC╬█╚Š╬’ĮĄĮŌŠ·│╔×ķā×ä▌Š·ĪŻ
▒ŠčąŠ┐ęį╗Ņąį╬█─Ó×ķĻ¢śOĄū╬’Ż¼─ŻöM▒ĮĘėųŲ╦ÄÅU╦«×ķĻ¢śO╗∙┘|Ż¼śŗĮ©ļp╩ęMFCŽĄĮyŻ¼╠Ē╝ėļŖ╗Ņąį╬ó╔·╬’S.oneidensisMR-1ī”MFCŽĄĮy▀Mąą╔·╬’ÅŖ╗»Ż¼═©▀^Ž“ŽĄĮyų▒Įė╝ė╚ļŠ·æęę║Ż©ė╬ļx╝Ü░¹Ż®┼c╣╠Č©╝Ü░¹Ż¼ī”▒╚Ęų╬÷╣”─▄ąįŠ·ųĻ═Č╝ėą╬╩Įī”╗ņ║ŽMFCŽĄĮy«aļŖąį─▄Īó╬█╚Š╬’╚ź│²ą¦╣¹Īó╬ó╔·╬’Š·╚║ĮYśŗĄ─ė░ĒæĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 īŹ“×čbų├
MFCŽĄĮy░³└©ļŖ│žčbų├║═ļŖ─▄▓╔╝»čbų├ā╔▓┐ĘųŻ¼ęŖłD1ĪŻ
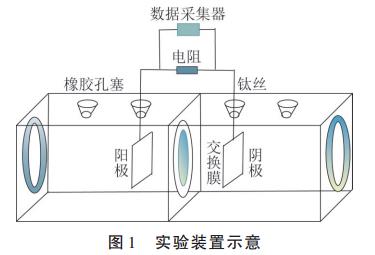
ļŖ│žčbų├×ķé„Įyļp╩ęśŗą═Ż¼▓─┘|×ķėąÖC▓Ż┴¦Ż¼ĻÄĻ¢ā╔╩ęėąą¦¾wĘeŠ∙×ķ118mLŻ¼ųąķgĖ¶ęįĻ¢ļxūėĮ╗ōQ─żŻ©CMI7000Ż®ĪŻ╩╣ė├ŅA╠Ä└Ē║¾Ą─╠╝ÜųŻ©30mmĪ┴30mmĪ┴2mmŻ®ū„×ķļŖśO▓─┴ŽŻ¼ĻÄĻ¢ļŖśOė├ŌüĮzŻ©ų▒ÅĮ×ķ0.6mmŻ®▀BĮė▓óė├Ž─z╚¹╣╠Č©Ż¼ā╔ļŖśOęį3cmķgĖ¶ŲĮąąŽÓī”ĪŻė├Ą¬ÜŌ┤ĄÆ▀ā╔śO╩ę▒Ż│ųģÆ解hŠ│Ż¼═ŌĮė1000”ĖļŖūĶśŗ│╔ķ]║Ž╗ž┬ĘĪŻļp╩ęMFC▀\ąą£žČ╚×ķŻ©30Ī└2Ż®ĪµĪŻ
ļŖ─▄▓╔╝»čbų├░³└©öĄō■▓╔╝»Ų„┼cļŖ─Xā╔▓┐ĘųĪŻöĄō■▓╔╝»Ų„×ķ╦{▓®ļŖ│ž£yį接ĮyŻ©LANBNTSŻ¼BT-2018CŻ®Ż¼═©▀^┼cļŖ─X▀BĮėīŹĢr’@╩ŠļŖ─▄öĄō■▓óėøõøĪŻģóöĄįOų├Ż║ļŖē║ĘČć·0~5VŻ¼▓╔╝»Š½Č╚1mVŻ¼▓╔╝»Ņl┬╩5min/┤╬ĪŻ
1.2 īŹ“×ĮėĘN╬’
1.2.1 ģÆč§╬█─Ó
╗Ņąį╬█─Ó╚Īūį╔Ž║Ż╩ą─│╬█╦«╠Ä└ĒÅSČ■│┴│žŻ¼ė├š¶s╦«╠įŽ┤3▒ķŻ¼▓óĮø200─┐║YŠW▀^×Vļs┘|Ż¼ļS║¾╝ė╚ļ▀m┴┐Ļ¢śOę║Ż¼ģÆ觌l╝■Ž┬ų├ė┌┤┼┴”öć░ĶŲ„╩ę£žŽ┬öć░Ķ3~5dŻ¼ņoų├Ęųīė╚ź╔ŽŪÕę║Ż¼├▄ĘŌéõė├ĪŻ▒ŠīŹ“×ļp╩ęMFCŽĄĮyŠ∙╠Ē╝ėģÆč§╬█─ÓŻ¼ģÆč§╬█─Ó┼cĻ¢śO╩ęĄ─¾wĘe▒╚×ķ1Ī├4ĪŻ
1.2.2 īŹ“×ė├╦«
Ļ¢śOę║ĮM│╔Ż║20mmol/L╚ķ╦ßŌcĪó1.42g/L┤ū╦ßŌcĪó0.31g/LNH4ClĪó0.13g/LKClĪó2.88g/LKH2PO4Īó6.57g/LK2HPO4Īó10mL/L╬ó┴┐į¬╦ž╚▄ę║║═10mL/LŠS╔·╦ž╚▄ę║ĪŻė├ŲŽ╠č╠Ūš{╣Ø▀M╦«CODĪŻ
─ŻöMųŲ╦ÄÅU╦«ĮM│╔Ż║▒ĮĘė┘|┴┐ØŌČ╚100mg/LŻ¼┴Ē═Ō╝ė╚ļ20mmol/L╚ķ╦ßŌcĪó0.31g/LNH4ClĪó0.13g/LKClĪó2.88g/LKH2PO4Īó6.57g/LK2HPO4Īó10mL/L╬ó┴┐į¬╦ž╚▄ę║║═10mL/LŠS╔·╦ž╚▄ę║ĪŻė├ŲŽ╠č╠Ūš{╣Ø▀M╦«CODĪŻ
ĻÄśO╚▄ę║Ż║0.1mol/LĶFŪĶ╗»Ōø╚▄ę║
1.2.3 «aļŖŠ·ĘN
S.oneidensisMR-1┘Åė┌ųąć°Ąõą═┼ÓB╬’▒Ż▓žųąą─Ż©CCTCCŻ®ĪŻ
S.oneidensisMR-1Š·ę║┼ÓBŻ║¤oŠ·Śl╝■Ž┬Ż¼ė├ĮėĘNŁh╠¶╚Ī╗Ņ╗»║¾Ą─S.oneidensisMR-1å╬Š·┬õŻ¼Įė╚ļ£ńŠ·└õģs║¾Ą─LB┼ÓB╗∙ųąŻ¼į┌30ĪµĪó120r/minŚl╝■Ž┬┼ÓBų┴ī”öĄ╔·ķL─®Ų┌ĪŻLBę║¾w┼ÓB╗∙ė╔10g/Lę╚Ą░░ūļ╦Īó5g/LĮ═─Ė╠ß╚Ī╬’║═10g/LNaClĮM│╔ĪŻ
S.oneidensisMR-1Š·æęę║ųŲéõŻ║Ž╚īóŠ·ę║į┌4000r/minŚl╝■Ž┬ļxą─15minŻ¼į┘ė├¤oŠ·ŠÅø_ę║Ž┤£ņ▓óųžæęĪŻ
1.3 MFCŽĄĮyĄ─ĮėĘN┼c▀\ąą
īŹ“×╔µ╝░Ą─3ĮMMFCŽĄĮy░³└©▓╗╠Ē╝ė«aļŖŠ·Ą─ļp╩ęMFCĪóė╬ļxæB╝Ü░¹ļp╩ęMFC║═╣╠Č©╗»╝Ü░¹ļp╩ęMFCŻ¼ę└┤╬ś╦ėø×ķMFC1ĪóMFC2║═MFC3ĪŻ
▒ŠīŹ“×▀xė├Ą─ĻÄĻ¢ļŖśO▓─┴ŽŠ∙×ķ╠╝ÜųŻ¼╩╣ė├ų«Ū░ąĶĮø╦ßąįųžŃt╦ßŌøĮ■┼▌Ż©60Īµ╦«įĪ╝ė¤ß30minŻ®┼c±RĖźĀtŅA╠Ä└ĒŻ©450Īµ╝ė¤ß30minŻ®Ż¼ŅA╠Ä└Ē║¾Ą─╠╝Üų┐╔ų▒Įėū„×ķļŖśOĪŻŲõųąŻ¼MFC3Ą─╠╝ÜųĻ¢śOąĶ▀Mę╗▓Į╠Ä└ĒŻ¼ųŲéõĘĮĘ©×ķīóŅA╠Ä└Ē║¾Ą─╠╝Üų▀BĮėŌüĮzŻ¼┼c3mLS.oneidensisMR-1ę║¾wŠ·ę║╣▓═¼╝ė╚ļ£ńŠ·║¾Ą─LB┼ÓB╗∙Ż¼į┌35ĪµĪó120r/minŚl╝■Ž┬┼ÓB7dĪŻMFC2╝ė╚ļ«aļŖŠ·Ą─ĘĮ╩Į×ķŽ“Ļ¢śO╩ę╠Ē╝ėS.oneidensisMR-1Š·æęę║5mLĪŻMFC1Ą─ĮėĘN╬’āH×ķģÆč§╬█─ÓĪŻ═©▀^š{š¹OD600īó3ĮMMFCčbų├Ą─Ļ¢śOę║╔·╬’┴┐▒Ż│ųę╗ų┬ĪŻ3ĮMMFCčbų├Ą─ĻÄśOę║Š∙×ķ0.1mol/LĶFŪĶ╗»Ōø╚▄ę║Ż¼×ķ▒ŻūC│õūŃĄ─ļŖūė╩▄¾wŻ¼«öĻÄśOę║ė╔³S╔½ūā×ķ£\ŠG╔½ĢrĖ³ōQĻÄśOę║ĪŻ
į┌åóäėļAČ╬Ż¼īóĻ¢śOę║╝ė╚ļMFCĻ¢śO╩ęŻ¼Ļ¢śO╩ę│§╩╝CODį┌Ż©2000Ī└100Ż®mg/LŻ¼▀B└mā╔éĆų▄Ų┌ūŅ┤¾ļŖē║ŽÓĮ³ęĢ×ķåóäė│╔╣”ĪŻį┌š²╩Į▀\ąąļAČ╬Ż¼īóĻ¢śOę║Ė³ōQ×ķ─ŻöMųŲ╦ÄÅU╦«Ż¼ļŖē║ĮĄų┴50mVęįŽ┬ęĢ×ķę╗éĆų▄Ų┌ĮY╩°Ż¼ąĶĖ³ōQĻÄĻ¢ļŖśOę║│ų└m▀\ąąŻ¼├┐ų▄Ų┌Ļ¢śO│§╩╝COD▒Ż│ųį┌Ż©3000Ī└100Ż®mg/LŻ¼▀B└m▀\ąą3éĆų▄Ų┌ĪŻ
1.4 öĄō■£yČ©┼cĘų╬÷
1.4.1 «aļŖąį─▄
ļŖ╗»īWąį─▄Ż║ļŖē║U═©▀^ļŖ─▄▓╔╝»čbų├▓╔╝»Ż╗ļŖ┴„IĖ∙ō■╩ĮŻ©1Ż®ÜW─ĘČ©┬╔ėŗ╦ŃŻ╗ļŖ┴„├▄Č╚IAĖ∙ō■╩ĮŻ©2Ż®ėŗ╦ŃŻ╗╣”┬╩├▄Č╚Ż©PAŻ®Ė∙ō■╩ĮŻ©3Ż®ėŗ╦ŃŻ╗śO╗»Ū·ŠĆ┼c╣”┬╩├▄Č╚ė╔═ŌļŖūĶĘ©£yČ©Ż¼═ŌĮėļŖūĶŽõė╔Ė▀ĄĮĄ═Ė─ūāļŖūĶųĄŻ¼ę└┤╬×ķ10000Īó8000Īó6000Īó4000Īó2000Īó1000Īó800Īó600Īó400Īó200Īó100”ĖŻ¼├┐éĆūĶųĄŽ┬▀\ąą15~20min▓óėøõøŻ╗ļŖ│žā╚ūĶrė╔śO╗»Ū·ŠĆą▒┬╩Ū¾Ą├Ż╗Ļ¢śO╔·╬’─żĄ─裣hĘ³░▓Ū·ŠĆŻ©CVŻ®═©▀^╚²ļŖśO¾wŽĄ£yĄ├Ż¼Æ▀├Ķ╦┘Č╚×ķ10mV/sŻ¼Æ▀├ĶļŖē║×ķ-0.8~0.4VŻ¼Ųõųąī”ļŖśO×ķŃKĮzļŖśOŻ¼ģó▒╚ļŖśO×ķAg/AgClļŖśOŻ¼╣żū„ļŖśO×ķĻ¢śO╠╝ÜųĪŻ
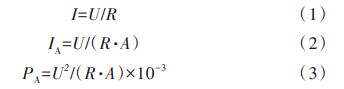
╩ĮųąŻ║IĪ¬Ī¬ļŖ┴„Ż¼mAŻ╗UĪ¬Ī¬ļŖē║Ż¼mVŻ╗RĪ¬Ī¬ļŖūĶŻ¼”ĖŻ╗IAĪ¬Ī¬ļŖ┴„├▄Č╚Ż¼mA/m2Ż╗AĪ¬Ī¬Ļ¢śO├µĘeŻ¼m2Ż╗PAĪ¬Ī¬╣”┬╩├▄Č╚Ż¼mW/m2ĪŻ
1.4.2 ╬█╚Š╬’╚ź│²ą¦╣¹
▒ĮĘė▓╔ė├╦─░▒╗∙░▓╠µ▒╚┴ųĘ©£yČ©Ż╗COD┼cNH4+-NĖ∙ō■ć°ś╦Ę©£yČ©Ż╗Äņü÷ą¦┬╩Ż©CEŻ®Ė∙ō■╩ĮŻ©4Ż®ėŗ╦ŃĪŻ
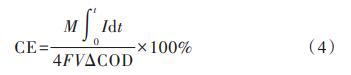
╩ĮųąŻ║CEĪ¬Ī¬Äņü÷ą¦┬╩Ż╗MĪ¬Ī¬O2Ą──”Ā¢┘|┴┐Ż¼32g/molŻ╗tĪ¬Ī¬ų▄Ų┌▀\ąąĢrķgŻ¼sŻ╗IĪ¬Ī¬tĢr┐╠Ą─ļŖ┴„Ż¼mAŻ╗VĪ¬Ī¬Ļ¢śO╩ę¾wĘeŻ¼mLŻ╗FĪ¬Ī¬Ę©└ŁĄ┌│ŻöĄŻ¼96485C/molŻ╗”żCODĪ¬Ī¬▀\ąą╩╝─®Ą─CODūā╗»┴┐Ż¼g/LĪŻ
1.4.3 Ļ¢śO╔·╬’─żą╬├▓▒Ēš„
Ļ¢śO╠╝ÜųĮø╬ņČ■┤╝╚▄ę║╣╠Č©Īó┴ū╦ß¹}ŠÅø_ę║ø_Ž┤Īó╠▌Č╚ęę┤╝╚▄ę║├ō╦«Īó└õā÷Ė╔į’ĪóćŖĮ╠Ä└Ē║¾Ż¼╩╣ė├Æ▀├ĶļŖūė’@╬óńRŻ©ZEISSGeminiSEM300Ż®ė^£yĻ¢śO╔·╬’─żą╬├▓ĪŻ
1.4.4 Ļ¢śO╔·╬’─ż╬ó╔·╬’╚║┬õĮYśŗĘų╬÷
▀\ąąĮY╩°║¾Ż¼īóĻ¢śO╠╝ÜųĘ┼╚ļPBS¤oŠ·ŠÅø_ę║ųąōu┤▓š±╩Ä30~60minŻ¼īóĻ¢śO╠╝Üų╚Ī│÷Ż¼Ž╚ė├ā╔īė¤oŠ·╝å▓╝▀^×V╚ź│²ļs┘|Ż¼į┘ė├0.22µmŽ§╦ß└wŠS╦ž×V─ż▀^×VŻ¼īó×V─ż╦═Öz16SrRNA£yą“ĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 «aļŖąį─▄Ęų╬÷
Ė„MFCŽĄĮyĄ─åóäėļŖē║Īóš²╩Į▀\ąą▌ö│÷ļŖē║ĪóśO╗»Ū·ŠĆ┼c╣”┬╩├▄Č╚ĪóCVŪ·ŠĆī”▒╚ŪķøręŖłD2ĪŻ
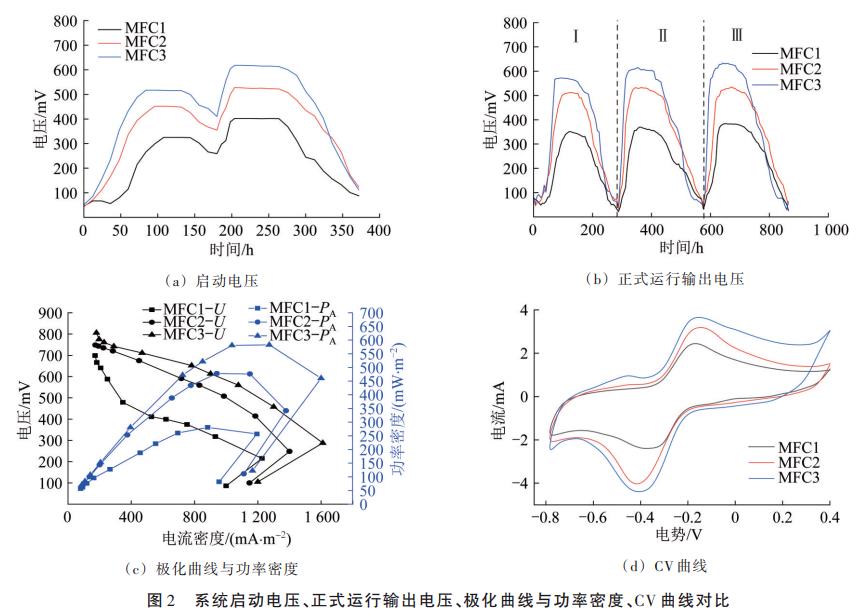
Ė„MFCŽĄĮyåóäė▀^│╠Ęų×ķā╔éĆļAČ╬Ż¼Ė„ļAČ╬ļŖē║ūā╗»╚ńłD2Ż©aŻ®╦∙╩ŠĪŻį┌Ą┌ó±ļAČ╬Ż¼MFC1ĪóMFC2ĪóMFC3▀_ĄĮūŅ┤¾ļŖē║╦∙ąĶĢrķgĘųäe×ķ108Īó93Īó82hŻ¼ī”æ¬Ą─ūŅ┤¾ļŖē║Ęųäe×ķ325Īó452Īó517mVĪŻ×ķ▀Mę╗▓Įį┌Ļ¢śO╔ŽĖ╗╝»ā×ä▌«aļŖŠ·╚║╝░╠ß╔²Ė„čbų├«aļŖąį─▄Ż¼į┌ļŖē║Ž┬ĮĄļAČ╬Ž“Ė„čbų├Ļ¢śOĘųäe╝ė╚ļ1gŲŽ╠č╠Ūęįča│õ╠╝į┤ĪŻį┌Ą┌ó“ļAČ╬Ż¼ļŖē║čĖ╦┘╔Ž╔²Ż¼MFC1ĪóMFC2ĪóMFC3Ą─ūŅ┤¾ļŖē║Ęųäe╔²Ė▀ų┴402Īó528Īó618mVŻ¼ŪęūŅ┤¾ļŖē║│ų└mĢrķg├„’@į÷╝ėŻ¼ęĢ×ķĖ„MFCŽĄĮyåóäė│╔╣”ĪŻ┤²ļŖē║ĮĄų┴100mVęįŽ┬Ż¼īóĻ¢śOę║Ė³ōQ×ķ─ŻöMųŲ╦ÄÅU╦«│ų└m▀\ąą3ų▄Ų┌ĪŻ
į┌š²╩Į▀\ąąļAČ╬Ż¼Ė„īŹ“×ĮM▌ö│÷ļŖē║ļSĢrķgūā╗»▀^│╠╚ńłD2Ż©bŻ®╦∙╩ŠĪŻ┐╔ė^▓ņĄĮŻ¼ė╔ė┌3ĮMčbų├Ą─Ļ¢śOųą╩ū┤╬╝ė╚ļųŲ╦ÄÅU╦«Ż¼3ĮMMFCčbų├╠Äė┌▀mæ¬ļAČ╬Ż¼į┌Ą┌ó±ų▄Ų┌MFC1ĪóMFC2ĪóMFC3Ą─ūŅ┤¾▌ö│÷ļŖē║Š∙Ą═ė┌åóäė▀^│╠Ą─Ą┌ó“ļAČ╬Ż¼Ęųäe×ķ351Īó512Īó572mVĪŻį┌Ą┌ó“Īóó¾ų▄Ų┌Ż¼ļSĻ¢śO▒Ē├µ╔·╬’─żųØu│╔╩ņŻ¼╬ó╔·╬’é„▀fĄĮĻ¢śOĄ─ļŖūėöĄ┴┐į÷╝ėŻ¼ŽĄĮy┌ģė┌ĘĆČ©Ż¼Ė„īŹ“×ĮMūŅĖ▀▌ö│÷ļŖē║│ų└mį÷╝ėŻ¼Š∙į┌Ą┌ó¾ų▄Ų┌╚ĪĄ├ūŅ┤¾ļŖē║Ż¼Ūęį┌▌^Ė▀ļŖē║Ž┬│ų└mĢrķgį÷ķLŻ¼MFC1ĪóMFC2ĪóMFC3▌ö│÷ļŖē║Ęųäe×ķ384Īó535Īó633mVĪŻė╔┤╦┐╔ęį┐┤│÷Ż¼į┌▒ŠčąŠ┐ųŲéõĄ─3ĮMMFCčbų├ųąŻ¼ęįųŲ╦ÄÅU╦«×ķĻ¢śOę║ė├ė┌░lļŖ╩Ū┐╔ąąĄ─ĪŻ
į┌Ą┌ó¾ų▄Ų┌£yĄ├Ė„čbų├śO╗»Ū·ŠĆ┼c╣”┬╩├▄Č╚Ū·ŠĆŻ¼╚ńłD2Ż©cŻ®╦∙╩ŠĪŻMFC1ĪóMFC2ĪóMFC3Ą─ūŅ┤¾╣”┬╩├▄Č╚Ęųäe×ķ280.9Īó477.9Īó582.7mW/m2Ż¼ā╚ūĶĘųäe×ķ516.7Īó459.2Īó398.8”ĖŻ¼ķ_┬ĘļŖē║Ęųäe×ķ674Īó808Īó836mVĪŻ┴Ē═ŌŻ¼┐╔ė^▓ņĄĮį┌Ė─ūā═ŌļŖūĶ▀^│╠ųąŻ¼«ö═ŌĮėļŖūĶė╔╚fÜWĪóŪ¦ÜW╝ēĮĄĄ═ĄĮ░┘ÜW╝ēĢrŻ¼ė╔ė┌Ļ¢śO╬ó╔·╬’ī”Ąū╬’Ą─└¹ė├┤µį┌ūĶ┴”ęį╝░ļŖūėé„▀f▀^│╠┤µį┌ūĶ┴”Ż¼╬ó╔·╬’¤oĘ©╠ß╣®ūŃē“Ą─ļŖūėęį╣®«aļŖŻ¼ī¦ų┬«aļŖ┴┐čĖ╦┘£p╔┘Ż¼╣”┬╩├▄Č╚Ū·ŠĆ┼cśO╗»Ū·ŠĆųą│÷¼F╗žš█ĪŻ
×ķ▀Mę╗▓Į╠ĮŠ┐Ļ¢śO╔·╬’─żĄ─ļŖ╗ŅąįŻ¼ī”▒╚Ęų╬÷Ė„īŹ“×ĮM╠╝ÜųĻ¢śOĄ─裣hĘ³░▓Ū·ŠĆŻ©CVŻ®Ż¼╚ńłD2Ż©dŻ®╦∙╩ŠĪŻŽÓ▒╚MFC1Ż¼MFC2ĪóMFC3Ļ¢śO╔·╬’─żĄ─č§╗»▀ĆįŁĘÕ▌^├„’@Ż¼ĘÕųĄļŖ┴„Ęųäe×ķ3.2Īó3.7mAĪŻŲõųąŻ¼MFC3Ą─ĘÕųĄļŖ┴„ūŅĖ▀Ż¼CVŪ·ŠĆĘeĘų├µĘeūŅ┤¾Ūęī”ĘQąį▌^║├Ż¼šf├„╣╠Č©╝Ü░¹MFCĻ¢śO╔·╬’─ż╗Ņąį▌^Ė▀Ż¼ļŖūė▐DęŲą¦╣¹╝░ī”ĘQąįĖ³╝čĪŻ
╔Ž╩÷ĮY╣¹▒Ē├„Ż¼╠Ē╝ė«aļŖŠ·Ą─ā╔ĮMMFCĄ─«aļŖąį─▄▌^āH╠Ē╝ė╬█─ÓĄ─ļp╩ęMFC«aļŖąį─▄├„’@╠ß╔²Ż¼ŪęåóäėĢrķg┐sČ╠Ż¼MFC3«aļŖąį─▄ūŅ╝čŻ¼ŲõūŅ┤¾╣”┬╩├▄Č╚▌^MFC1ĪóMFC2Ęųäe╠ßĖ▀┴╦107.4%Īó21.9%ĪŻį┌Ļ¢śO╩ęųą╠Ē╝ė«aļŖŠ·S.oneidensisMR-1╠ß╔²┴╦MFCĄ─«aļŖąį─▄Ż¼Ųõ┤┘▀MŽĄĮy«aļŖĄ─įŁ└Ē×ķS.oneidensisMR-1ā╚─żĪó═Ō─ż║═ų▄┘|┐šķg┤µį┌Ą─ČÓĘNč§╗»▀ĆįŁĄ░░ū─▄═©▀^ų▒Įė║═ķgĮėļŖūėé„▀f▀^│╠▀Mąąėąč§/¤oč§║¶╬³Ż¼▓óĘų├┌║╦³S╦žū„×ķģó┼c░¹═ŌļŖūė▐DęŲ▀^│╠Ą─č§╗»▀ĆįŁĮķ¾wŻ¼╠ß╔²░¹═ŌļŖūė▐DęŲ─▄┴”Ż¼┤┘▀MĻ¢śOč§╗»Ę┤æ¬Ż¼▀MČ°╠ß╔²ŽĄĮyĄ─č§╗»▀ĆįŁĘ┤æ¬╦┘┬╩ĪŻ
2.2 ╬█╚Š╬’╚ź│²ą¦╣¹Ęų╬÷
×ķ£yČ©▓╗═¼MFCŽĄĮyĻ¢śO╩ę╬█╚Š╬’ĮĄĮŌą¦╣¹╝░ķgĮėšŲ╬š╬ó╔·╬’Š·╚║Ą─┤·ųxŪķørŻ¼į┌š²╩Įåóäė║¾ī”3ĮMMFCčbų├Ļ¢śO╩ęCODĪóNH4+-NĪó▒ĮĘėĪóÄņü÷ą¦┬╩▀Mąą3ų▄Ų┌▒O£yŻ¼Ė„ų▄Ų┌╬█╚Š╬’╚ź│²┬╩ęŖ▒Ē1Ż¼3ų▄Ų┌ā╚╬█╚Š╬’ŲĮŠ∙╚ź│²ą¦╣¹╝░Ė„ų▄Ų┌Äņü÷ą¦┬╩ęŖłD3ĪŻ
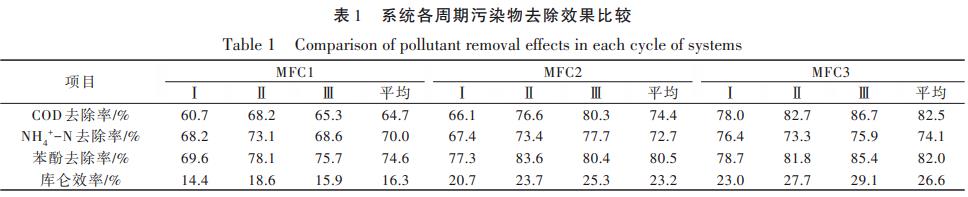
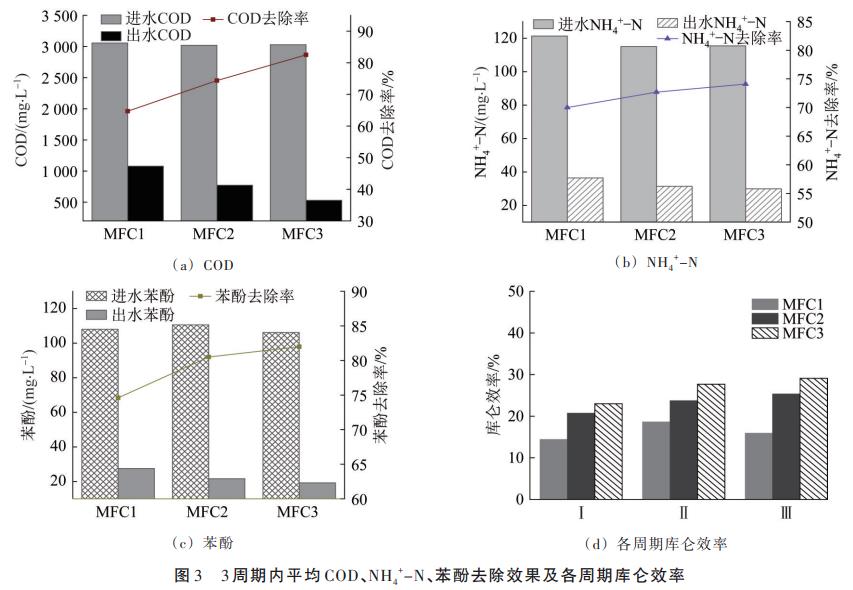
COD─▄ē“Ę┤ė│MFCųąėąÖC╬’ĮĄĮŌŪķørĪŻė╔łD3Ż©aŻ®┐╔ęŖŻ¼3ų▄Ų┌ā╚MFC1ĪóMFC2ĪóMFC3ŲĮŠ∙▀M╦«CODĘųäe×ķ3055.3Īó3019.3Īó3028.7mg/LŻ¼ŲĮŠ∙│÷╦«CODĘųäe×ķ1078.0Īó772.3Īó530.7mg/LŻ¼ŲĮŠ∙COD╚ź│²┬╩Ęųäe×ķ64.7%Īó74.4%Īó82.5%Ż¼MFC3Ą─ŲĮŠ∙COD╚ź│²┬╩├„’@Ė▀ė┌MFC1║═MFC2Ż¼šf├„╣╠Č©╝Ü░¹MFCī”ėąÖCĄū╬’Ą─┤·ųx─▄┴”ūŅÅŖĪŻ
ė╔łD3Ż©bŻ®┐╔ęŖŻ¼3ų▄Ų┌ā╚MFC1ĪóMFC2ĪóMFC3Ą─ŲĮŠ∙NH4+-N╚ź│²┬╩ŽÓ▓Ņ▓╗┤¾Ż¼Ęųäe×ķ70.0%Īó72.7%Īó74.1%Ż¼NH4+-N─▄ʱį┌╔·╬’ļŖ╗»īWŽĄĮyųąų▒Įėū„×ķļŖūė╩▄¾w╔ą¤oČ©šōŻ¼Ļ¢śO╩ęĄ─NH4+-Nų„ę¬═©▀^ģÆč§░▒č§╗»ū„ė├ĪóģÆč§Ę┤Ž§╗»ū„ė├Īó░▒Ą¬▀węŲū„ė├╚ź│²ĪŻ
ė╔łD3Ż©cŻ®┐╔ęŖŻ¼3ų▄Ų┌ā╚MFC1Ą─ŲĮŠ∙▒ĮĘė╚ź│²┬╩ūŅĄ═Ż¼×ķ74.6%Ż¼Č°MFC2║═MFC3Ą─ŲĮŠ∙▒ĮĘė╚ź│²┬╩ŽÓĮ³Ż¼Ęųäe×ķ80.5%Īó82.0%ĪŻ═©▀^MFCĮĄĮŌ║¼▒ĮĘėÅU╦«╩Ū┐╔ąąĄ─Ż¼ŽÓĻP蹊┐▒Ē├„┼cå╬ę╗▒ĮĘė╚╝┴ŽŽÓ▒╚Ż¼ęį▒ĮĘė║═ŲŽ╠č╠Ū╗ņ║Ž╬’×ķ╚╝┴ŽĖ³ęū┤┘▀MMFCŽĄĮyĄ─«aļŖąį─▄ĪŻ
Äņü÷ą¦┬╩Ż©CEŻ®─▄ē“Ę┤ė│Ė„ų▄Ų┌Ąū╬’╗∙┘|▐DęŲĄĮĻ¢śOĄ─īŹļHļŖūėöĄ┴┐┼c└ĒšōļŖūėöĄ┴┐ų«ķgĄ─ĻPŽĄŻ¼╩ŪįuārMFCī”ÅU╦«╠Ä└Ēą¦╣¹Ą─ųžę¬ųĖś╦ų«ę╗ĪŻė╔łD3Ż©dŻ®║═▒Ē1┐╔ęŖŻ¼MFC1Ą─Äņü÷ą¦┬╩Ž╚╔²Ė▀║¾Ž┬ĮĄŻ¼Č°MFC2┼cMFC3Ą─Äņü÷ą¦┬╩į┌Ą┌ó“Īóó¾ų▄Ų┌ā╚Š∙╔²Ė▀Ż¼MFC1ĪóMFC2ĪóMFC3į┌3ų▄Ų┌ā╚Ą─ŲĮŠ∙Äņü÷ą¦┬╩Ęųäe×ķ16.3%Īó23.2%Īó26.6%ĪŻMFC2ĪóMFC3Ą─Ąū╬’ėąą¦«aļŖ└¹ė├┬╩▌^Ė▀Ż¼«aļŖŠ·S.oneiden⁃sisMR-1ī”MFCŽĄĮyŲĄĮ┴╦╔·╬’ÅŖ╗»ū„ė├Ż¼╝ėÅŖ┴╦ŽĄĮy«aļŖąį─▄┼c╬█╚Š╬’╚ź│²─▄┴”ĪŻ
į┌Ą┌ó¾ų▄Ų┌Ż¼MFCŽĄĮyųąĖ„╬█╚Š╬’Ct/C0ļSĢrķgūā╗»Ą─┌ģä▌ęŖłD4ĪŻ
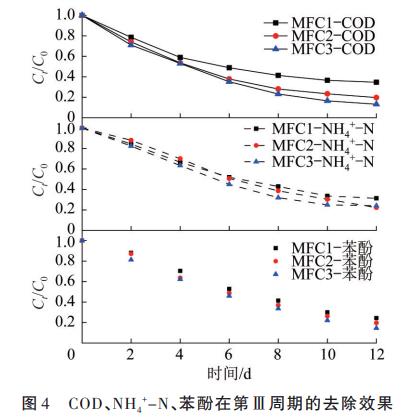
ŽÓ▌^ė┌MFC1Ż¼MFC2║═MFC3Ą─Ė„╬█╚Š╬’╚ź│²╦┘┬╩Š∙ėą├„’@╠ß╔²Ż¼MFC3Ą─Ė„╬█╚Š╬’╚ź│²╦┘┬╩ūŅĖ▀ĪŻĮøę╗╝ēĘ┤æ¬äė┴”īWöM║ŽŻ¼MFC3╚ź│²CODĪóNH4+-NĪó▒ĮĘėĄ─ę╗╝ēĘ┤æ¬äė┴”īW╦┘┬╩│ŻöĄĘųäe×ķ0.18Ż©R2=0.99Ż®Īó0.13Ż©R2=0.97Ż®Īó0.16d-Ż©1R2=0.98Ż®ĪŻ
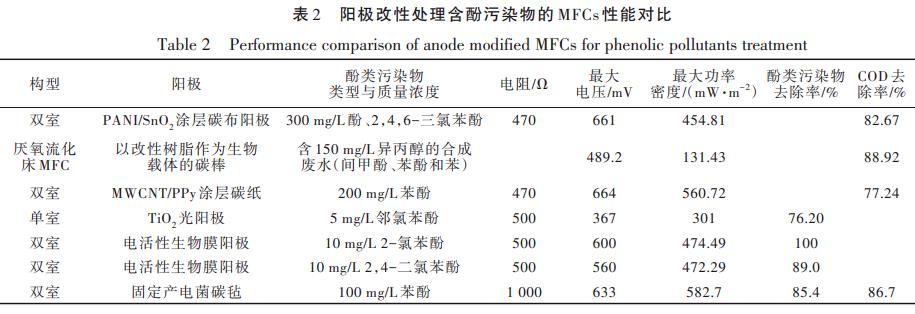
═©▀^ī”▒╚╬█╚Š╬’╚ź│²┬╩┼c╚ź│²╦┘┬╩Ą├│÷Ż¼╣╠Č©╗»╝Ü░¹MFCī”╬█╚Š╬’╚ź│²ą¦╣¹ūŅ╝čĪŻZhuangzhuangLIUĄ╚Å─ži╝SųąĘųļx│÷1ųĻą┬ą═╦─Łh╦ž├ō│²Š·Ż¼įōŠ·ųĻį┌ė╬ļxæBī”╦─Łh╦žūŅĖ▀╚ź│²┬╩×ķ71.62%Ż¼╩╣ė├¶╚╝ū╗∙└wŠS╦ž║═Š█ČÓ░═░Ę╣╠Č©╗Ņ╝Ü░¹║¾Ż¼╦─Łh╦ž╚ź│²┬╩▀_ĄĮ91.16%ĪŻė╬ļxæBŠ·ųĻęū┼cįŁėąŠ·╚║ĖéĀÄŻ¼ī¦ų┬┤µ╗Ņ┬╩▌^Ą═Ż¼ė░Ēæ╬█╚Š╬’╚ź│²ą¦╣¹Ż¼Č°╣╠Č©╗»╝Ü░¹╝╝ąg─▄ėąą¦╠ßĖ▀╝Ü░¹├▄Č╚╝░╗ŅąįŻ¼Ė³▀mė├ė┌ĮĄĮŌÅ═ļs╬█╚Š╬’ĪŻį┌▒ŠīŹ“×3ų▄Ų┌Ą─£yįćųąŻ¼╣╠Č©╗»╝Ü░¹MFCĄ─«aļŖąį─▄┼c╬█╚Š╬’╚ź│²─▄┴”ūŅ╝čŻ¼┼cŲõ╦¹ŽÓĻP蹊┐Ż©▒Ē2Ż®ī”▒╚Ż¼╣╠Č©╗»╝Ü░¹╝╝ągæ¬ė├ė┌MFCŽĄĮyųąŠ▀ėąį┌╚ź│²Å═ļs╬█╚Š╬’═¼Ģr«a╔·ļŖ─▄Ą─Øō┴”ĪŻ
2.3 Ļ¢śO╔·╬’─żą╬├▓▒Ēš„
×ķ▀Mę╗▓ĮšŲ╬šĻ¢śO╬ó╔·╬’ĖĮų°ŪķørŻ¼ī”Ļ¢śO╔·╬’─ż▀MąąSEMą╬├▓▒Ēš„Ż¼ęŖłD5ĪŻ

łD5Ż©aŻ®×ķāHĮøųžŃt╦ßŌø╚▄ę║┼c±RĖźĀt╝ė¤ßŅA╠Ä└ĒĄ─┐š░ū╠╝ÜųŻ¼Ųõ▒Ē├µ╣Ō╗¼Īó┐pŽČ┤¾Ż¼×ķ╬ó╔·╬’Ą─ĖĮų°╠ß╣®┴╦Śl╝■ĪŻļSMFC│╔╣”åóäė┼c▀\ąąŻ¼╬ó╔·╬’į┌Ļ¢śO▒Ē├µĖ╗╝»│╔─żŻ¼łD5Ż©bŻ®ĪółD5Ż©cŻ®║═łD5Ż©dŻ®Ęųäe×ķMFC1ĪóMFC2║═MFC3Ą─Ļ¢śOą╬├▓łDŻ¼MFC2ĪóMFC3Ą─Ļ¢śO▒╚▒Ē├µĘe┼c┤ų▓┌Č╚▌^┤¾Ż¼ėą└¹ė┌╬ó╔·╬’Ą─ĖĮų°Ż¼ĖĮų°╬ó╔·╬’Ą─ĘNŅÉĖ³×ķžSĖ╗ĪŻ
2.4 Ļ¢śO╔·╬’─ż╬ó╔·╬’╚║┬õĮYśŗĘų╬÷
Ļ¢śO╔·╬’─żŠ·╚║ĮYśŗ╩Ūė░Ēæ╬█╚Š╬’╚ź│²║═ļŖ─▄«a╔·Ą─ųžę¬ę“╦žŻ¼Ļ¢śO╬ó╔·╬’╚║┬õų«ķg┤µį┌ģf═¼ū„ė├Ż¼Š▀ėą▓╗═¼╣”─▄Ą─╬ó╔·╬’Ż©╚ń«aļŖŠ·Īó╦«ĮŌ╝ÜŠ·┼c░lĮ═╝ÜŠ·Ż®į┌ŽĄĮyųą╣▓┤µŻ¼ĮĄĮŌ╬█╚Š╬’▓ó½@Ą├ļŖ─▄ĪŻĻ¢śO╔·╬’─żį┌ķT╦«ŲĮ║═ī┘╦«ŲĮŽ┬Ą─╬ó╔·╬’ĮYśŗĮM│╔ęŖłD6ĪŻ
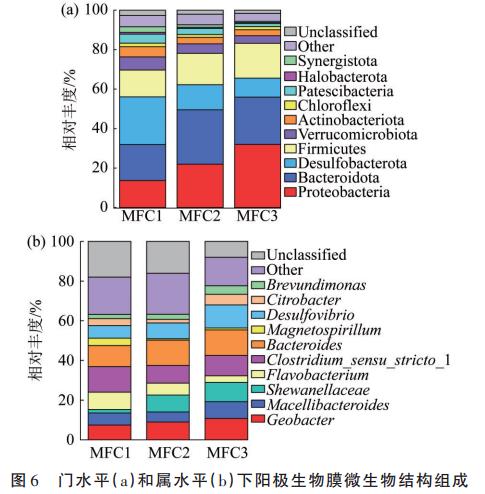
ė╔łD6┐╔ų¬Ż¼┼c▓╗╠Ē╝ė«aļŖŠ·Ą─MFC1ŽÓ▒╚Ż¼╠Ē╝ėė╬ļxæB╝Ü░¹Ą─MFC2Īó╣╠Č©╗»╝Ü░¹Ą─MFC3Ą─Ļ¢śO╔·╬’─ż╝ÜŠ·╚║┬õĮYśŗ░l╔·┴╦ę╗Č©ūā╗»ĪŻį┌ķT╦«ŲĮŽ┬Ż¼3ĮMčbų├Ļ¢śO╔·╬’─żĄ─Ū░4ĘNā×ä▌Š·ķTŠ∙░³└©ProteobacteriaŻ©ūāą╬Š·ķTŻ®ĪóBacteroidotaŻ©öMŚUŠ·ķTŻ®ĪóDesulfobacterotaŻ©├ō┴“ŚUŠ·ķTŻ®║═FirmicutesŻ©║±▒┌Š·ķTŻ®Ż¼╩Ū│ŻęŖė┌MFCŽĄĮyĄ─ļŖ╗ŅąįŠ·ķTŻ¼┐╔▀MąąģÆ觎¹╗»▓óį÷ÅŖŽĄĮy«aļŖąį─▄Ż¼▀@4ĘNā×ä▌Š·ķTį┌MFC1ĪóMFC2ĪóMFC3ųąĄ─┐éŽÓī”žSČ╚Ęųäe×ķ69.63%Īó78.13%Īó83.23%Ż¼ŪęĖ„MFCŽĄĮy4ĘNā×ä▌Š·ķTśŗ│╔▒╚└²ėą╦∙▓╗═¼ĪŻ
į┌ī┘╦«ŲĮŽ┬Ż¼ūāą╬Š·ķTųąĄõą═Ą─ļŖ╗Ņąį╬ó╔·╬’GeobacterŻ©ĄžŚUŠ·ī┘Ż®ĪóDesulfovibrioŻ©├ō┴“╗ĪŠ·ī┘Ż®ĪóCitrobacterŻ©ÖÄ├╩╦ߌUŠ·ī┘Ż®ĪóShewanellaceaeŻ©ŽŻ═▀╩ŽŠ·ī┘Ż®į┌Ļ¢śO╔·╬’─ż╔ŽĄ├ĄĮ┴╦Ė╗╝»ĪŻŲõųąŻ¼Geobacterį┌MFC1ĪóMFC2ĪóMFC3ųąĄ─ŽÓī”žSČ╚Ęųäe×ķ7.40%Īó8.92%Īó10.74%Ż╗Desulfovibrioį┌MFC1ĪóMFC2ĪóMFC3ųąĄ─ŽÓī”žSČ╚Ęųäe×ķ6.36%Īó7.91%Īó11.66%Ż╗Citrobacterį┌MFC1ĪóMFC2ĪóMFC3ųąĄ─ŽÓī”žSČ╚Ęųäe×ķ3.53%Īó1.84%Īó5.29%Ż╗MFC3ųąShe⁃wanellaceaeĄ─ŽÓī”žSČ╚ūŅĖ▀Ż¼×ķ9.72%Ż¼šf├„╣╠Č©╗»╝╝ągėąą¦╠ßĖ▀┴╦MFCųąShewanellaceaeĄ─├▄Č╚╝░╗ŅąįĪŻ░lĮ═╝ÜŠ·Clostridium_sensu_stricto_1Ż©╦¾ĀŅč┐░¹ŚUŠ·Ż®ĪóBacteroidesŻ©öMŚUŠ·Ż®į┌Ė„īŹ“×ĮMĄ─Ļ¢śO╔·╬’─ż╔ŽĄ├ĄĮĖ╗╝»Ż¼Ųõū„ė├╩ŪĮĄĮŌėąÖC╬’┘|Ż¼×ķļŖ╗Ņąį╬ó╔·╬’╠ß╣®╠╝į┤ĪŻį┌Ļ¢śO╔·╬’─ż╔Ž▀ĆÖz£yĄĮMagneto⁃spirillumŻ©”┴-ūāą╬Š·ŠV┤┼┬▌Š·ī┘Ż®Ż¼MagnetospirillumĄ─╠ž³c╩Ū║Ž│╔┤┼ąĪ¾w║═▀Mąą┌ģ┤┼▀\äėŻ¼Š▀ėąČÓśė╗»Ą─╔·└Ē┤·ųx▀^│╠Ż¼Ą½Ųõį┌MFCŽĄĮy░ńč▌Ą─ĮŪ╔½╔ąŪę▓╗├„ĪŻBrevundimonasŻ©Č╠▓©å╬░¹Š·ī┘Ż®Š▀ėąĘ┤Ž§╗»─▄┴”Ż¼į┌MFC1ĪóMFC2ĪóMFC3ųąĄ─ŽÓī”žSČ╚Ęųäe×ķ2.10%Īó2.53%Īó4.36%Ż¼ūC├„┴╦Ę┤Ž§╗»╩ŪĻ¢śOĄ¬į┤╚ź│²Ą─═ŠÅĮų«ę╗ĪŻ
3ĪóĮYšō
1Ż®īó«aļŖŠ·S.oneidensisMR-1ęįė╬ļxæB┼c╣╠Č©╗»ą╬╩Į╝ė╚ļļp╩ęMFC═¼▓Į╠Ä└Ē─ŻöM▒ĮĘėųŲ╦ÄÅU╦«Ż¼S.oneidensisMR-1╝ė┐ņ┴╦ļŖūėé„▀f┼cč§╗»▀ĆįŁĘ┤æ¬╦┘┬╩Ż¼╠ß╔²┴╦ī”╬█╚Š╬’Ą─╠Ä└Ēą¦╣¹┼c░lļŖąį─▄Ż¼ī”MFCŽĄĮyŲĄĮ┴╦╔·╬’ÅŖ╗»ū„ė├Ż¼×ķÅU╦«ųą╬█╚Š╬’Ą─╚ź│²║═─▄į┤▐D╗»╠ß╣®┴╦ą┬╦╝┬ĘĪŻ
2Ż®╣╠Č©╗»╝Ü░¹ļp╩ęMFC«aļŖąį─▄┼c╬█╚Š╬’╚ź│²ą¦╣¹Š∙ā×ė┌ė╬ļxæB╝Ü░¹ļp╩ęMFCĪŻį┌3ų▄Ų┌Ą─▀B└m▀\ąąŽ┬Ż¼╣╠Č©╗»╝Ü░¹ļp╩ęMFCŽĄĮyĄ─ūŅ┤¾▌ö│÷ļŖē║ĪóūŅ┤¾╣”┬╩├▄Č╚ĪóŲĮŠ∙COD╚ź│²┬╩ĪóŲĮŠ∙Äņü÷ą¦┬╩Ęųäe×ķ633mVĪó582.7mW/m2Īó82.5%Īó26.6%Ż¼┼cė╬ļxæB╝Ü░¹ļp╩ęMFCŽÓ▒╚Ęųäe╠ß╔²┴╦18.7%Īó21.9%Īó10.9%Īó14.7%Ż¼╣╠Č©╗»╝Ü░¹╝╝ągŠ▀ėąį┌MFCųąīŹļHæ¬ė├Ą─Øō┴”ĪŻ
3Ż®╣╠Č©į┌ļp╩ęMFCĻ¢śOĄ─S.oneidensisMR-1┼cŽĄĮyųąįŁėąŠ·╚║ŲĄĮ┴╦ģf═¼ū„ė├Ż¼Ļ¢śO╔·╬’─ż╔ŽĖ╗╝»ĄĮ┤┘▀M░lļŖ┼cĄū╬’└¹ė├Ą─╗ņ║ŽŠ·╚║ĪŻ╬ó╔·╬’╚║┬õĮYśŗĮY╣¹’@╩ŠŻ¼╣╠Č©╗»╝Ü░¹ļp╩ęMFCĄ─Ļ¢śO╔·╬’─ż╔ŽļŖ╗Ņąį╝ÜŠ·┼c░lĮ═╝ÜŠ·Ą├ĄĮĖ╗╝»Ż¼ā×ä▌Š·ķT×ķProteobacteriaĪóBacteroidotaĪóFirmicutesĪóDesulfobacterotaŻ¼ā×ä▌Š·ī┘×ķDesulfovibrioĪóBacteroidesĪóClostridium_sensu_stricto_1ĪóGeobacterĪŻŻ©üĒį┤Ż║╔Ž║Żæ¬ė├╝╝ąg┤¾īW╗»īW┼cŁhŠ│╣ż│╠īWį║Ż®



