╚Š┴ŽÅU╦«▀M(j©¼n)╚ļ╦«¾wĪó═┴╚└Ż¼Ģ■(hu©¼)įņ│╔’ŗė├╦«į┤╬█╚ŠĪó╦«╔·╬’å╩╩¦╔·├³Īó╔·æB(t©żi)Š░ė^É║╗»ĪóŁh(hu©ón)Š│┘|(zh©¼)┴┐Ž┬ĮĄĄ╚å¢Ņ}Ż¼ī”(du©¼)╚╦ŅÉęį╝░Ųõ╦¹╔·╬’Ą─╔·┤µ«a(ch©Żn)╔·śO┤¾Ą─═■├{ĪŻ─┐Ū░│Żė├ė┌╠Ä└Ē╚Š┴ŽÅU╦«Ą─ĘĮĘ©ų„ę¬ėą╗»īW(xu©”)Ę©Īó╬’└Ē╗»īW(xu©”)Ę©║═╔·╬’Ę©Ą╚Ż¼Ųõųąęį╬’└Ē╗»īW(xu©”)Ę©ųąĄ─╬³ĖĮĘ©æ¬(y©®ng)ė├▒╚▌^ÅVĘ║ĪŻ╦«─²─zū„×ķę╗ĘNą┬ą═Ą─Ė▀Ęųūė╣”─▄▓─┴ŽŻ¼Ųõā╚(n©©i)▓┐║¼ėąČÓĘN╦«ąį╗∙łF(tu©ón)╚ń┴u╗∙Īó¶╚╗∙Ą╚Ż¼ŪęŠ▀ėąĖ▀┼“├ø▒Č┬╩Ż¼ī”(du©¼)╚Š┴ŽĮY(ji©”)Š¦ūŽ(crystalvioletŻ¼CV)Š▀ėą▌^ÅŖ(qi©óng)Ą─ĮY(ji©”)║Ž─▄┴”Ż¼╦«─²─z▓╗āHōĒėą┴╝║├Ą─ŠW(w©Żng)Įj(lu©░)ĮY(ji©”)śŗ(g©░u)Ż¼Č°Ūęį┌╦«ųą╚▄├øėų▓╗╚▄ė┌╦«Ż¼╦«─²─z╬³ĖĮ║¾śOęū┼cę║ŽÓĘųļxŻ¼║▄┤¾│╠Č╚╔Ž£p▌p║¾└m(x©┤)Ą─Ęųļx╣żū„Ż¼╩Ūę╗ĘN╩«Ęų└ĒŽļĄ─╬³ĖĮä®ĪŻĄ½╦«─²─z▒Š╔ĒÖC(j©®)ąĄÅŖ(qi©óng)Č╚▓╗Ė▀Ż¼ęūŲŲ╦ķŻ¼╗žė├▌^×ķ└¦ļyŻ¼Č°─Š┘|(zh©¼)╦žŠ▀ėąžSĖ╗Ą─╣┘─▄łF(tu©ón)ĮY(ji©”)śŗ(g©░u)Ż¼Ūęā”(ch©│)┴┐žSĖ╗Īó│╔▒ŠĄ═ĪóŁh(hu©ón)Š│ėč║├║═┐╔╔·╬’ĮĄĮŌŻ¼▒╗ęĢ×ķ└ĒŽļĄ─ėąÖC(j©®)Š█║Ž╬’ĮMĘųĪŻėąčąŠ┐▒Ē├„Ż¼į┌╦«─²─zųąę²╚ļ─Š┘|(zh©¼)╦žŅÉŠ█║Ž╬’Ż¼┐╔ęįą╬│╔╗ź┤®ŠW(w©Żng)Įj(lu©░)ĮY(ji©”)śŗ(g©░u)Ż¼į÷╝ė╬³ĖĮ╬╗³c(di©Żn)Ż¼▀M(j©¼n)Č°ėąą¦╠ßĖ▀ŲõÖC(j©®)ąĄÅŖ(qi©óng)Č╚║═╬³ĖĮą¦┬╩ĪŻ×ķ┴╦╠ßĖ▀╬³ĖĮ▓─┴ŽĄ─╗ž╩š└¹ė├ąįŻ¼į┌╬³ĖĮ▓─┴Žųąę²╚ļ┤┼ąį╬ó┴ŻŻ¼ą╬│╔┤┼ąį╬³ĖĮ▓─┴ŽŻ¼═Ō╝ė┤┼ł÷(ch©Żng)╝┤┐╔īóŲõĘųļxŻ¼Ūę╝ė╚ļ┤┼ąį╬ó┴Ż║¾Ż¼į÷┤¾┴╦╬³ĖĮ䮥─╗Ņąį╬╗³c(di©Żn)║═▒╚▒Ē├µĘeŻ¼Å─Č°Ė³ėą└¹ė┌╬³ĖĮ▓─┴ŽĄ─╬³ĖĮ▀^│╠ĪŻ
ę“┤╦Ż¼▒ŠčąŠ┐═©▀^ūįė╔╗∙Įėų”╣▓Š█║═įŁ╬╗│┴ĄĒĘ©ųŲéõ┤┼ąį─Š┘|(zh©¼)╦ž╗Ū╦ßŌc╦«─²─z(Fe3O4@LS)Ż¼╠ĮŠ┐į┌Ė„ĘNå╬ę“╦žŚl╝■Ž┬Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮąį─▄Ż¼▓ó▀M(j©¼n)ąą╬³ĖĮäė(d©░ng)┴”īW(xu©”)║═╬³ĖĮĄ╚£žŠĆöM║ŽĘų╬÷Ż¼┐╝▓ņŲõį┘╔·ąį─▄║═╣▓┤µļxūėī”(du©¼)╬³ĖĮąį─▄Ą─ė░ĒæŻ¼▓óī”(du©¼)Fe3O4@LSĄ─╬³ĖĮÖC(j©®)└Ē▀M(j©¼n)ąą┴╦Ęų╬÷ĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 īŹ(sh©¬)“×(y©żn)▓─┴Ž
─Š┘|(zh©¼)╦ž╗Ū╦ßŌc(LS)║═N,NĪ»-üå╝ū╗∙ļp▒¹Ž®§Ż░Ę(MBA)Š∙┘Å(g©░u)ūį╠ņĮ“╩ą╣ŌÅ═(f©┤)Š½╝Ü(x©¼)╗»╣żčąŠ┐╦∙Ż¼▒¹Ž®§Ż░Ę(AM)┘Å(g©░u)ūį╠ņĮ“╩ą┐Ų├▄ÜW╗»īW(xu©”)įćä®ėąŽ▐╣½╦ŠŻ¼▀^┴“╦ßŌø(KPS)┘Å(g©░u)ūį╠ņĮ“╩ą▒▒┬ō(li©ón)Š½╝Ü(x©¼)╗»īW(xu©”)ŲĘķ_░l(f©Ī)ėąŽ▐╣½╦ŠŻ¼N,N,NĪ»,NĪ»-╦─ęę╗∙ęęČ■░Ę(TEMED)┘Å(g©░u)ūį╠▌ŽŻÉ█(╔Ž║Ż)╗»│╔╣żśI(y©©)░l(f©Ī)š╣ėąŽ▐╣½╦ŠŻ¼ęį╔Žįćä®╝āČ╚Įį×ķĘų╬÷╝āĪŻ
1.2 ▓─┴ŽųŲéõ╝░ĮY(ji©”)śŗ(g©░u)▒Ēš„
ĘQ╚Ī0.400g─Š┘|(zh©¼)╦ž╗Ū╦ßŌc(LS)Īó1.400g▒¹Ž®§Ż░Ę(AM)║═0.024gĮ╗┬ō(li©ón)ä®(MBA)Ę┼╚ļ¤²▒Łųą╝ė╚ļ20mLš¶s╦«Ż¼╩ę£žŽ┬öć░Ķ╚▄ĮŌŻ╗ĘQ╚Ī0.220g▀^┴“╦ßŌø(KPS)╝ė╚ļ10mLš¶s╦«┼õųŲ│╔╚▄ę║Ę┼╚ļ┴Ē═Ōę╗éĆ(g©©)¤²▒ŁųąĪŻ40ĪµŽ┬ŅA(y©┤)¤ß10min║¾Ż¼īó2éĆ(g©©)¤²▒ŁĄ─╚▄ę║╗ņ║Žōuä“Ż¼╝ė╚ļ0.050mL┤▀╗»ä®(TEMED)Ż¼öć░ĶŠ∙ä“║¾┐ņ╦┘Ą╣╚ļ─ŻŠ▀Ż¼į┌40ĪµŽ┬Š█║Ž10min║¾Ż¼Ą├ĄĮ─Š┘|(zh©¼)╦ž╦«─²─zĪŻŽ┤ā¶║¾Ż¼īó╦«─²─zų├ė┌ę╗Č©▒╚└²╗ņ║ŽĄ─FeSO4Īż7H2O║═FeCl3Īż6H2O(1:1.4)╗ņ║Ž╚▄ę║ųąĮ■┼▌8hŻ¼Ž┤╚ź▒Ē├µ╚▄ę║║¾Ż¼ų├ė┌50mL1molĪżL−1NaOH╚▄ę║ųąĮ■┼▌8hŻ¼Ą├ĄĮ┤┼ąį╦«─²─zFe3O4@LSĪŻŽ┤ā¶║¾į┌60Īµ║µŽõųą║µĖ╔ų┴║ŃųžŻ¼éõė├ĪŻģó┐╝▒ŠšnŅ}ĮMŪ░Ų┌ĻP(gu©Īn)ė┌Fe3O4@LSĄ─▒Ēš„ĮY(ji©”)╣¹Ż¼ī”(du©¼)Fe3O4@LSĄ─ĮY(ji©”)śŗ(g©░u)▀M(j©¼n)ąąĘų╬÷ĪŻ
1.3 ▓─┴Ž╬³ĖĮąį─▄īŹ(sh©¬)“×(y©żn)
į┌Fe3O4@LS╬³ĖĮĮY(ji©”)Š¦ūŽ(CV)─ŻöMÅU╦«īŹ(sh©¬)“×(y©żn)ųąŻ¼▓╔ė├Ęų╣Ō╣ŌČ╚Ę©£y(c©©)Č©583nm╠ÄĄ─╬³╣ŌČ╚AŻ¼└¹ė├ś╦(bi©Īo)£╩(zh©│n)Ū·ŠĆĘĮ│╠A=0.04259+0.25801C(R2=0.99908)ėŗ(j©¼)╦Ń╠Ä└Ē║¾╦«ųą╩ŻėÓCV┘|(zh©¼)┴┐ØŌČ╚ĪŻ
╠ĮŠ┐žō(f©┤)▌d┤┼ąįŪ░║¾ī”(du©¼)╬³ĖĮCVĄ─ė░ĒæŻ╗īó0.05gĖ╔Fe3O4@LS╚▄├ø║¾╝ė╚ļ▓╗═¼pH(3Īó4Īó5Īó6Īó7Īó8Īó9Īó10)Ą─50mLCV(50mgĪżL−1)╚▄ę║ųąŻ¼╠ĮŠ┐╚▄ę║pHī”(du©¼)╬³ĖĮĄ─ė░ĒæŻ╗īó0.05gĖ╔Fe3O4@LS╚▄├ø║¾═Č╚ļ50mL50mgĪżL−1CV╚▄ę║ųąŻ¼į┌▓╗═¼Ģr(sh©¬)ķg£y(c©©)Č©CV╩ŻėÓØŌČ╚Ż¼╠ĮŠ┐╬³ĖĮĢr(sh©¬)ķgī”(du©¼)╬³ĖĮĄ─ė░ĒæŻ╗īó▓╗═¼┘|(zh©¼)┴┐Ą─Fe3O4@LS═Č╚ļ50mL50mgĪżL−1CV╚▄ę║ųąŻ¼╠ĮŠ┐╬³ĖĮä®ė├┴┐ī”(du©¼)╬³ĖĮĄ─ė░ĒæŻ╗īó0.02gĖ╔Fe3O4@LS╚▄├ø║¾═Č╚ļ▓╗═¼ØŌČ╚Ą─CV╚▄ę║ųąŻ¼╠ĮŠ┐CV│§╩╝ØŌČ╚ī”(du©¼)╬³ĖĮĄ─ė░ĒæĪŻīó0.02gĖ╔Fe3O4@LS╚▄├ø║¾═Č╚ļ50mL100mgĪżL−1CV╚▄ę║ųąŻ¼į┌▓╗═¼£žČ╚Ž┬▀M(j©¼n)ąą╬³ĖĮŻ¼╠ĮŠ┐╬³ĖĮ£žČ╚ī”(du©¼)╬³ĖĮĄ─ė░ĒæĪŻęį╔Ž├┐éĆ(g©©)öĄ(sh©┤)ō■(j©┤)³c(di©Żn)ū÷3┤╬īŹ(sh©¬)“×(y©żn)Ż¼╚ĪŲĮŠ∙ųĄĪŻ
╬³ĖĮäė(d©░ng)┴”īW(xu©”)Ż║╚ĪFe3O4@LSų├ė┌100mLŠ▀╚¹ÕFą╬Ų┐ųąŻ¼Ęųäe╝ė╚ļ50mLØŌČ╚×ķ25Īó50Īó100mgĪżL−1Ą─CV╚▄ę║Ż¼į┌298KŽ┬Ż¼ęį150rĪżmin−1į┌║Ń£ž╦«įĪš±╩ÄŲ„ųąš±╩Ä╬³ĖĮŻ¼├┐Ė¶ę╗Č╬Ģr(sh©¬)ķg╚Ī╔ŽīėŪÕę║£y(c©©)Č©╬³╣ŌČ╚ęįėŗ(j©¼)╦ŃØŌČ╚Ż¼├┐éĆ(g©©)öĄ(sh©┤)ō■(j©┤)³c(di©Żn)ū÷3┤╬īŹ(sh©¬)“×(y©żn)Ż¼╚ĪŲĮŠ∙ųĄĪŻ▀xō±öMę╗ļA(╩Į(1))ĪóöMČ■ļA(╩Į(2))ęį╝░ā╚(n©©i)öU(ku©░)╔óäė(d©░ng)┴”īW(xu©”)─Żą═(╩Į(3))▀M(j©¼n)ąąöM║ŽĪŻ

╩ĮųąŻ║t×ķ╬³ĖĮĢr(sh©¬)ķgŻ¼minŻ╗Qt║═QeĘųäe┤·▒Ē╬³ĖĮĢr(sh©¬)ķg×ķt║═╬³ĖĮŲĮ║ŌĢr(sh©¬)Ą─╬³ĖĮ┴┐Ż¼mgĪżg−1Ż╗k1×ķöMę╗╝ē(j©¬)Ę┤æ¬(y©®ng)╦┘┬╩│ŻöĄ(sh©┤)Ż¼min−1Ż╗k2×ķöMČ■╝ē(j©¬)Ę┤æ¬(y©®ng)╦┘┬╩│ŻöĄ(sh©┤)Ż¼gĪż(mgĪżmin)−1Ż╗ki×ķ┴Żūėā╚(n©©i)öU(ku©░)╔ó╦┘┬╩│ŻöĄ(sh©┤)Ż¼mgĪżg−1Īżmin−0.5Ż╗P×ķ┼c▀ģĮńīė║±Č╚ŽÓĻP(gu©Īn)Ą─│ŻöĄ(sh©┤)ĪŻ═©▀^ęįī”(du©¼)tū„łDŻ¼k1║═QeĄ─ųĄĘųäeī”(du©¼)æ¬(y©®ng)×ķą▒┬╩║═ĮžŠÓŻ╗k2║═Qe┐╔ęįė╔t/Qtī”(du©¼)tū„łDŻ¼═©▀^öM║ŽŪ·ŠĆĄ─ĮžŠÓ║═ą▒┬╩ėŗ(j©¼)╦Ń╦∙Ą├ĪŻ
╬³ĖĮĄ╚£žŠĆŻ║╚Ī50mL│§╩╝ØŌČ╚×ķ50~500mgĪżL−1Ą─CV╚▄ę║ų├ė┌ę╗ŽĄ┴ąśėŲĘŲ┐ųąŻ¼▓óš{(di©żo)╣Ø(ji©”)╚▄ę║pH×ķ7Ż¼╝ė╚ļFe3O4@LSŻ¼Ęųäeį┌298Īó318Īó338K£žČ╚Ž┬ęį150rĪżmin−1į┌║Ń£ž╦«įĪš±╩ÄŲ„ųąš±╩Ä╬³ĖĮ2hĪŻė├┤┼ĶFĘųļxFe3O4@LSŻ¼£y(c©©)Č©╬³╣ŌČ╚ėŗ(j©¼)╦ŃØŌČ╚ĪŻ├┐éĆ(g©©)öĄ(sh©┤)ō■(j©┤)³c(di©Żn)ū÷3┤╬īŹ(sh©¬)“×(y©żn)Ż¼╚ĪŲĮŠ∙ųĄĪŻ▓╔ė├Langmuir(╩Į(4))ĪóFreundlich(╩Į(5))║═Temkin(╩Į(6))▀@3ĘN╬³ĖĮĄ╚£žŠĆ─Żą═ī”(du©¼)īŹ(sh©¬)“×(y©żn)╦∙Ą├öĄ(sh©┤)ō■(j©┤)▀M(j©¼n)ąąöM║ŽĪŻ

╩ĮųąŻ║Ce×ķ╬³ĖĮŲĮ║ŌĢr(sh©¬)╚▄ę║ųąCVĄ─ØŌČ╚Ż╗Qm×ķ’¢║═╬³ĖĮ┴┐Ż¼mgĪżg−1Ż╗KL×ķ╬³ĖĮŽĄöĄ(sh©┤)Ż¼LĪżmg−1Ż╗KF║═nŠ∙×ķ│ŻöĄ(sh©┤)Ż¼n>1Ģr(sh©¬)Ż¼╬³ĖĮ×ķęū╬³ĖĮ▀^│╠Ż╗”┴║═”┬Š∙×ķ│ŻöĄ(sh©┤)ĪŻęįCe/Qeī”(du©¼)Ceū„łDŻ¼Qm║═KL×ķĄ─ųĄĘųäeī”(du©¼)æ¬(y©®ng)×ķĮžŠÓ║═ą▒┬╩Ż╗KF║═nĄ─ųĄ┐╔ęį═©▀^lnQeī”(du©¼)lnCeū„łDŻ¼═©▀^öM║ŽŪ·ŠĆĄ─ĮžŠÓ║═ą▒┬╩ėŗ(j©¼)╦Ń╦∙Ą├ĪŻ
×ķĖ³▀M(j©¼n)ę╗▓Į蹊┐╬³ĖĮĄ─¤ß┴”īW(xu©”)ąį┘|(zh©¼)Ż¼▓╔ė├ĘČ╠ž╗¶Ę“ĘĮ│╠║═Gibbs-HelmhotzĘĮ│╠ėŗ(j©¼)╦Ń│÷▓╗═¼£žČ╚Ž┬Ą─╝¬▓╝╦╣ūįė╔─▄(╩Į(7))Īóņ╩ūā(╩Į(8))║═ņžūā(╩Į(9))ĪŻ

╩ĮųąŻ║∆G×ķ╝¬▓╝╦╣ūįė╔─▄kJĪżmol−1Ż╗∆H×ķņ╩ūāŻ¼kJĪżmol−1Ż╗∆S×ķņžūāŻ¼JĪż(molĪżK)−1Ż╗R×ķÜŌ¾w│ŻöĄ(sh©┤)Ż¼8.314JĪż(molĪżK)−1Ż╗T×ķĮ^ī”(du©¼)£žČ╚Ż¼KŻ╗KL×ķŲĮ║Ō│ŻöĄ(sh©┤)Ż¼LĪżg−1ĪŻ┐╔ė╔ln(Qe/Ce)ī”(du©¼)Qe▀M(j©¼n)ąąöM║ŽŻ¼ĮžŠÓ×ķlnKLŻ¼═©▀^lnKLī”(du©¼)1/Tū„łDŻ¼∆H║═∆SĘųäeī”(du©¼)æ¬(y©®ng)×ķą▒┬╩║═ĮžŠÓĪŻ
┤┼ąį─▄║═ĮŌ╬³į┘╔·ąį─▄Ż║▓╔ė├├└ć°(gu©«)LakeShore╣½╦ŠĄ─VSM7307ą═š±äė(d©░ng)śėŲĘ┤┼ÅŖ(qi©óng)ėŗ(j©¼)▀M(j©¼n)ąąFe3O4@LS║═Fe3O4Ą─┤┼ąį─▄£y(c©©)Č©ĪŻį┌ūŅ╝čĄ─╬³ĖĮŚl╝■Ž┬Ż¼īóę╗Č©┴┐Fe3O4@LS╚▄├ø║¾═Č╚ļ50mL100mgĪżL−1CV╚▄ę║ųąŻ¼š{(di©żo)╣Ø(ji©”)pH=7Ż¼į┌298KŽ┬║Ń£žš±╩Ä╬³ĖĮ2h║¾Ż¼╚Ī│÷Ż¼ė├╚źļxūė╦«Ž┤ā¶Ż¼ų├ė┌50mL¤o╦«ęę┤╝╗“0.1molĪżL−1Ą─NaOHųąŻ¼ņoų├ĮŌ╬³5hŻ¼Ž┤£ņŻ¼Ė╔į’ĪŻ▀B└m(x©┤)▀M(j©¼n)ąąöĄ(sh©┤)┤╬╬³ĖĮ-ĮŌ╬³īŹ(sh©¬)“×(y©żn)üĒ╠ĮŠ┐Fe3O4@LS╦«─²─zĄ─į┘╔·ąį─▄ĪŻ
1.4 ╣▓┤µļxūėė░ĒæīŹ(sh©¬)“×(y©żn)
┼õųŲę╗ŽĄ┴ą║¼ėą▓╗═¼Na+ĪóK+ĪóCa2+ĪóMg2+ļxūėÅŖ(qi©óng)Č╚Ą─CV╗ņ║Ž╚▄ę║Ż¼▒Ż│ųCVØŌČ╚×ķ100mgĪżL−1ĪŻ╚Ī╗ņ║Ž╚▄ę║50mLŻ¼š{(di©żo)╣Ø(ji©”)╚▄ę║pH=6Ż¼═Č╝ė0.05gFe3O4@LSŻ¼į┌25Īµ║Ń£ž╦«įĪųąęį150rĪżmin−1Ą─▐D(zhu©Żn)╦┘š±╩Ä╬³ĖĮ2hŻ¼£y(c©©)Č©╚▄ę║ųąCVĄ─║¼┴┐Ż¼├┐éĆ(g©©)öĄ(sh©┤)ō■(j©┤)³c(di©Żn)ū÷ČÓ┤╬īŹ(sh©¬)“×(y©żn)Ż¼╚ĪĄ├ŲĮŠ∙ųĄĘųäeėŗ(j©¼)╦Ń╬³ĖĮ┴┐ĪŻ
2ĪóĮY(ji©”)╣¹┼cėæšō
2.1 ĮY(ji©”)śŗ(g©░u)▒Ēš„Ęų╬÷
ė╔▒ŠšnŅ}ĮMŪ░Ų┌蹊┐│╔╣¹┐╔ų¬Ż¼Fe3O4─▄ē“│╔╣”žō(f©┤)▌dĄĮLS╔ŽŻ¼Ūęį┌žō(f©┤)▌d▀^│╠ųąŻ¼Fe3O4Ą─Š¦¾wĮY(ji©”)śŗ(g©░u)╬┤░l(f©Ī)╔·Ė─ūāĪŻį┌╬³ĖĮ▀^│╠ųąŻ¼Fe3O4ę▓┐╔ęįū„×ķ╬³ĖĮ䮥─╗Ņąį╬╗³c(di©Żn)Ż¼ę“┤╦Ż¼╦«─²─z│╔╣”žō(f©┤)▌dį┌Fe3O4╔Ž║¾Ż¼╗Ņąį╬╗³c(di©Żn)į÷╝ėŻ¼╩╣Ą├Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮąį─▄┤¾┤¾╠ßĖ▀ĪŻFe3O4@LS│╩¼F(xi©żn)╚²ŠS┴ó¾wČÓ┐ūĮY(ji©”)śŗ(g©░u)Ż¼×ķĘų▓╝▌^ęÄ(gu©®)š¹Ą─ĘõĖCĀŅ┐ūČ┤Ż¼▀@ą®ĮY(ji©”)śŗ(g©░u)ėą└¹ė┌╗Ņąį╬╗³c(di©Żn)Ą─▒®┬ČŻ¼▀M(j©¼n)Č°╠ßĖ▀╬³ĖĮ䮥─╬³ĖĮąį─▄ĪŻė╔BET▒Ēš„ĮY(ji©”)╣¹(▒Ē1)┐╔ęŖŻ¼Fe3O4@LS▓─┴ŽŠ▀ėąĮķ┐ūĮY(ji©”)śŗ(g©░u)Ż¼Fe3O4@LSĄ─▒╚▒Ē├µĘe×ķ3.6692m2Īżg−1Ż¼Ė▀ė┌LSĄ─▒╚▒Ē├µĘe(2.3422m2Īżg−1)ĪŻ▀@▒Ē├„╦«─²─zžō(f©┤)▌dFe3O4║¾Ż¼Fe3O4@LSĄ─▒╚▒Ē├µĘeį÷┤¾Ż¼ėą└¹ė┌╠ßĖ▀╬³ĖĮą¦┬╩ĪŻę“┤╦Ż¼Fe3O4į┌Fe3O4@LSųą┐╔╠ß╣®┤¾┴┐Ą─╗Ņąį╬╗³c(di©Żn)Ż¼▓óŪęFe3O4@LS▒Š╔ĒĄ─▌^┤¾▒╚▒Ē├µĘe╩╣Ą├╗Ņąį╬╗³c(di©Żn)Ė³╚▌ęū▒®┬ČŻ¼▀@ą®╠ž³c(di©Żn)┐╔╩╣Ą├Fe3O4@LSį┌╬³ĖĮ▀^│╠ųąš╣¼F(xi©żn)│÷▌^║├Ą─╬³ĖĮą¦╣¹ĪŻ
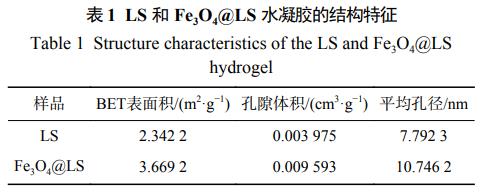
2.2 ╬³ĖĮąį─▄▒╚▌^
ė╔łD1(a)┐╔ęį┐┤│÷Ż¼į┌═¼Ą╚īŹ(sh©¬)“×(y©żn)Śl╝■Ž┬Ż¼«ö(d©Īng)Fe3O4žō(f©┤)▌dĄĮ╦«─²─z╔Ž║¾(Fe3O4@LS)Ż¼¤ošō╩Ūī”(du©¼)CVĄ─╬³ĖĮ┴┐▀Ć╩Ū╚ź│²┬╩Š∙├„’@Ė▀ė┌LSĪŻė╔łD1(b)┐╔ęį┐┤│÷Ż¼Fe3O4@LSĄ─╚▄├ø┬╩├„’@Ė▀ė┌LSĪŻī¦(d©Żo)ų┬2ĘN╬³ĖĮä®╬³ĖĮąį─▄▓Ņ«ÉĄ─įŁę“į┌ė┌Ż¼Fe3O4@LSĄ─ā╚(n©©i)▓┐ėąFe3O4╝{├ū┴ŻūėŻ¼Č°Fe3O4╝{├ū┴Żūėį┌╠ß╣®╗Ņąį╬╗³c(di©Żn)Ą─═¼Ģr(sh©¬)▀M(j©¼n)Č°į÷╝ėā╚(n©©i)▓┐ĮY(ji©”)śŗ(g©░u)Ą─┐ūŽČŻ¼╩╣Ą├Ųõ╚▄├ø┬╩Ė³Ė▀Ż¼╚▄├ø║¾Ą─¾wĘeĖ³┤¾Ż¼▒Ē├µĘeę▓ļSų«ūā┤¾Ż¼▀M(j©¼n)Č°╠ßĖ▀╬³ĖĮąį─▄ĪŻ
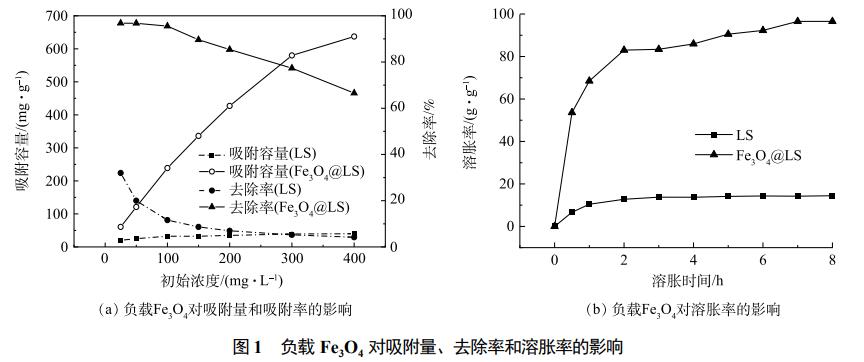
pHī”(du©¼)╬³ĖĮCVĄ─ė░ĒæĮY(ji©”)╣¹╚ńłD2(a)╦∙╩ŠĪŻ«ö(d©Īng)pHė╔3╔Ž╔²ĄĮ7Ģr(sh©¬)Ż¼╬³ĖĮ╚▌┴┐║═CVĄ─╚ź│²┬╩Š∙čĖ╦┘╔Ž╔²Ż¼╚ź│²┬╩į┌pH=7Ģr(sh©¬)▀_(d©ó)ĄĮūŅ┤¾ųĄŻ¼×ķ96.68%Ż╗«ö(d©Īng)pH└^└m(x©┤)╔²Ė▀Ż¼Fe3O4@LSī”(du©¼)CVĄ─╚ź│²┬╩║═╬³ĖĮ┴┐ūā╗»▓╗┤¾ĪŻ«ö(d©Īng)pH┤¾ė┌11Ģr(sh©¬)Ż¼CVĢ■(hu©¼)╔·│╔ūŽ╔½ą§ĀŅ│┴ĄĒĪŻę“┤╦Ż¼▓╗┐╝æ]▀^Ė▀Ą─pHī”(du©¼)CV╬³ĖĮĄ─ė░ĒæĪŻėąčąŠ┐▒Ē├„Ż¼Fe3O4@LSĄ─ZetaļŖ╬╗Ą─Ą╚ļŖ╬╗³c(di©Żn)╝s×ķ3.2ĪŻ«ö(d©Īng)pH3.2Ģr(sh©¬)Ż¼Fe3O4@LS▒Ē├µĄ─ļŖžō(f©┤)ąįį÷ÅŖ(qi©óng)Ż¼▓─┴Ž▒Ē├µ┼cCVų«ķgę▓Ģ■(hu©¼)«a(ch©Żn)╔·ņoļŖ╬³ę²┴”Ż¼Å─Č°┐╔į÷╝ė╬³ĖĮ╚▌┴┐ĪŻĄ½«ö(d©Īng)pH▌^Ą═Ģr(sh©¬)Ż¼╬³ĖĮą¦╣¹▌^▓ŅŻ¼įŁę“╩Ū╬³ĖĮ䮥─▒Ē├µ╣┘─▄łF(tu©ón)▒╗┘|(zh©¼)ūė╗»Ż¼Å─Č°Ž„╚§┴╦╬³ĖĮä®┼cCVĄ─“³║Žū„ė├ĪŻ═¼Ģr(sh©¬)Ż¼╚▄ę║ųą┤¾┴┐Ą─H+Ģ■(hu©¼)┼cCVą╬│╔Ėé(j©¼ng)ĀÄ(zh©źng)ąį╗Ņąį╬╗³c(di©Żn)Ż¼ī”(du©¼)CVĄ─╬³ĖĮėąęųųŲū„ė├ĪŻ┴Ē═ŌŻ¼Fe3O4@LSį┌╦ßąįŚl╝■Ž┬¾wĘeĢ■(hu©¼)╩š┐sŻ¼ī¦(d©Żo)ų┬▒Ē├µĘeūāąĪŻ¼┐ūŽČ£p╔┘ĪŻę“┤╦Ż¼Fe3O4@LSį┌╦ßąįŚl╝■Ž┬ī”(du©¼)CVĄ─╬³ĖĮą¦╣¹▌^▓ŅĪŻļSų°pHĄ─į÷╝ėŻ¼Fe3O4@LS▒Ē├µĄ─╣┘─▄łF(tu©ón)ųØu╚ź┘|(zh©¼)ūė╗»Ż¼╚▄ę║ųąĄ─H+£p╔┘Ż¼Fe3O4@LSĄ─¾wĘe▓╗į┘╩▄ė░ĒæĪŻH+ī”(du©¼)╗Ņąį╬╗³c(di©Żn)Ėé(j©¼ng)ĀÄ(zh©źng)Ą─ė░Ēæ£p╚§Ż¼ŽÓī”(du©¼)╗Ņąį╬╗³c(di©Żn)į÷╝ėĪŻÅ─Č°╠ßĖ▀┴╦ī”(du©¼)CVĄ─╬³ĖĮ─▄┴”ĪŻ
ė╔łD2(b)┐╔ęį┐┤│÷Ż¼╬³ĖĮ30minFe3O4@LSī”(du©¼)CV╚ź│²┬╩┐╔▀_(d©ó)90%ęį╔ŽŻ¼į┌╬³ĖĮĄ─│§╩╝ļAČ╬Ż¼Fe3O4@LS╠ß╣®┴╦│õūŃĄ─╬³ĖĮ╬╗³c(di©Żn)Ż¼CVėą▌^Ė▀Ą─Ė┼┬╩┼cFe3O4@LSųąĄ─▒ŖČÓ╗Ņąį╬╗³c(di©Żn)ėąą¦Įėė|ĪŻį┌80minęį║¾Ż¼╬³ĖĮ╗∙▒Š▀_(d©ó)ĄĮŲĮ║ŌŻ¼Fe3O4@LSī”(du©¼)CVĄ─╚ź│²┬╩║═╬³ĖĮ╚▌┴┐╗∙▒Š▓╗į┘░l(f©Ī)╔·ūā╗»Ż¼Fe3O4@LS▒Ē├µĄ─╗Ņąį╬╗³c(di©Żn)┤¾ČÓöĄ(sh©┤)Š∙ęč▒╗š╝ō■(j©┤)Ż¼CV┼c╬³ĖĮ╬╗³c(di©Żn)Ą─Įėė|Ė┼┬╩┤¾Ę∙Č╚ĮĄĄ═Ż¼Å─Č°╩╣╬³ĖĮ▀^│╠ūāĄ├ŠÅ┬²ĪŻ
ė╔łD2(c)┐╔ų¬Ż¼Fe3O4@LSī”(du©¼)ĮY(ji©”)Š¦ūŽĄ─╚ź│²┬╩ļSFe3O4@LS═Č╝ė┴┐Ą─į÷╝ėČ°į÷┤¾ĪŻ«ö(d©Īng)Fe3O4@LS═Č╝ė┴┐×ķ400mgĪżL−1Ģr(sh©¬)Ż¼╚ź│²┬╩▀_(d©ó)ĄĮ94%ęį╔ŽŻ¼▓óŪę┤╦Ģr(sh©¬)Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┴┐┐╔▀_(d©ó)127.4mgĪżg−1ĪŻ┤╦║¾į┘į÷┤¾Fe3O4@LS═Č╝ė┴┐Ż¼╚ź│²┬╩Ą─į÷╝ė┌ģä▌(sh©¼)▓╗├„’@Ż¼╬³ĖĮ┴┐┤¾Ę∙Č╚Ž┬ĮĄĪŻŲõįŁę“┐╔─▄╩Ū«ö(d©Īng)CVØŌČ╚ę╗Č©Ģr(sh©¬)Ż¼Fe3O4@LS═Č╝ė┴┐įĮ┤¾Ż¼┐╔╠ß╣®╬³ĖĮĄ─╗Ņąį╬╗³c(di©Żn)į÷ČÓŻ¼ī”(du©¼)╦«ųąCVĄ─╚ź│²┬╩įĮ┤¾Ż╗Ą½▀^┴┐Ą─Fe3O4@LSĢ■(hu©¼)╩╣Fe3O4@LSųž»B╗“Š█║Žī¦(d©Żo)ų┬─▄└¹ė├Ą─▒Ē├µĘe║═ėąą¦Ą─╬³ĖĮ╗Ņąį╬╗³c(di©Żn)ŽÓæ¬(y©®ng)£p╔┘Ż¼Č°Ūęå╬╬╗┘|(zh©¼)┴┐╬³ĖĮä®╦∙╬³ĖĮĄ─CV┐é┴┐ę▓Ģ■(hu©¼)ĮĄĄ═ĪŻ
╚ńłD2(d)╦∙╩ŠŻ¼Fe3O4@LSĄ─╚ź│²┬╩ļSCV│§╩╝ØŌČ╚╔²Ė▀Č°Ž┬ĮĄŻ¼╬³ĖĮ┴┐ļS│§╩╝ØŌČ╚╔²Ė▀Č°╔Ž╔²ĪŻį┌CV×ķ100mgĪżL−1Ą─ŪķørŽ┬Ż¼CVļxūė┼c╬³ĖĮä®▒Ē├µĄ─╬³ĖĮ╬╗³c(di©Żn)Įėė|Ą─Ė┼┬╩į÷╝ėŻ¼Š▀ėą▌^Ė▀Ą─╚ź│²┬╩ĪŻCVØŌČ╚│ų└m(x©┤)╔Ž╔²Ģr(sh©¬)Ż¼CV┼cFe3O4@LS▒Ē├µĄ─╗Ņąį╬╗³c(di©Żn)Įėė|Ė┼┬╩į÷╝ėŻ¼╬³ĖĮ┴┐į÷╝ėŻ¼Ą½ė╔ė┌Fe3O4@LSĄ─┴┐ę╗Č©Ż¼ī¦(d©Żo)ų┬Ųõ▒Ē├µĄ─╬³ĖĮ╬╗³c(di©Żn)ėąŽ▐Ż¼CVØŌČ╚╔Ž╔²Ģr(sh©¬)é„┘|(zh©¼)ūĶ┴”╠ßĖ▀ĪŻ╬³ĖĮę▓ųØu┌ģė┌’¢║═ĪŻ
ė╔łD2(e)┐╔ų¬Ż¼Ę┤æ¬(y©®ng)£žČ╚ī”(du©¼)ė┌Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮė░Ēæ▓╗┤¾Ż¼į┌25ĪµĢr(sh©¬)Ż¼╬³ĖĮ┴┐▀_(d©ó)ĄĮ237.08mgĪżg−1Ż¼«ö(d©Īng)£žČ╚╔²Ė▀Ģr(sh©¬)Ż¼╚ź│²┬╩║═╬³ĖĮ┴┐Š∙│÷¼F(xi©żn)┬į╬óĮĄĄ═┌ģä▌(sh©¼)ĪŻę“?y©żn)ķ┤┼ąį╦«─²─zī”(du©¼)ĮY(ji©”)Š¦ūŽĄ─╬³ĖĮ╩ŪĘ┼¤ß▀^│╠Ż¼ļSų°£žČ╚╔²Ė▀Ż¼▓┐Ęų┤┼ąį╦«─²─z┐╔─▄│÷¼F(xi©żn)├ōĖĮŻ¼╩╣CVĄ─╬³ĖĮ┴┐ĮĄĄ═ĪŻ
2.3 ╬³ĖĮäė(d©░ng)┴”īW(xu©”)
▀xō±öMę╗ļAĪóöMČ■ļAęį╝░ā╚(n©©i)öU(ku©░)╔óäė(d©░ng)┴”īW(xu©”)─Żą═ķ_š╣╬³ĖĮäė(d©░ng)┴”īW(xu©”)蹊┐Ż¼ŲõųąöMę╗ļAäė(d©░ng)┴”īW(xu©”)╩Ū╝┘įO(sh©©)Ųõ╬³ĖĮ╩▄ĄĮöU(ku©░)╔ó▓Į¾EĄ─┐žųŲŻ╗öMČ■ļAäė(d©░ng)┴”īW(xu©”)─Żą═╩Ū╝┘įO(sh©©)╬³ĖĮ╦┘┬╩ė╔╬³ĖĮä®▒Ē├µ╬┤▒╗š╝ėąĄ─╬³ĖĮ┐š╬╗öĄ(sh©┤)─┐Ą─ŲĮĘĮųĄøQČ©Ż¼╬³ĖĮ▀^│╠╩▄╗»īW(xu©”)╬³ĖĮÖC(j©®)└ĒĄ─┐žųŲŻ¼▀@ĘN╗»īW(xu©”)╬³ĖĮ╔µ╝░ĄĮ╬³ĖĮä®┼c╬³ĖĮ┘|(zh©¼)ų«ķgĄ─ļŖūė╣▓ė├╗“ļŖūė▐D(zhu©Żn)ęŲŻ╗Č°ā╚(n©©i)öU(ku©░)╔óät├Ķ╩÷╬³ĖĮ┘|(zh©¼)į┌Ņw┴Żā╚(n©©i)▓┐öU(ku©░)╔óĄ─▀^│╠ĪŻ
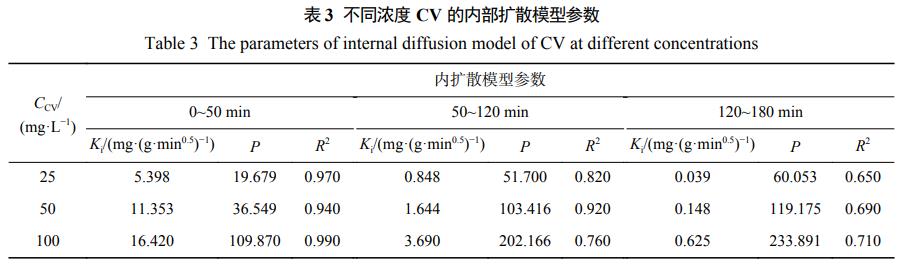
Ė∙ō■(j©┤)╩Į(1)Īó╩Į(2)Īó╩Į(3)ī”(du©¼)īŹ(sh©¬)“×(y©żn)╦∙Ą├öĄ(sh©┤)ō■(j©┤)▀M(j©¼n)ąąöM║ŽŻ¼öM║ŽĄ─äė(d©░ng)┴”īW(xu©”)ģóöĄ(sh©┤)╚ń▒Ē2Īó▒Ē3╦∙╩ŠĪŻį┌3ĘN▓╗═¼CVØŌČ╚Ž┬Ż¼ī”(du©¼)ė┌Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ▀^│╠Ż¼öMČ■╝ē(j©¬)äė(d©░ng)┴”īW(xu©”)─Żą═Ą─ŽÓĻP(gu©Īn)ŽĄöĄ(sh©┤)(R2>0.999)Š∙├„’@Ė▀ė┌öMę╗╝ē(j©¬)äė(d©░ng)┴”īW(xu©”)─Żą═ĪŻę“┤╦Ż¼öMČ■╝ē(j©¬)äė(d©░ng)┴”īW(xu©”)ĘĮ│╠─▄Ė³║├Ą─├Ķ╩÷Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ▀^│╠Ż¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┤µį┌ČÓéĆ(g©©)╬³ĖĮļAČ╬Ż¼Ųõųą╬’└Ē╬³ĖĮ║═╗»īW(xu©”)╬³ĖĮ═¼Ģr(sh©¬)┤µį┌Ż¼ęį╗»īW(xu©”)╬³ĖĮ×ķų„ĪŻ
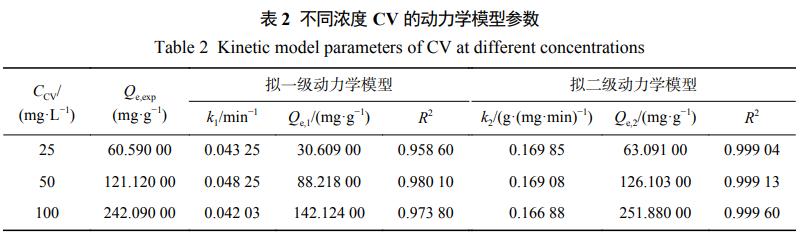
2.4 ╬³ĖĮĄ╚£žŠĆ蹊┐
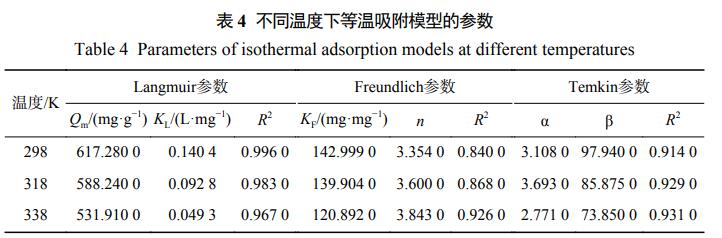
Ė∙ō■(j©┤)╩Į(4)Īó╩Į(5)Īó╩Į(6)ī”(du©¼)īŹ(sh©¬)“×(y©żn)╦∙Ą├öĄ(sh©┤)ō■(j©┤)▀M(j©¼n)ąą┴╦öM║ŽŻ¼öM║ŽĄ─ģóöĄ(sh©┤)╚ń▒Ē4╦∙╩ŠĪŻė╔▒Ē4┐╔ų¬Ż¼į┌3ĘN£žČ╚Śl╝■Ž┬Ż¼ė╔Langmuir─Żą═öM║ŽĄ─R2Š∙┤¾ė┌0.96Ż¼┤¾ė┌Freundlich║═Temkin─Żą═ĪŻ▀@šf├„Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ▀^│╠Ę¹║ŽLangmuir╬³ĖĮ─Żą═ĪŻė╔┤╦═Ų£y(c©©)Ż¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮī┘ė┌å╬Ęųūėīė╬³ĖĮĪŻį┌LangmuirĄ╚£ž╬³ĖĮųąŻ¼ļS£žČ╚Ą─╔²Ė▀Ż¼╬³ĖĮ┴┐║═KLŠ∙ėąŽ┬ĮĄŻ¼▒Ē├„Ą═£žėą└¹ė┌╬³ĖĮĄ─▀M(j©¼n)ąąĪŻį┌£žČ╚×ķ298KĢr(sh©¬)Ż¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┴┐ūŅ┤¾Ż¼×ķ617.28mgĪżg−1ĪŻ
2.5 ╬³ĖĮ¤ß┴”īW(xu©”)蹊┐
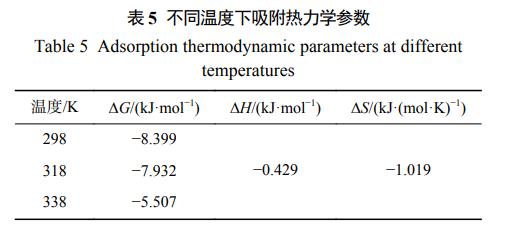
×ķĖ³▀M(j©¼n)ę╗▓Į蹊┐╬³ĖĮĄ─¤ß┴”īW(xu©”)ąį┘|(zh©¼)Ż¼Ė∙ō■(j©┤)╩Į(7)Īó╩Į(8)Īó╩Į(9)ėŗ(j©¼)╦Ń│÷▓╗═¼£žČ╚Ž┬Ą─╝¬▓╝╦╣ūįė╔─▄ūāĪóņ╩ūā║═ņžūāŻ¼ĮY(ji©”)╣¹╚ń▒Ē5╦∙╩ŠŻ¼┤┼ąį╦«─²─z╬³ĖĮä®į┌▓╗═¼£žČ╚Ž┬ī”(du©¼)CV╬³ĖĮ▀^│╠Ą─∆GŠ∙ąĪė┌┴ŃŻ¼šf├„╬³ĖĮ▀^│╠╩Ūūį░l(f©Ī)▀M(j©¼n)ąąĄ─Ż¼▓óŪę∆GļSų°£žČ╚Ą─╔²Ė▀Č°ūā┤¾Ż¼šf├„Ė▀£ž▓╗└¹ė┌╬³ĖĮĄ─▀M(j©¼n)ąąĪŻ∆H<0Ż¼šf├„╬³ĖĮ▀^│╠ī┘ė┌Ę┼¤ßŻ╗∆S<0Ż¼šf├„╬³ĖĮ▀^│╠╩ŪņžųĄ£pąĪĄ─▀^│╠ĪŻ
2.6 Fe3O4@LSĄ─┤┼ąį─▄║═ĮŌ╬³į┘╔·ąį─▄
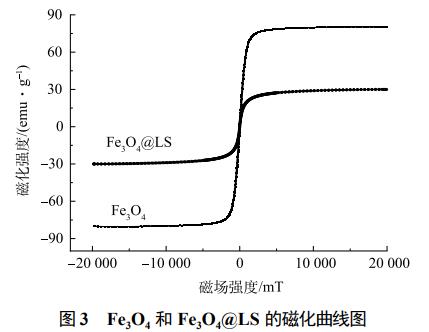
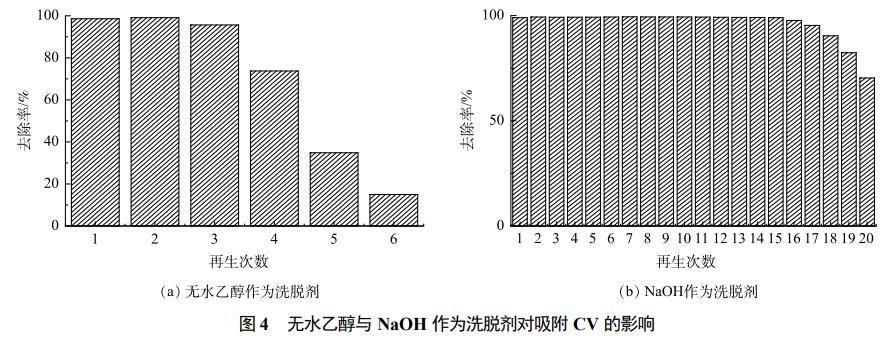
łD3×ķį┌│Ż£žŽ┬Ż¼╝āFe3O4Ę█─®┼cFe3O4@LSĄ─┤┼╗»Ū·ŠĆĪŻė╔łD3┐╔ęŖŻ¼Fe3O4@LSĄ─’¢║═┤┼ÅŖ(qi©óng)(30emuĪżg−1)╝s×ķ╝āFe3O4Ę█─®(80emuĪżg−1)Ą─38%ĪŻė╔┤┼╗»Ū·ŠĆ┐╔ęŖŻ¼2ĘNśėŲĘŠ∙╬┤│÷¼F(xi©żn)┤┼£■¼F(xi©żn)Ž¾Ż¼Č°Ūę╩Ż┤┼║═│CŅB┴”Š∙×ķ0Ż¼▒Ē├„└¹ė├įŁ╬╗│┴ĄĒĘ©║Ž│╔Ą─Fe3O4@LSŠ▀ėą│¼Ēś┤┼ąį╠žš„Ż¼ī”(du©¼)═Ō╝ė┤┼ł÷(ch©Żng)Š▀ėą┴╝║├Ą─Ēææ¬(y©®ng)─▄┴”Ż¼─▄ē“į┌═ŌĮń┤┼ł÷(ch©Żng)Ą─┤┼ąįū„ė├Ž┬īŹ(sh©¬)¼F(xi©żn)╣╠ę║Ęųļx║═╗ž╩š└¹ė├Ż¼▀@śėĄ─ąį┘|(zh©¼)ī”(du©¼)ė┌╬³ĖĮ▓─┴Žį┌īŹ(sh©¬)ļHæ¬(y©®ng)ė├ųąĄ─┐ņ╦┘╣╠ę║Ęųļx╝░ųžÅ═(f©┤)╗ž╩š└¹ė├Š∙Š▀ėąųžę¬ęŌ┴xĪŻė╔CV╚▄ę║pHī”(du©¼)╬³ĖĮąį─▄Ą─ė░Ēæ(łD2(a))┐╔ęį┐┤│÷Ż¼Fe3O4@LS▀mė├ė┌ųąąį╗“ēAąį╚▄ę║ū„×ķŽ┤├ōę║▀M(j©¼n)ąą├ōĖĮŻ¼ę“┤╦▒ŠīŹ(sh©¬)“×(y©żn)▀xė├¤o╦«ęę┤╝║═NaOH╚▄ę║ū„×ķŽ┤├ōä®ĪŻė╔łD4(a)┐╔ų¬Ż¼▓╔ė├¤o╦«ęę┤╝ū„×ķŽ┤├ō䮯¼ļSų°čŁŁh(hu©ón)┤╬öĄ(sh©┤)Ą─į÷╝ėŻ¼Fe3O4@LSį┌Ū░3┤╬į┘╔·Ą─╬³ĖĮą¦╣¹▌^║├Ż¼Č°į┌Ą┌4┤╬Ž┤├ō║¾Ż¼Fe3O4@LSĄ─╬³ĖĮą¦╣¹ėą╦∙Ž┬ĮĄĪŻŲõįŁę“┐╔─▄╩Ūę“?y©żn)ķŽ┤├ō裣h(hu©ón)┤╬öĄ(sh©┤)▀^ČÓŻ¼Fe3O4@LSĮY(ji©”)śŗ(g©░u)▒╗ŲŲē─Ż¼ī¦(d©Żo)ų┬╬³ĖĮ╬╗³c(di©Żn)ųØu£p╔┘ĪŻė╔łD4(b)┐╔ų¬Ż¼▓╔ė├NaOH╚▄ę║ū„×ķŽ┤├ō䮯¼«ö(d©Īng)į┘╔·┤╬öĄ(sh©┤)×ķ15Ģr(sh©¬)Ż¼Fe3O4@LS╚ź│²┬╩╚į┐╔▀_(d©ó)ĄĮ98%ęį╔ŽŻ¼Č°Fe3O4@LSį┌ČÓ┤╬╚▄├ø-║µĖ╔Ą─▀^│╠ųąėą▓┐Ęųōp╩¦Ż¼Å─Č°ī¦(d©Żo)ų┬į┘╔·┤╬öĄ(sh©┤)┤¾ė┌15┤╬║¾╚ź│²┬╩ėą╦∙Ž┬ĮĄĪŻ╔Ž╩÷ĮY(ji©”)╣¹šf├„NaOH╚▄ę║┐╔ęįėąą¦ĄžĮŌ╬³│÷Fe3O4@LS╬³ĖĮĄ─CVŻ¼▓óŪę▓╗Ģ■(hu©¼)ŲŲē─Fe3O4@LSĄ─ā╚(n©©i)▓┐ĮY(ji©”)śŗ(g©░u)Ż¼▒Ē├„Fe3O4@LSŠ▀ėą▌^║├Ą─┐╔裣h(hu©ón)└¹ė├ąį─▄ĪŻ
2.7 ╣▓┤µļxūėī”(du©¼)╬³ĖĮąį─▄Ą─ė░Ēæ
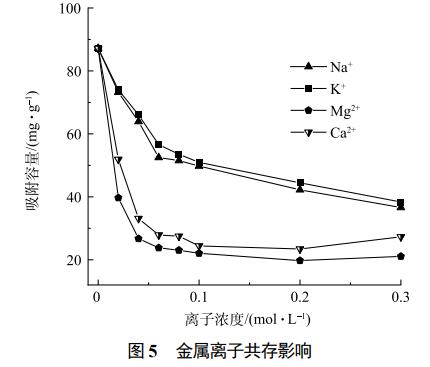
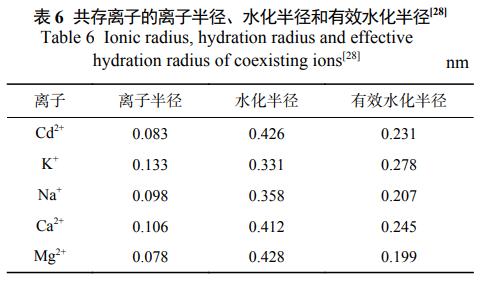
┐╝æ]ĄĮīŹ(sh©¬)ļHėĪ╚ŠÅU╦«ĮMĘųĄ─Å═(f©┤)ļsąįŻ¼┐╝▓ņ┴╦Įī┘ļxūėī”(du©¼)Fe3O4@LS╬³ĖĮąį─▄Ą─ė░ĒæĪŻė╔łD5┐╔ęŖŻ¼ļSų°╝ė╚ļĄ─Na+ĪóK+ĪóCa2+║═Mg2+ØŌČ╚į÷╝ėŻ¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┴┐│╩Ž┬ĮĄ┌ģä▌(sh©¼)Ż¼«ö(d©Īng)╬┤╝ė╚ļNa+ĪóK+ļxūėĢr(sh©¬)Ż¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┴┐×ķ87.18mgĪżg−1ĪŻ«ö(d©Īng)╝ė╚ļĄ─Na+ĪóK+ĪóCa2+║═Mg2+ļxūėØŌČ╚▀_(d©ó)ĄĮ0.3molĪżL−1Ģr(sh©¬)Ż¼Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ┴┐ĮĄ×ķ36.6Īó31.37Īó21.1Īó27.3mgĪżg−1ĪŻį┌ŽÓ═¼ØŌČ╚Śl╝■Ž┬Ż¼Č■ār(ji©ż)Ļ¢(y©óng)ļxūė(Ca2+║═Mg2+)Ą─ęųųŲū„ė├ÅŖ(qi©óng)ė┌ę╗ār(ji©ż)Ļ¢(y©óng)ļxūė(K+║═Na+)Ż¼ęųųŲū„ė├Ēśą“?y©żn)?/span>Mg2+>Ca2+>Na+>K+ĪŻį┌═¼ŅÉą═ļxūė╣▓┤µĄ─ŪķørŽ┬Ż¼ļxūėØŌČ╚įĮ┤¾Ż¼ī”(du©¼)CVĄ─ęųųŲū„ė├įĮ’@ų°Ż¼ī”(du©¼)CVĄ─╬³ĖĮ┴┐įĮĄ═ĪŻŲõįŁę“┐╔─▄╩Ū╬³ĖĮ䮥─╬³ĖĮĒśą“┼cļxūėĄ─ļŖ║╔öĄ(sh©┤)Īó╦«╗»─▄Īóļxūė░ļÅĮ║═ėąą¦╦«╗»░ļÅĮ├▄ŪąŽÓĻP(gu©Īn)ĪŻę╗░ŃŪķørŽ┬Ż¼ļŖ║╔ļxūėöĄ(sh©┤)┴┐įĮČÓŻ¼░ļÅĮįĮąĪŻ¼Ėé(j©¼ng)ĀÄ(zh©źng)╬³ĖĮ─▄┴”įĮÅŖ(qi©óng)ĪŻę“┤╦Ż¼į┌ŽÓ═¼ØŌČ╚Ž┬Ż¼Č■ār(ji©ż)ļxūė(Ca2+║═Mg2+)ī”(du©¼)CVĄ─╬³ĖĮęųųŲū„ė├ÅŖ(qi©óng)ė┌ę╗ār(ji©ż)ļxūė(K+║═Na+)ĪŻ╚ń▒Ē6╦∙╩ŠŻ¼«ö(d©Īng)ļŖ║╔öĄ(sh©┤)ŽÓ═¼Ģr(sh©¬)Ż¼ėąą¦╦«╗»░ļÅĮę└┤╬×ķMg2+<Ca2+<Na+<K+ĪŻę“┤╦Ż¼ī”(du©¼)CVĄ─╬³ĖĮęųųŲĒśą“?y©żn)?/span>Mg2+>Ca2+>Na+>K+ĪŻ
2.8 ┼cŲõ╦¹▓─┴Ž╬³ĖĮCVĄ─ą¦╣¹▒╚▌^
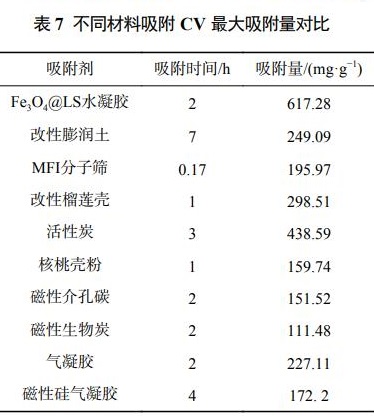
īó▒ŠčąŠ┐║Ž│╔Ą─┤┼ąįFe3O4@LS╦«─²─z┼cŲõ╦¹╬─½I(xi©żn)ųą╬³ĖĮCV╦∙╩╣ė├Ą─▓─┴Ž▀M(j©¼n)ąąī”(du©¼)▒╚Ż¼ęįūŅ┤¾╬³ĖĮ┴┐ū„×ķī”(du©¼)▒╚ę└ō■(j©┤)ĪŻ▒╚▌^ĮY(ji©”)╣¹╚ń▒Ē7╦∙╩ŠŻ¼░l(f©Ī)¼F(xi©żn)┤┼ąįFe3O4@LS╦«─²─zī”(du©¼)ė┌CVĄ─╬³ĖĮąį─▄├„’@ā×(y©Łu)ė┌Ųõ╦¹▓─┴ŽŻ¼šf├„┤┼ąįFe3O4@LS╦«─²─zį┌CV╚Š┴ŽÅU╦«╠Ä└Ē╔ŽŠ▀ėąśO┤¾Ą─ā×(y©Łu)ä▌(sh©¼)║═æ¬(y©®ng)ė├Ū░Š░ĪŻ
3ĪóĮY(ji©”)šō
1)ŽÓ▒╚ė┌LSŻ¼Fe3O4@LS┐╔╠ß╣®Ė³ČÓĄ─╬³ĖĮ╬╗³c(di©Żn)Ż¼▓óŪęFe3O4@LSŠ▀ėą▒╚LSĖ³┤¾Ą─▒╚▒Ē├µĘeŻ¼Ė³ėą└¹ė┌╗Ņąį╬╗³c(di©Żn)Ą─▒®┬ČŻ¼▀@ą®ā×(y©Łu)ä▌(sh©¼)ėą└¹ė┌╠ßĖ▀╬³ĖĮąį─▄ĪŻ
2)Fe3O4@LS╬³ĖĮĮY(ji©”)Š¦ūŽĄ─ūŅ╝čŚl╝■×ķŻ║į┌25ĪµŽ┬ĪóFe3O4@LS═Č╝ė┴┐×ķ400mgĪżL−1ĪóCVÅU╦«pH=7.0ĪóCV│§╩╝ØŌČ╚×ķ100mgĪżL−1Īó╬³ĖĮĢr(sh©¬)ķg80minŻ¼┤╦Śl╝■Ž┬Ż¼ī”(du©¼)CVĄ─ŲĮ║Ō╬³ĖĮ┴┐║═╚ź│²┬╩Ęųäe×ķ237.08mgĪżg−1║═94.83%ĪŻ
3)Fe3O4@LSī”(du©¼)CVĄ─╬³ĖĮ▀^│╠Ę¹║ŽöMČ■╝ē(j©¬)äė(d©░ng)┴”īW(xu©”)ĘĮ│╠╝░Langmuir╬³ĖĮ─Żą═Ż¼Fe3O4@LS╦«─²─zī”(du©¼)CVĄ─╬³ĖĮī┘ė┌ęį╗»īW(xu©”)╬³ĖĮ×ķų„Ūę×ķå╬Ęųūėīė╬³ĖĮĪŻš¹éĆ(g©©)╬³ĖĮ▀^│╠╩Ūūį░l(f©Ī)▀M(j©¼n)ąąĄ─Ż¼╣Ø(ji©”)─▄▒Ń└¹ĪŻ
4)▓╔ė├NaOH╚▄ę║ū„×ķŽ┤├ō䮯¼«ö(d©Īng)į┘╔·┤╬öĄ(sh©┤)×ķ10Ģr(sh©¬)Ż¼Fe3O4@LS╚ź│²┬╩╚į┐╔▀_(d©ó)ĄĮ98%ęį╔ŽŻ¼šf├„Fe3O4@LSŠ▀ėą║▄║├Ą─裣h(hu©ón)└¹ė├ąį─▄ĪŻ
5)ę╗ār(ji©ż)║═Č■ār(ji©ż)Įī┘ļxūėŠ∙ī”(du©¼)CVĄ─╬³ĖĮėąęųųŲū„ė├Ż¼┼cNa+ĪóK+ļxūėŽÓ▒╚Ż¼Ca2+║═Mg2+ļxūėī”(du©¼)╬³ĖĮĄ─ęųųŲū„ė├Ė³×ķ├„’@Ż¼ęųųŲĒśą“?y©żn)?/span>Mg2+>Ca2+>Na+>K+Ż¼╣▓┤µļxūėī”(du©¼)╬³ĖĮĄ─ė░Ēæ┼cŲõ╗»║Žār(ji©ż)ęį╝░ļxūėĄ─╦«║Ž░ļÅĮĄ╚ąį┘|(zh©¼)ėąĻP(gu©Īn)ĪŻŻ©üĒį┤Ż║ķL(zh©Żng)ĮŁ┤¾īW(xu©”)╗»īW(xu©”)┼cŁh(hu©ón)Š│╣ż│╠īW(xu©”)į║Ż®



